Ci Dice Come è Formata Una Molecola

Quante volte ti sei trovato a fissare un esercizio di chimica, chiedendoti: "Ma come fanno gli atomi a mettersi insieme? Cosa li spinge a formare queste molecole complesse?". Non sei solo! La formazione delle molecole è un concetto fondamentale, ma spesso percepito come ostico. Questo articolo è qui per aiutarti a navigare questo affascinante mondo, rendendolo accessibile e comprensibile.
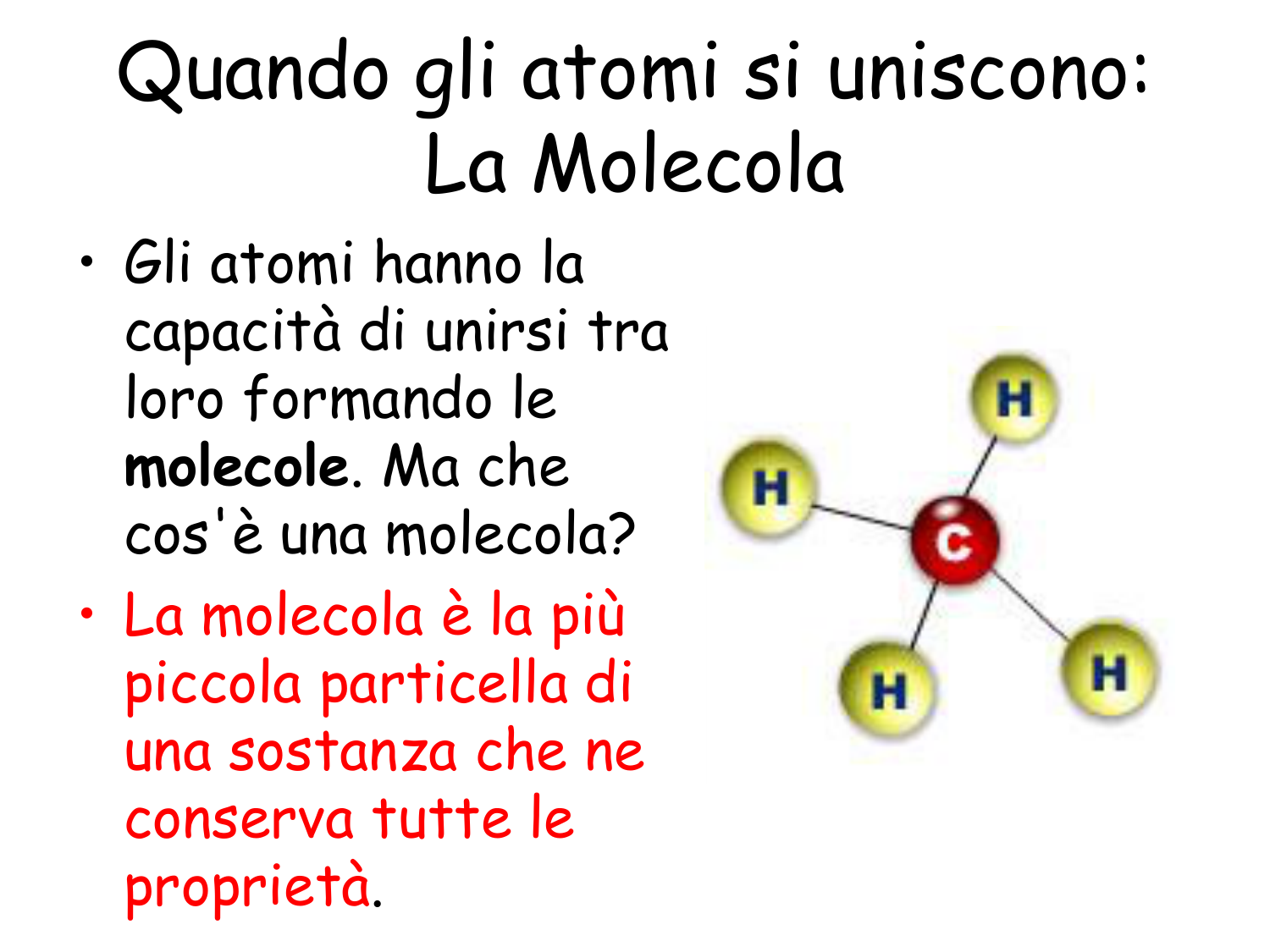
Cosa Sono Esattamente le Molecole?
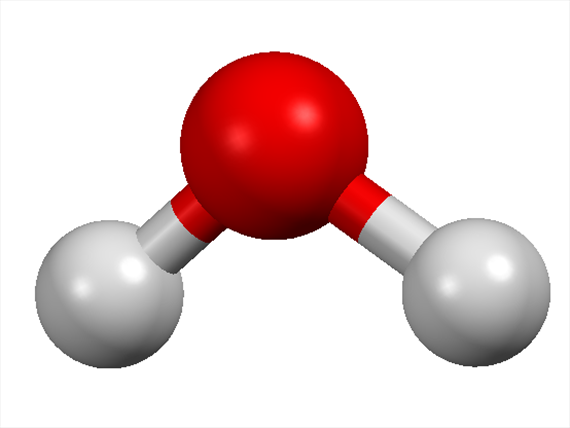
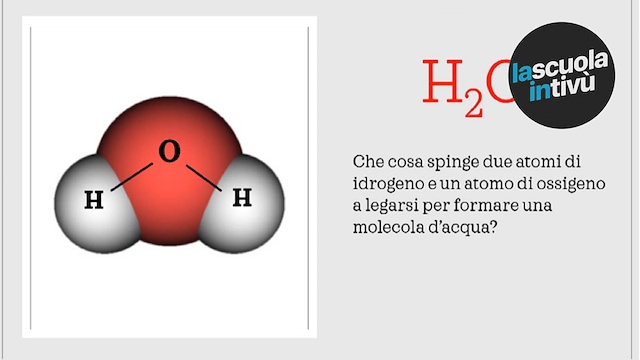
Una molecola è, in termini semplici, un gruppo di due o più atomi tenuti insieme da legami chimici. Questi legami sono forze attrattive che mantengono gli atomi uniti, creando una "unità" stabile. Pensa all'acqua (H₂O): due atomi di idrogeno si legano a un atomo di ossigeno per formare la molecola che conosciamo e amiamo (e di cui abbiamo bisogno per vivere!).
Come afferma il famoso chimico Linus Pauling, premio Nobel per la Chimica, "Le proprietà di una sostanza dipendono dalle molecole che la compongono e dal modo in cui queste molecole sono disposte". Questa frase sottolinea l'importanza cruciale delle molecole per comprendere il mondo che ci circonda.
Must Read
La Chiave: Gli Elettroni di Valenza
Per capire come si formano i legami, dobbiamo concentrarci sugli elettroni di valenza. Cosa sono? Sono gli elettroni presenti nell'ultimo livello energetico (guscio) di un atomo. Questi elettroni sono i protagonisti principali quando si tratta di formare legami.
Ogni atomo "desidera" avere un guscio di valenza completo, ovvero raggiungere una configurazione elettronica stabile, simile a quella dei gas nobili (elio, neon, argon, etc.). Questi elementi sono inerti, cioè non tendono a reagire, perché hanno già un guscio di valenza completo. La "regola dell'ottetto" (più un'approssimazione che una regola ferrea, ma utile per iniziare) afferma che gli atomi tendono a combinarsi in modo da avere otto elettroni nel loro guscio di valenza.

I Diversi Tipi di Legami Chimici
Esistono diversi tipi di legami chimici, ognuno con le proprie caratteristiche. I più comuni sono:
- Legame Ionico: Si forma quando un atomo cede uno o più elettroni a un altro atomo. Questo crea ioni: atomi con una carica elettrica positiva (cationi) o negativa (anioni). L'attrazione elettrostatica tra ioni di carica opposta genera il legame. Un esempio classico è il cloruro di sodio (NaCl), il comune sale da cucina. Il sodio (Na) cede un elettrone al cloro (Cl), formando Na⁺ e Cl⁻, che si attraggono reciprocamente.
- Legame Covalente: Si forma quando due atomi condividono uno o più elettroni. Questo permette a entrambi gli atomi di raggiungere una configurazione elettronica più stabile. L'acqua (H₂O) è un esempio di molecola con legami covalenti. Ogni atomo di idrogeno condivide un elettrone con l'atomo di ossigeno.
- Legame Metallico: Presente nei metalli, si basa sulla "condivisione" di elettroni di valenza tra molti atomi. Gli elettroni formano una sorta di "mare" in cui gli ioni metallici sono immersi. Questo spiega perché i metalli sono buoni conduttori di elettricità e calore.
Legami Covalenti: Ancora Più nel Dettaglio
All'interno dei legami covalenti, possiamo distinguere:
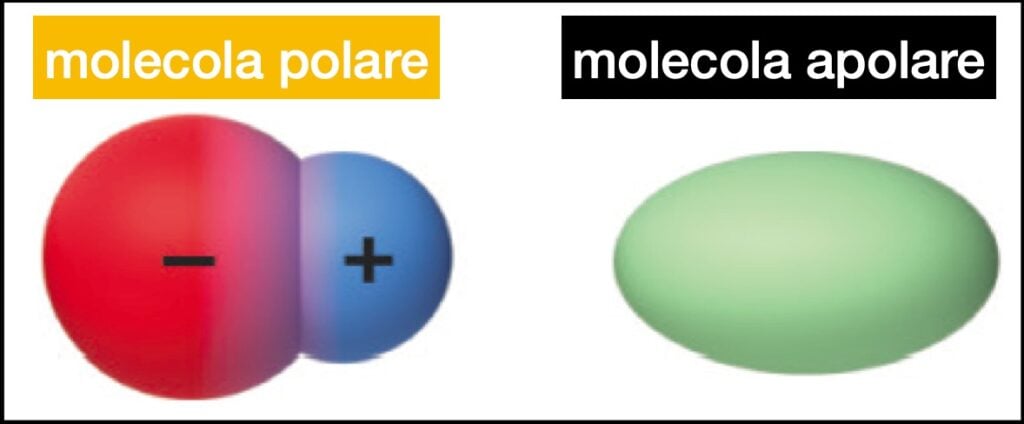
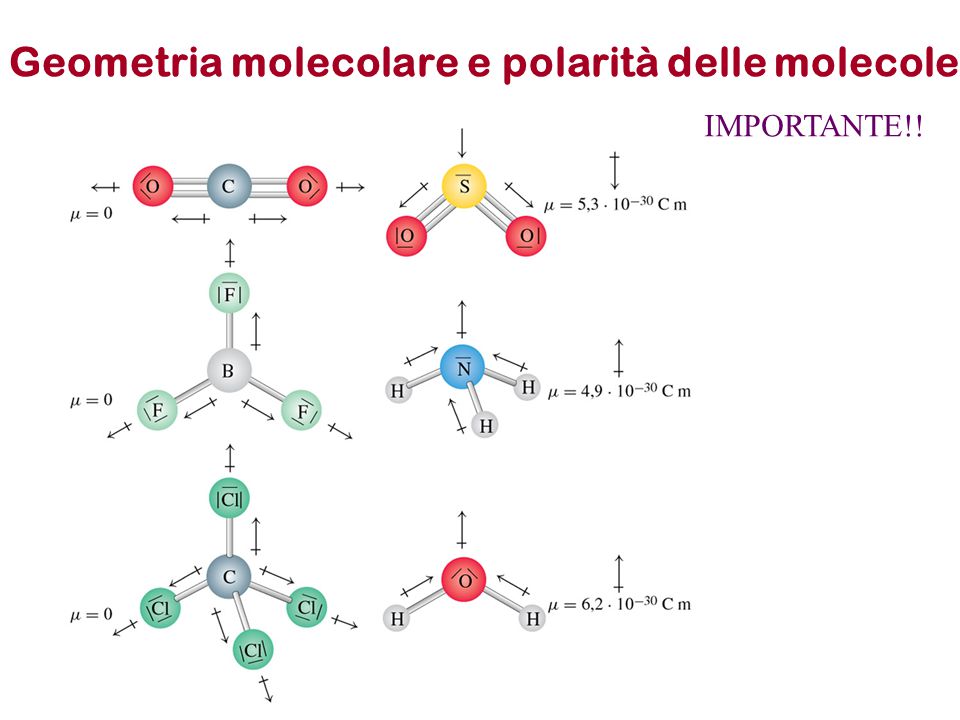
- Legame Covalente Puro (o Non Polare): Gli elettroni sono condivisi equamente tra i due atomi. Questo accade quando i due atomi hanno la stessa elettronegatività (la capacità di attrarre gli elettroni). Un esempio è la molecola di idrogeno (H₂).
- Legame Covalente Polare: Gli elettroni sono condivisi inequamente tra i due atomi. Questo accade quando i due atomi hanno elettronegatività diverse. L'atomo più elettronegativo attira gli elettroni verso di sé, creando una parziale carica negativa (δ⁻) e l'altro atomo una parziale carica positiva (δ⁺). L'acqua (H₂O) è un esempio. L'ossigeno è più elettronegativo dell'idrogeno, quindi attira gli elettroni verso di sé, creando una parziale carica negativa sull'ossigeno e parziali cariche positive sugli idrogeni. Questa polarità rende l'acqua un ottimo solvente.
Come Prevedere la Formazione di un Legame
Prevedere il tipo di legame che si formerà tra due atomi dipende principalmente dalla loro elettronegatività. Una grande differenza di elettronegatività porta alla formazione di un legame ionico, mentre una piccola differenza porta alla formazione di un legame covalente polare o non polare. Esistono tabelle di elettronegatività che puoi consultare per fare queste previsioni.

Un'altra regola pratica è considerare la posizione degli elementi nella tavola periodica. Gli elementi del gruppo 1 (metalli alcalini) tendono a formare legami ionici con gli elementi del gruppo 17 (alogeni).
Strumenti e Metodi per Visualizzare le Molecole
Visualizzare le molecole può aiutarti a comprendere meglio la loro struttura e i legami che le tengono insieme. Ecco alcuni strumenti e metodi:
- Modelli Molecolari: Puoi utilizzare kit di modelli molecolari fisici per costruire le molecole. Questi kit ti permettono di visualizzare la disposizione degli atomi nello spazio.
- Software di Modellazione Molecolare: Esistono numerosi software gratuiti o a pagamento che permettono di visualizzare le molecole in 3D. Alcuni esempi sono Avogadro, ChemDraw, e PyMOL.
- Diagrammi di Lewis: Questi diagrammi rappresentano gli atomi e i loro elettroni di valenza, mostrando i legami che si formano. Sono un ottimo modo per visualizzare la condivisione degli elettroni nei legami covalenti.
Esempi Pratici: Come Si Formano Alcune Molecole Comuni
Vediamo alcuni esempi di come si formano alcune molecole comuni:
- Acqua (H₂O): L'ossigeno ha 6 elettroni di valenza e ha bisogno di 2 elettroni per completare il suo ottetto. Ogni atomo di idrogeno ha 1 elettrone di valenza e ha bisogno di 1 elettrone per completare il suo duetto (nel caso dell'idrogeno e dell'elio, la regola dell'ottetto si applica raggiungendo 2 elettroni, non 8). Ogni atomo di idrogeno condivide un elettrone con l'ossigeno, formando due legami covalenti polari.
- Anidride Carbonica (CO₂): Il carbonio ha 4 elettroni di valenza e ha bisogno di 4 elettroni per completare il suo ottetto. Ogni atomo di ossigeno ha 6 elettroni di valenza e ha bisogno di 2 elettroni per completare il suo ottetto. Il carbonio condivide due elettroni con ogni atomo di ossigeno, formando due legami covalenti doppi.
- Metano (CH₄): Il carbonio ha 4 elettroni di valenza e ha bisogno di 4 elettroni per completare il suo ottetto. Ogni atomo di idrogeno ha 1 elettrone di valenza e ha bisogno di 1 elettrone per completare il suo duetto. Il carbonio condivide un elettrone con ogni atomo di idrogeno, formando quattro legami covalenti.
Consigli Utili per Approfondire
- Esercitati a disegnare i diagrammi di Lewis: Questo ti aiuterà a visualizzare la formazione dei legami.
- Usa i modelli molecolari: Manipolare fisicamente le molecole ti aiuterà a capire la loro struttura tridimensionale.
- Studia la tavola periodica: Comprendere le proprietà degli elementi ti aiuterà a prevedere il tipo di legame che si formerà.
- Non aver paura di chiedere aiuto: Se hai difficoltà, chiedi al tuo insegnante o a un tutor.
La comprensione di come si formano le molecole è un passo fondamentale per padroneggiare la chimica. Con un po' di impegno e i giusti strumenti, sarai in grado di comprendere e apprezzare la bellezza e la complessità del mondo molecolare. Ricorda che la chimica è ovunque intorno a noi!
Come diceva Madame Curie: "Non bisogna aver paura di niente nella vita, bisogna solo capire".