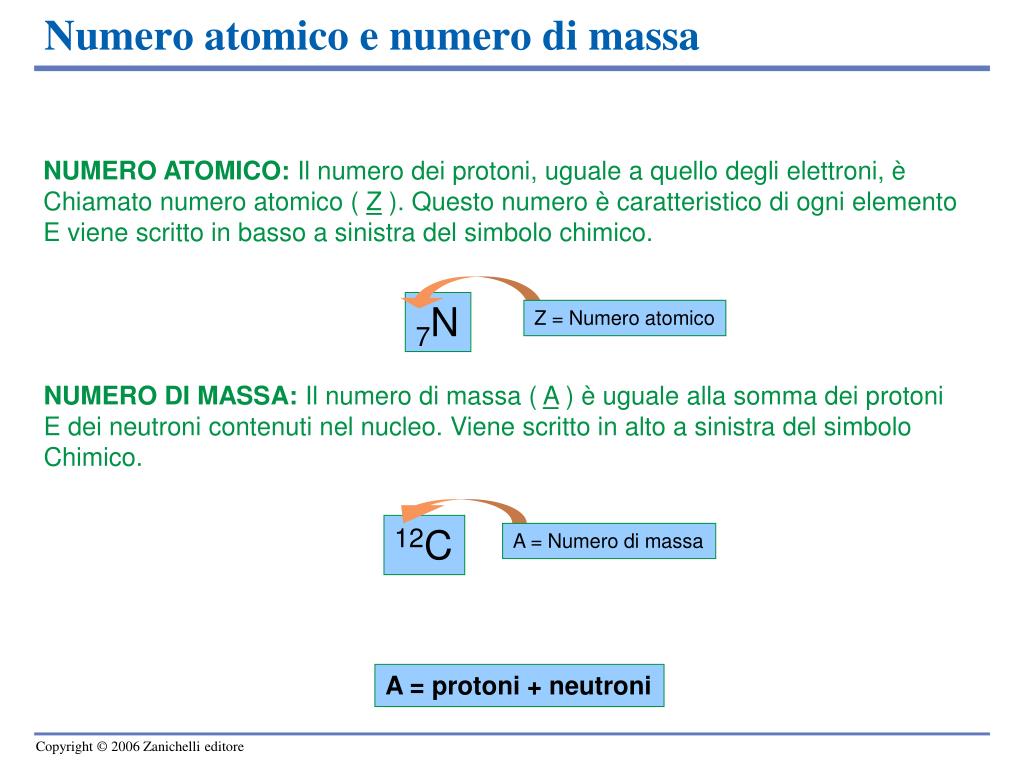
Come Calcolare Il Numero Di Atomi In Un Elemento
Capita a tutti: guardi un problema di chimica e ti senti perso. Calcolare il numero di atomi in un elemento può sembrare ostico, soprattutto quando ti imbatti in termini come "mole", "massa molare" e numeri enormi. Ma non preoccuparti, siamo qui per semplificare le cose e rendere questo concetto accessibile a tutti. Vedremo insieme come affrontare questi calcoli, passo dopo passo, con esempi pratici e un linguaggio chiaro.
Comprendere i Concetti Fondamentali
Prima di tuffarci nei calcoli, è essenziale avere ben chiari alcuni concetti base:
Cos'è una Mole?
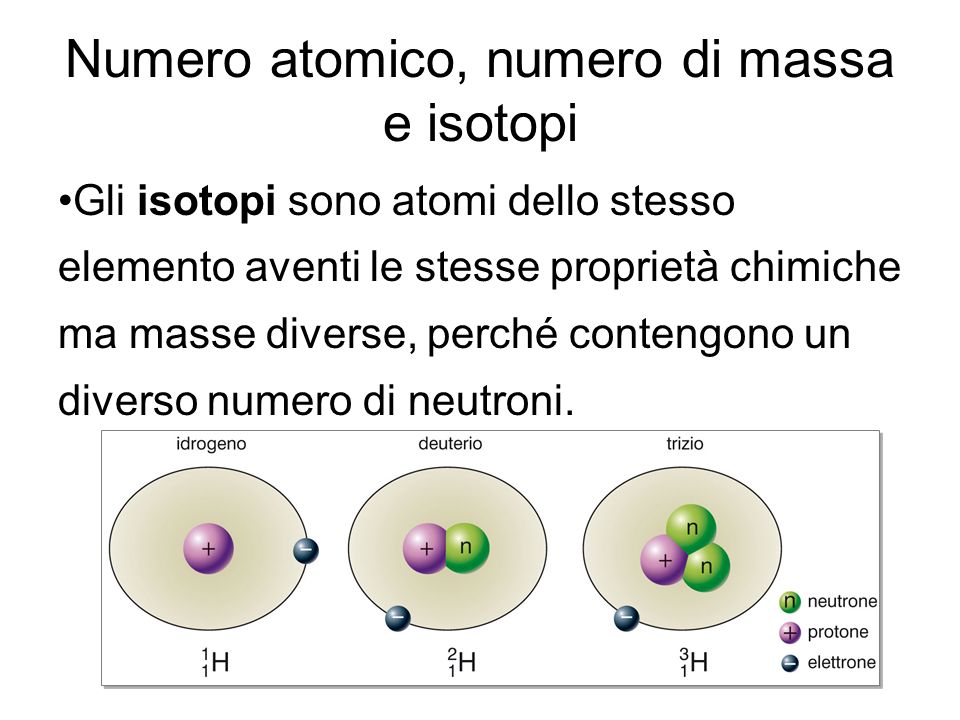
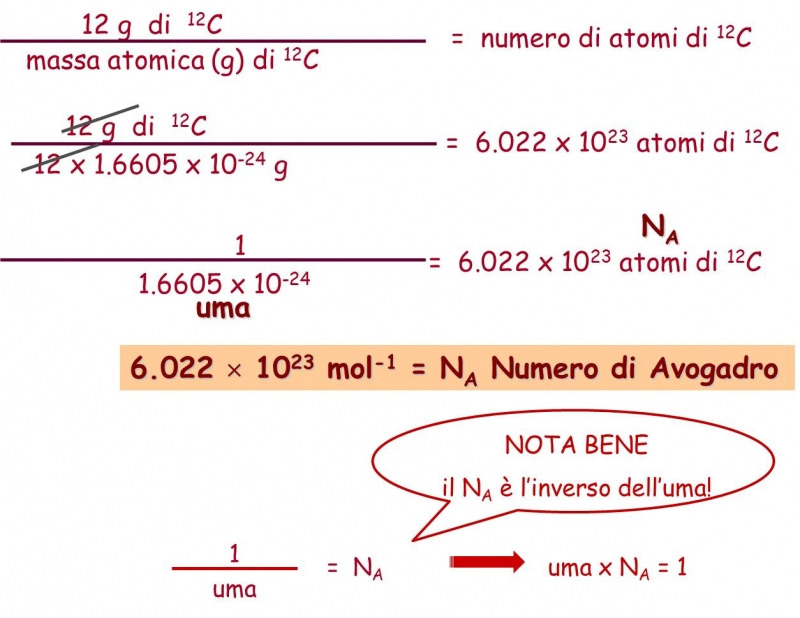
Immagina di dover contare un'enorme quantità di fagioli. Invece di contarli uno a uno, potresti raggrupparli in sacchi da, diciamo, 1000 fagioli ciascuno. La mole è un po' come quel sacco: è un'unità di misura che rappresenta una quantità specifica di particelle (atomi, molecole, ioni, ecc.). In particolare, una mole contiene 6.022 x 1023 particelle. Questo numero magico è chiamato Numero di Avogadro.
Must Read
Massa Molare: Il Peso di una Mole
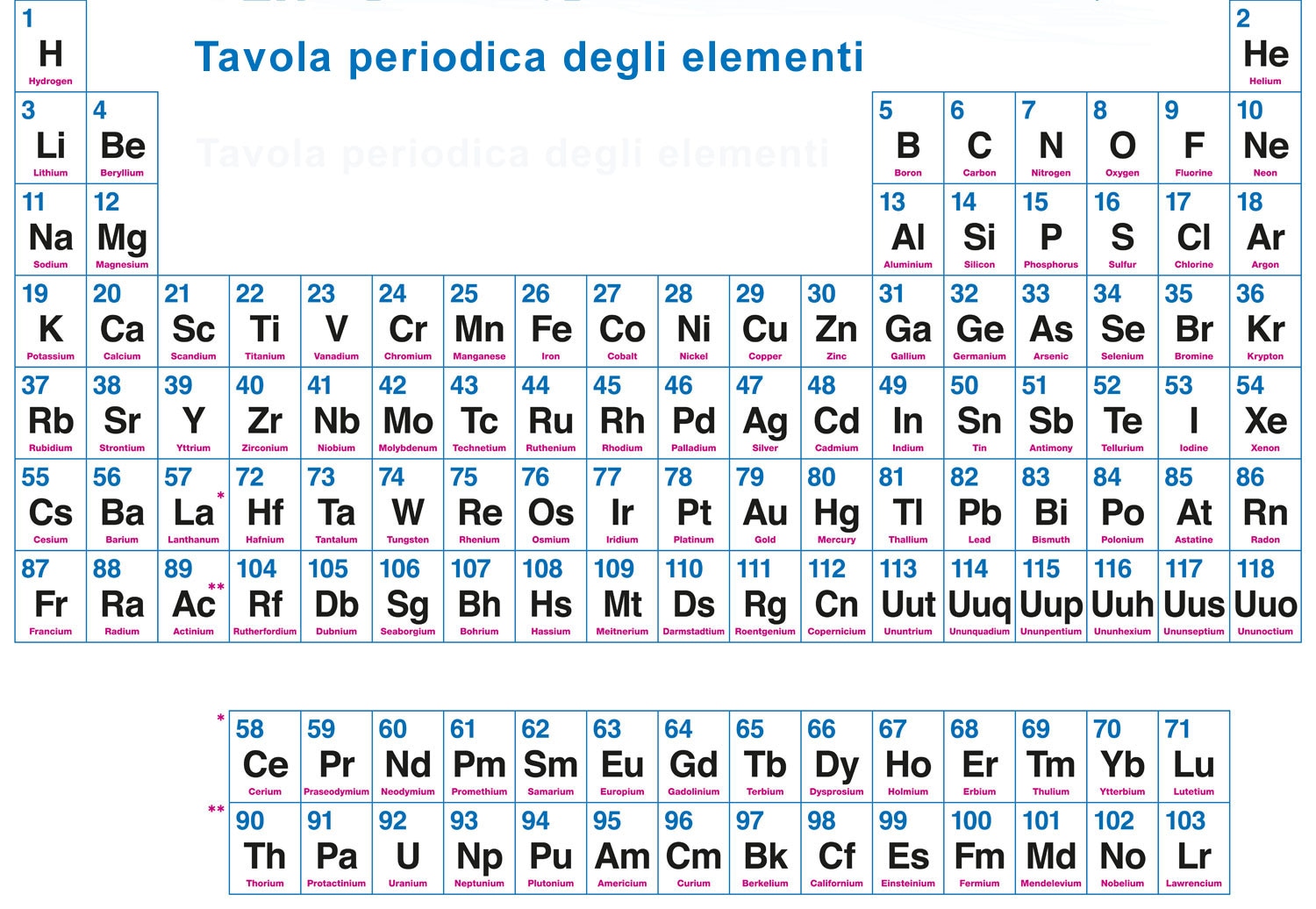
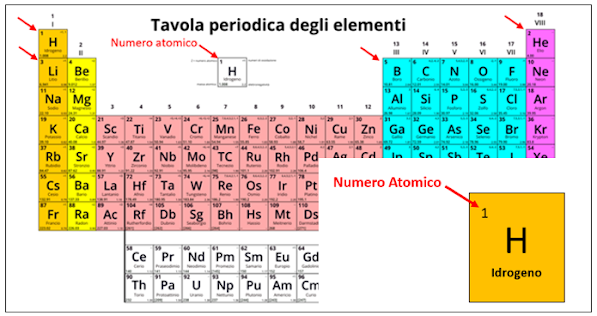
La massa molare è la massa in grammi di una mole di una sostanza. La puoi trovare facilmente sulla tavola periodica degli elementi, sotto il simbolo di ciascun elemento. Ad esempio, la massa molare del carbonio (C) è circa 12.01 g/mol. Ciò significa che una mole di atomi di carbonio pesa 12.01 grammi.
Calcolare il Numero di Atomi: Passo dopo Passo
Ora che abbiamo definito i concetti chiave, vediamo come calcolare il numero di atomi in un elemento:
- Identifica la massa del campione. Il problema ti fornirà la massa dell'elemento, ad esempio "10 grammi di ferro".
- Trova la massa molare dell'elemento. Consulta la tavola periodica per la massa molare. Per il ferro (Fe), è circa 55.85 g/mol.
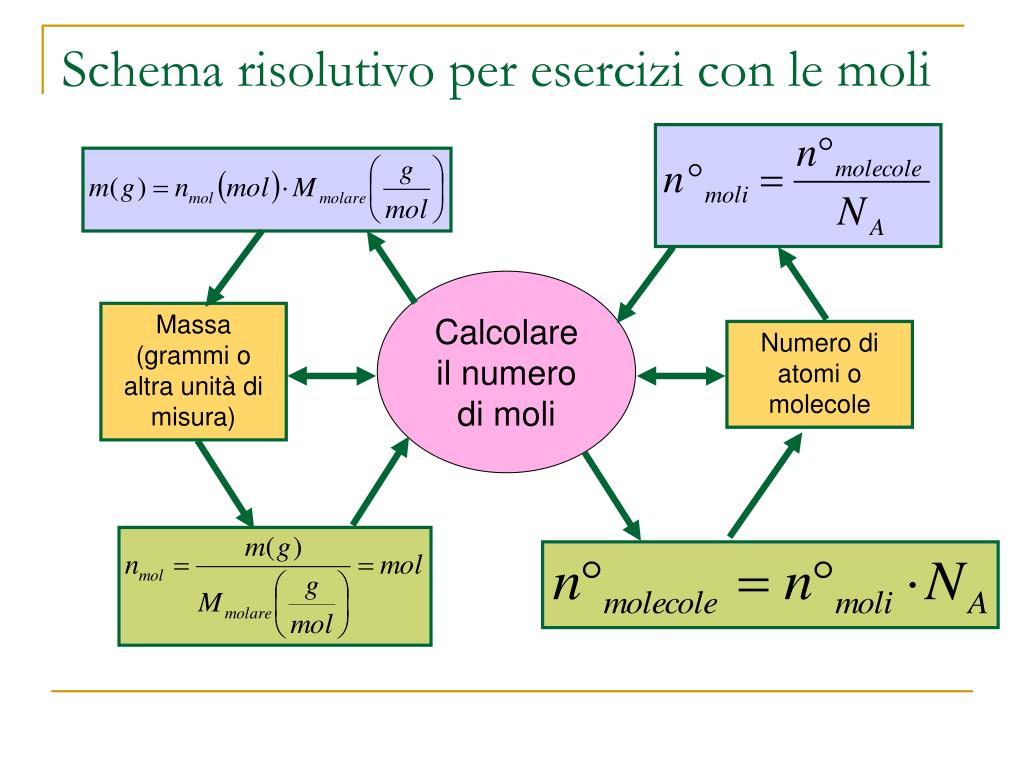
- Calcola il numero di moli. Dividi la massa del campione per la massa molare. Numero di moli = Massa del campione / Massa molare. Nell'esempio del ferro: 10 g / 55.85 g/mol ≈ 0.179 moli.
- Calcola il numero di atomi. Moltiplica il numero di moli per il Numero di Avogadro. Numero di atomi = Numero di moli x Numero di Avogadro. Per il ferro: 0.179 moli x 6.022 x 1023 atomi/mole ≈ 1.08 x 1023 atomi.
Quindi, in 10 grammi di ferro, ci sono circa 1.08 x 1023 atomi di ferro.
Esempio Pratico
Calcoliamo il numero di atomi in 5 grammi di oro (Au).
- Massa del campione: 5 g
- Massa molare dell'oro: 196.97 g/mol (dalla tavola periodica)
- Numero di moli: 5 g / 196.97 g/mol ≈ 0.025 moli
- Numero di atomi: 0.025 moli x 6.022 x 1023 atomi/mole ≈ 1.51 x 1022 atomi
In 5 grammi di oro, ci sono circa 1.51 x 1022 atomi di oro.
Consigli e Trucchi
- Fai attenzione alle unità di misura. Assicurati che la massa del campione e la massa molare siano espresse nelle unità corrette (grammi e grammi/mole, rispettivamente).
- Scrivi tutti i passaggi. Questo ti aiuterà a evitare errori e a capire meglio il processo.
- Usa la calcolatrice scientifica. Maneggiare numeri esponenziali richiede una calcolatrice scientifica.
- Esercitati! Più ti eserciti, più diventerai bravo.
Calcolare il numero di atomi in un elemento può sembrare difficile all'inizio, ma con la pratica e la comprensione dei concetti base, diventerà un'abilità che ti tornerà utile in molti ambiti della chimica. Non scoraggiarti di fronte alle difficoltà: ogni problema risolto è un passo avanti verso la comprensione!