Come Calcolare La Concentrazione Di Una Soluzione

Quante volte ti sei trovato davanti a un compito di chimica, con una provetta in mano e la sensazione di non capire assolutamente come calcolare la concentrazione di quella soluzione misteriosa? Non sei solo! Molti studenti, e anche professionisti all'inizio della loro carriera, si scontrano con questa sfida. Ma non temere, imparare a calcolare la concentrazione è più semplice di quanto sembri. Prendiamoci per mano e scopriamo insieme come fare, passo dopo passo.
Cos'è la Concentrazione? Una Definizione Chiara
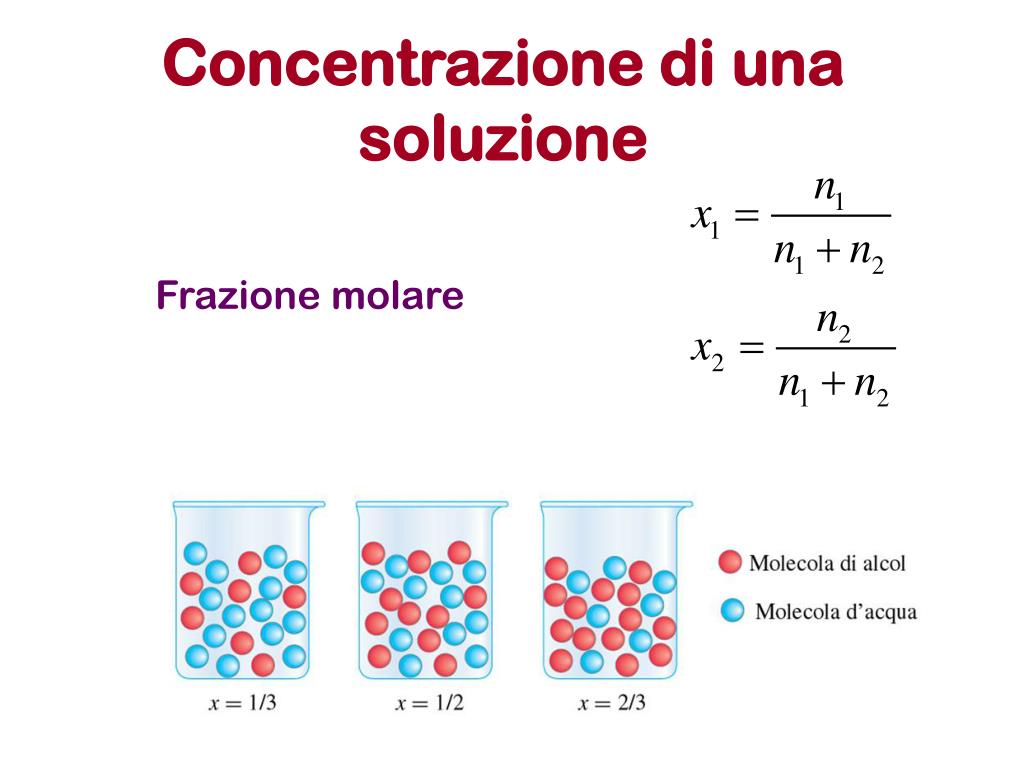
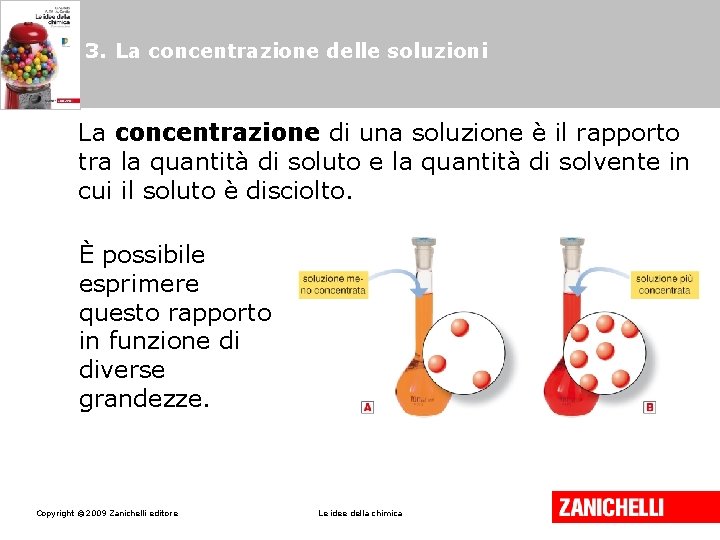
Prima di immergerci nei calcoli, cerchiamo di capire cosa significa "concentrazione". Immagina di preparare una limonata. Se metti poco succo di limone, la limonata sarà leggera, poco concentrata. Se invece ne metti tanto, sarà forte, molto concentrata. In chimica, la concentrazione esprime la quantità di soluto (il limone) presente in una determinata quantità di solvente (l'acqua) o di soluzione (la limonata).
Come spiega la Professoressa Maria Rossi, docente di Chimica all'Università di Bologna, "La concentrazione è una proprietà fondamentale delle soluzioni e ne determina molte delle loro caratteristiche chimiche e fisiche."
Must Read
Unità di Misura della Concentrazione: Orientarsi nel Labirinto
Esistono diverse unità di misura per esprimere la concentrazione. Conoscerle è fondamentale per scegliere quella giusta in base al problema che devi risolvere.
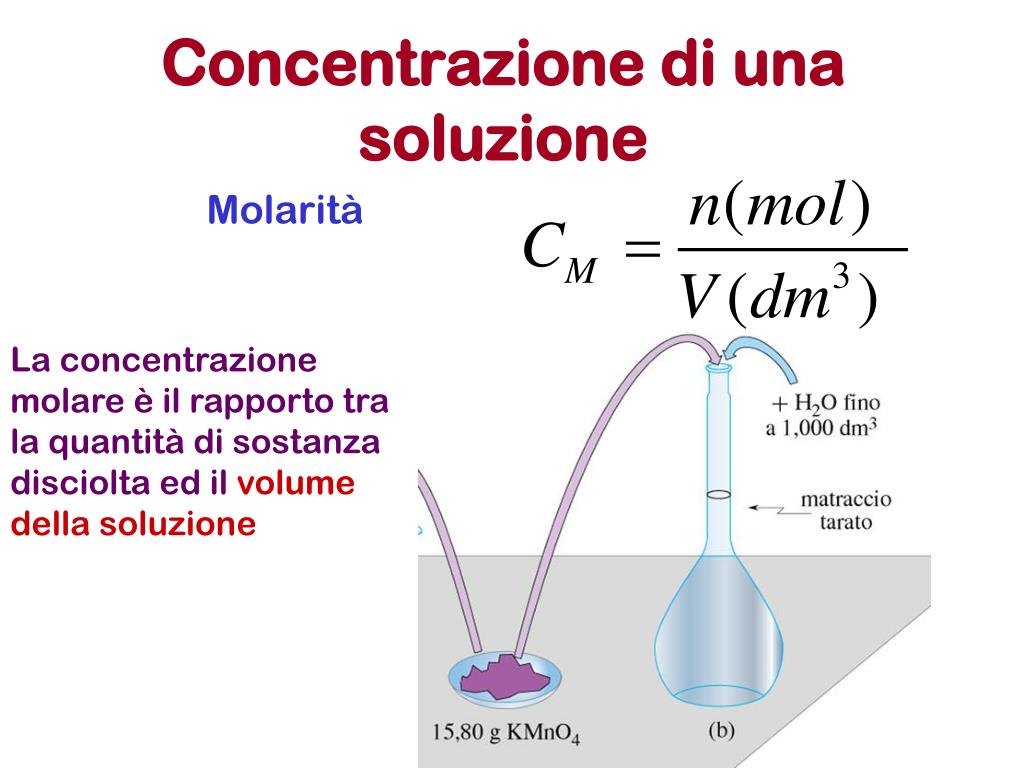
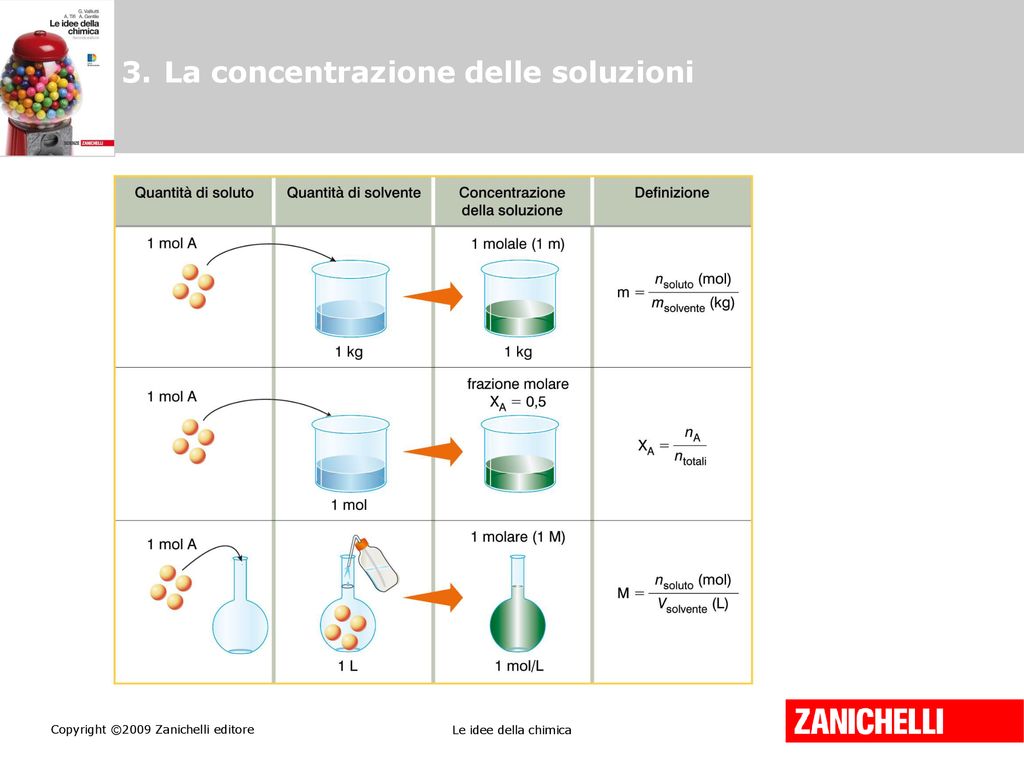
- Molarità (M): Definisce il numero di moli di soluto per litro di soluzione (mol/L). È una delle unità più utilizzate in laboratorio.
- Molalità (m): Indica il numero di moli di soluto per chilogrammo di solvente (mol/kg). È utile quando la temperatura varia, perché il volume della soluzione può cambiare, a differenza della massa del solvente.
- Percentuale in massa (% m/m): Esprime la massa del soluto in grammi per 100 grammi di soluzione. Ad esempio, una soluzione al 5% m/m contiene 5 grammi di soluto in 100 grammi di soluzione.
- Percentuale in volume (% v/v): Indica il volume del soluto in millilitri per 100 millilitri di soluzione. Viene spesso usata per soluzioni liquide.
- Parti per milione (ppm): Esprime la quantità di soluto per milione di parti di soluzione. È utile per concentrazioni molto basse, ad esempio per misurare la quantità di inquinanti in acqua.
Un consiglio: cerca di memorizzare le definizioni di queste unità di misura. Ti aiuterà a capire meglio i problemi e a scegliere la formula giusta per risolverli.
Come Calcolare la Molarità (M): Esempio Pratico
La molarità è una delle unità di concentrazione più utilizzate, quindi impariamo a calcolarla con un esempio pratico:
Esempio: Calcola la molarità di una soluzione preparata sciogliendo 4 grammi di idrossido di sodio (NaOH) in acqua fino a ottenere un volume finale di 500 mL.
Passo 1: Calcola il numero di moli di soluto.
Per fare questo, hai bisogno della massa molare dell'NaOH. La massa molare è la somma delle masse atomiche degli elementi che compongono la molecola. Per l'NaOH, è circa 40 g/mol (Na: 23 g/mol, O: 16 g/mol, H: 1 g/mol).
Numero di moli di NaOH = massa di NaOH / massa molare di NaOH = 4 g / 40 g/mol = 0.1 mol
Passo 2: Converti il volume della soluzione in litri.

500 mL = 0.5 L
Passo 3: Calcola la molarità.
Molarità (M) = numero di moli di soluto / volume della soluzione in litri = 0.1 mol / 0.5 L = 0.2 mol/L = 0.2 M
Quindi, la molarità della soluzione è 0.2 M.
Consiglio pratico: Usa sempre le unità di misura corrette. Se sbagli le unità, il risultato sarà sbagliato.
Calcolo della Molalità (m): Un Esempio Guidato
Vediamo ora come calcolare la molalità, un'altra unità di concentrazione importante, soprattutto quando la temperatura gioca un ruolo significativo.
Esempio: Calcola la molalità di una soluzione ottenuta sciogliendo 10 grammi di glucosio (C6H12O6) in 200 grammi di acqua.
Passo 1: Calcola il numero di moli di soluto.
La massa molare del glucosio è circa 180 g/mol.

Numero di moli di glucosio = massa di glucosio / massa molare di glucosio = 10 g / 180 g/mol = 0.0556 mol (circa)
Passo 2: Converti la massa del solvente in chilogrammi.
200 g = 0.2 kg
Passo 3: Calcola la molalità.
Molalità (m) = numero di moli di soluto / massa del solvente in chilogrammi = 0.0556 mol / 0.2 kg = 0.278 mol/kg = 0.278 m (circa)
Quindi, la molalità della soluzione è circa 0.278 m.
Percentuale in Massa e Volume: Calcoli Semplici
Le percentuali in massa e volume sono relativamente semplici da calcolare. Ecco come fare:
Percentuale in Massa (% m/m)
Formula: % m/m = (massa del soluto / massa della soluzione) * 100

Esempio: Una soluzione è preparata sciogliendo 25 grammi di sale in 100 grammi di acqua. Qual è la percentuale in massa della soluzione?
Massa della soluzione = massa del soluto + massa del solvente = 25 g + 100 g = 125 g
% m/m = (25 g / 125 g) * 100 = 20%
Percentuale in Volume (% v/v)
Formula: % v/v = (volume del soluto / volume della soluzione) * 100
Esempio: Una soluzione è preparata mescolando 50 mL di etanolo con acqua fino a ottenere un volume finale di 200 mL. Qual è la percentuale in volume della soluzione?
% v/v = (50 mL / 200 mL) * 100 = 25%
Ricorda: Assicurati che le unità di misura siano coerenti (grammi con grammi, millilitri con millilitri) prima di eseguire il calcolo.
Parti per Milione (ppm): Quando le Concentrazioni Sono Molto Basse
Quando la concentrazione del soluto è estremamente bassa, si usa l'unità di misura delle parti per milione (ppm).
Definizione: ppm = (massa del soluto / massa della soluzione) * 1,000,000
Esempio: Un campione di acqua contiene 2 mg di piombo in 1 kg di acqua. Qual è la concentrazione di piombo in ppm?
Prima di tutto, dobbiamo rendere coerenti le unità di misura: 1 kg = 1,000,000 mg
ppm = (2 mg / 1,000,000 mg) * 1,000,000 = 2 ppm
Importante: Le ppm sono spesso usate per indicare la concentrazione di inquinanti in acqua o aria.
Strumenti Utili per il Calcolo della Concentrazione
Oltre alla carta e alla penna, esistono diversi strumenti che possono semplificare il calcolo della concentrazione:
- Calcolatrici scientifiche: Utili per eseguire calcoli complessi e per memorizzare formule.
- Fogli di calcolo (Excel, Google Sheets): Perfetti per organizzare i dati e per automatizzare i calcoli. Puoi creare tabelle e utilizzare formule predefinite per calcolare la concentrazione in diverse unità di misura.
- Calcolatori online: Esistono numerosi calcolatori online che ti permettono di calcolare la concentrazione inserendo semplicemente i valori noti.
- App per smartphone: Alcune app per smartphone sono dedicate al calcolo della concentrazione e possono essere molto utili in laboratorio o durante lo studio.
Consiglio: Sperimenta con diversi strumenti per trovare quello che si adatta meglio alle tue esigenze.
Esercizi Pratici: Mettiti alla Prova!
Il modo migliore per imparare a calcolare la concentrazione è fare pratica. Ecco alcuni esercizi per metterti alla prova:
- Calcola la molarità di una soluzione preparata sciogliendo 15 grammi di cloruro di sodio (NaCl) in acqua fino a ottenere un volume finale di 250 mL.
- Calcola la molalità di una soluzione ottenuta sciogliendo 5 grammi di urea (CH4N2O) in 150 grammi di acqua.
- Una soluzione contiene 30 grammi di zucchero in 200 grammi di soluzione. Qual è la percentuale in massa della soluzione?
- Una soluzione contiene 75 mL di acido acetico in 500 mL di soluzione. Qual è la percentuale in volume della soluzione?
- Un campione di acqua contiene 0.5 mg di mercurio in 500 g di acqua. Qual è la concentrazione di mercurio in ppm?
Ricorda: Controlla sempre i tuoi risultati e, se hai dubbi, chiedi aiuto al tuo insegnante o a un compagno di studi.
Conclusioni: La Concentrazione Non Fa Più Paura!
Spero che questa guida ti abbia aiutato a capire meglio come calcolare la concentrazione di una soluzione. Ricorda che la pratica è fondamentale per acquisire sicurezza e padronanza. Non aver paura di sperimentare e di fare errori: sono un'opportunità per imparare e migliorare. Come diceva Albert Einstein, "Non ho fallito. Ho semplicemente trovato 10.000 modi che non funzionano." Quindi, continua a provare e vedrai che presto calcolare la concentrazione diventerà un gioco da ragazzi! Buon lavoro!





+Pb2%2B(aq)+%2B+SO42-(aq).jpg)