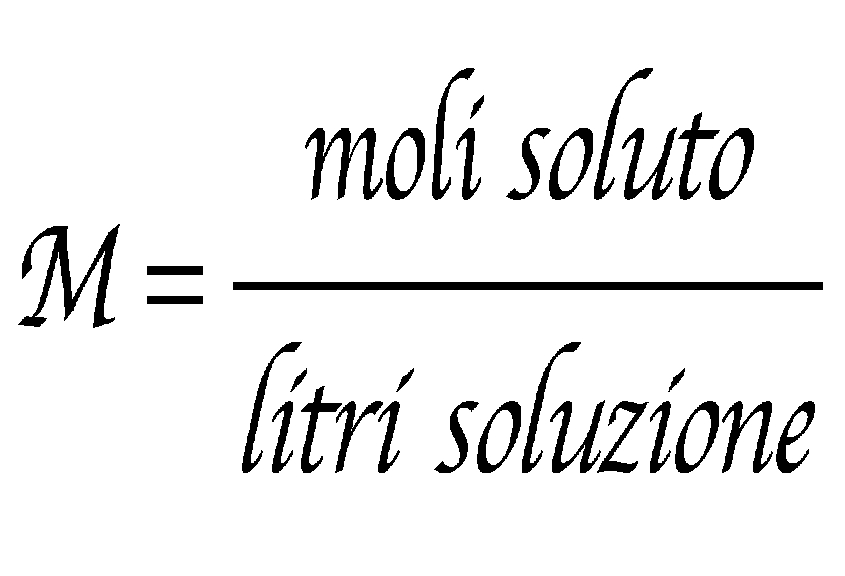Come Si Calcola Il Numero Di Moli

Il concetto di mole è fondamentale in chimica. Rappresenta una quantità specifica di una sostanza, precisamente la quantità che contiene tante entità elementari (atomi, molecole, ioni, ecc.) quanti sono gli atomi contenuti in 12 grammi di carbonio-12. È un ponte essenziale tra il mondo microscopico degli atomi e delle molecole e il mondo macroscopico che possiamo misurare in laboratorio.
Che Cos'è il Numero di Moli?
Il numero di moli indica quante volte quella quantità standard (la mole) è contenuta in un dato campione di una sostanza. Calcolarlo è un'abilità cruciale per risolvere problemi di stechiometria, preparare soluzioni con concentrazioni precise e comprendere le reazioni chimiche.
Perché è Importante Calcolare il Numero di Moli?
La capacità di calcolare il numero di moli è essenziale per gli studenti di chimica per diverse ragioni:
Must Read
- Stechiometria: Permette di determinare le quantità di reagenti necessarie e di prodotti ottenuti in una reazione chimica. Senza la conoscenza delle moli, non si può prevedere quanto prodotto si formerà.
- Concentrazioni: È fondamentale per preparare soluzioni con concentrazioni note, come molarità (moli di soluto per litro di soluzione).
- Leggi dei Gas: Permette di applicare le leggi dei gas, che mettono in relazione pressione, volume, temperatura e numero di moli di un gas.
- Comprensione Concettuale: Rafforza la comprensione della natura quantitativa della chimica.
Come afferma il chimico Linus Pauling: "La comprensione della mole è la chiave per aprire il mondo della chimica".
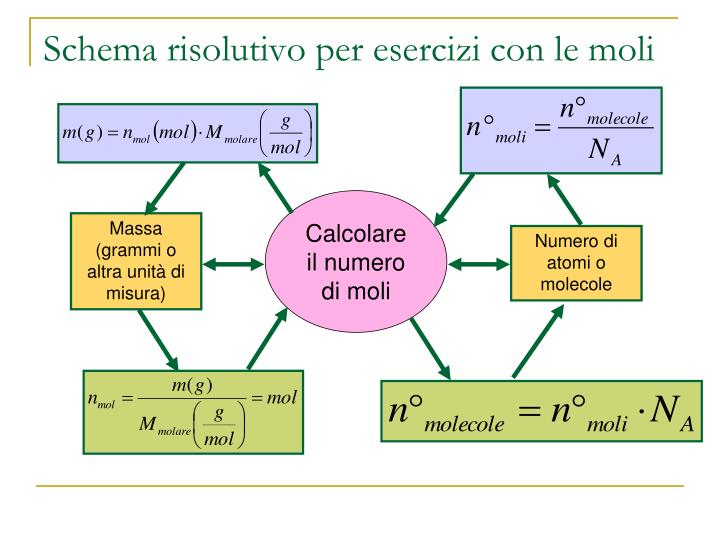
Come Calcolare il Numero di Moli: Formule e Metodi
Esistono diverse formule per calcolare il numero di moli, a seconda delle informazioni disponibili:

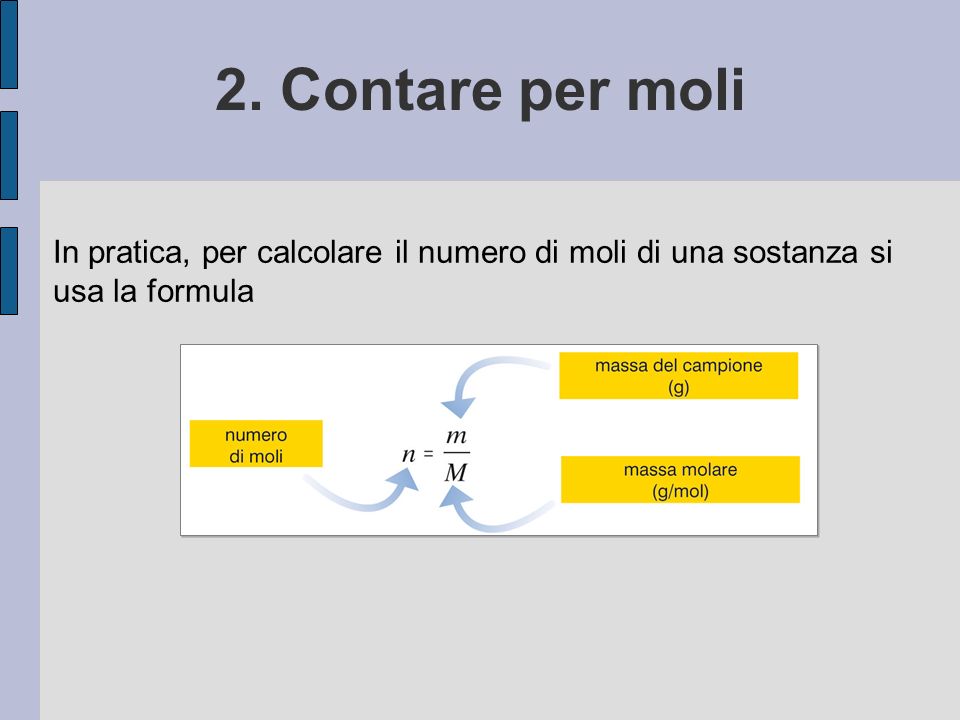
1. A Partire dalla Massa:
La formula più comune è:
numero di moli (n) = massa (m) / massa molare (M)
Dove:

- n è il numero di moli (solitamente espresso in mol)
- m è la massa del campione (solitamente espressa in grammi, g)
- M è la massa molare della sostanza (solitamente espressa in grammi per mole, g/mol). La massa molare si ricava dalla tavola periodica sommando le masse atomiche degli elementi che compongono la molecola.
Esempio: Calcolare il numero di moli in 10 grammi di acqua (H2O). La massa molare dell'acqua è circa 18 g/mol (2*1 + 16). Quindi, n = 10 g / 18 g/mol = 0.56 mol.
2. A Partire dal Volume di un Gas (a condizioni standard):
A condizioni standard (0°C e 1 atm), un mole di qualsiasi gas occupa un volume di 22.4 litri. Quindi:
numero di moli (n) = volume (V) / volume molare (Vm)
Dove:

- n è il numero di moli
- V è il volume del gas (in litri, L)
- Vm è il volume molare (22.4 L/mol a condizioni standard).
Esempio: Calcolare il numero di moli in 11.2 litri di ossigeno (O2) a condizioni standard. Quindi, n = 11.2 L / 22.4 L/mol = 0.5 mol.
3. A Partire dal Numero di Particelle:
Una mole contiene sempre 6.022 x 1023 particelle (numero di Avogadro, NA). Quindi:
numero di moli (n) = numero di particelle (N) / numero di Avogadro (NA)
Dove:
- n è il numero di moli
- N è il numero di particelle
- NA è il numero di Avogadro (6.022 x 1023 particelle/mol).
Esempio: Calcolare il numero di moli in 1.204 x 1024 atomi di carbonio. Quindi, n = (1.204 x 1024 atomi) / (6.022 x 1023 atomi/mol) = 2 mol.
Applicazioni Pratiche nella Vita Scolastica e Quotidiana
Calcolare il numero di moli non è solo un esercizio teorico. Ha applicazioni pratiche in laboratorio, ad esempio per preparare soluzioni a concentrazione specifica per esperimenti. Anche in cucina, se si vuole modificare una ricetta, la conoscenza delle moli può aiutare a mantenere le proporzioni corrette degli ingredienti, anche se non si fanno esplicitamente calcoli con le moli, il concetto di proporzioni è strettamente legato.