Come Si Calcola La Massa In Chimica

Ciao studenti! La chimica può sembrare un universo complicato, pieno di formule e concetti astratti. Ma non lasciatevi spaventare! In realtà, è un mondo affascinante che ci aiuta a capire la materia che ci circonda. Oggi ci concentreremo su un concetto fondamentale: come si calcola la massa in chimica. Sembra difficile? Assolutamente no!
Prima di tutto, cerchiamo di capire cosa intendiamo per "massa". Nella vita di tutti i giorni, usiamo spesso "peso" e "massa" come sinonimi, ma in chimica (e in fisica) sono concetti ben distinti. La massa è la quantità di materia presente in un oggetto, mentre il peso è la forza con cui la gravità attrae quell'oggetto. Per fortuna, sulla Terra, la massa e il peso sono proporzionali, quindi possiamo usare una bilancia per misurare la massa (e indirettamente il peso).
Ora, come calcoliamo la massa in chimica? Ci sono diverse situazioni in cui potremmo doverlo fare, e ognuna richiede un approccio leggermente diverso.
Must Read
Calcolare la Massa di un Singolo Atomo o Molecola
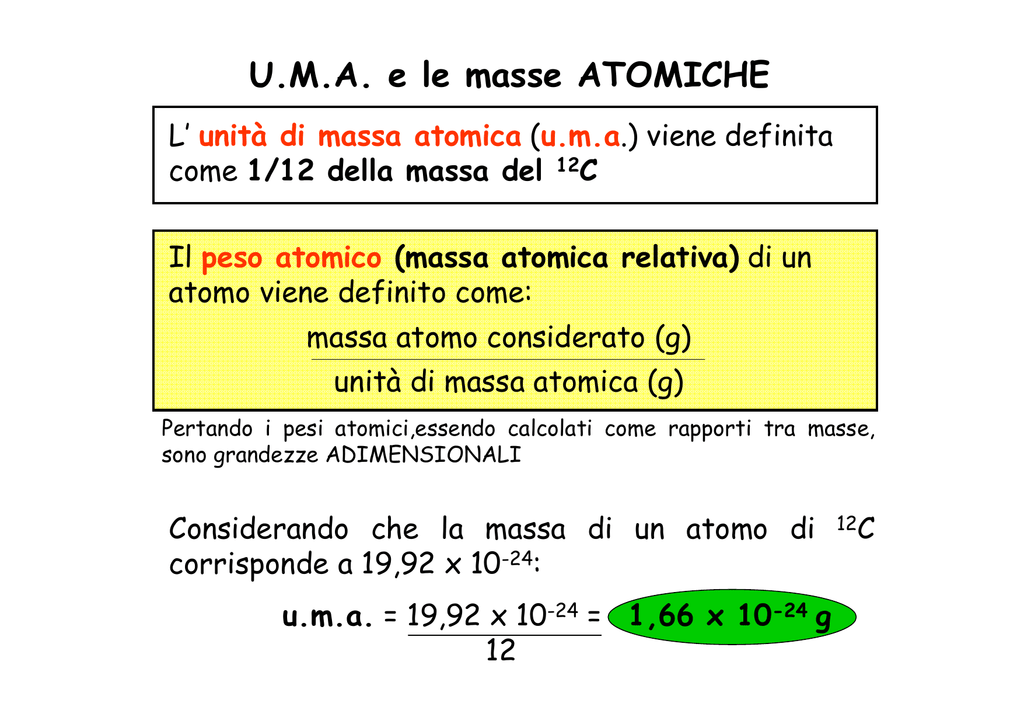
Qui entra in gioco la tavola periodica degli elementi! Ogni elemento ha un numero atomico (il numero di protoni nel nucleo) e una massa atomica, indicata solitamente in unità di massa atomica (u.m.a.). La massa atomica è la massa media di un atomo di quell'elemento, tenendo conto dei suoi isotopi (atomi dello stesso elemento con un diverso numero di neutroni).
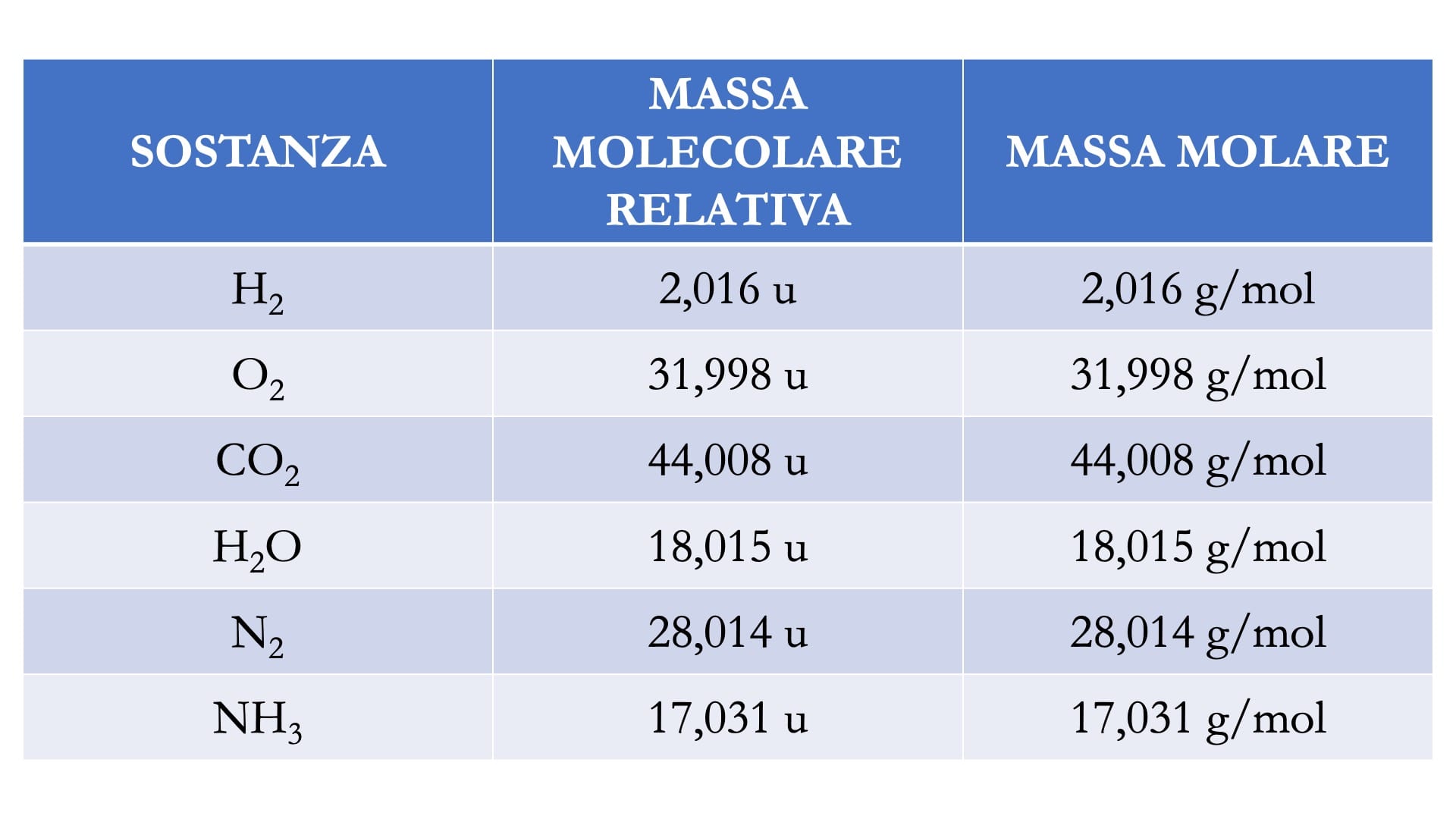
Per calcolare la massa di una molecola, sommiamo le masse atomiche di tutti gli atomi che la compongono. Ad esempio, prendiamo l'acqua (H2O). La massa atomica dell'idrogeno (H) è circa 1 u.m.a., e quella dell'ossigeno (O) è circa 16 u.m.a. Quindi, la massa molecolare dell'acqua è (2 * 1) + 16 = 18 u.m.a.

Dalla u.m.a. ai Grammi: il Concetto di Mole
L'unità di massa atomica è utile per confrontare le masse degli atomi e delle molecole, ma è troppo piccola per essere usata nelle misurazioni di laboratorio. Ecco perché introduciamo il concetto di mole. Una mole è definita come il numero di atomi presenti in 12 grammi di carbonio-12. Questo numero, noto come numero di Avogadro (circa 6.022 x 1023), ci permette di collegare la massa atomica in u.m.a. alla massa molare in grammi/mole.
La massa molare di una sostanza è la massa di una mole di quella sostanza. Ad esempio, la massa molare dell'acqua è 18 g/mol. Questo significa che una mole di molecole d'acqua pesa 18 grammi.

Calcolare la Massa di una Sostanza in una Reazione Chimica
Le reazioni chimiche seguono delle leggi precise, e una delle più importanti è la legge di conservazione della massa: la massa totale dei reagenti è uguale alla massa totale dei prodotti. Per calcolare la massa di una sostanza coinvolta in una reazione, usiamo la stechiometria, che si basa sui coefficienti nella reazione bilanciata.
Per esempio, consideriamo la reazione di sintesi dell'ammoniaca (NH3): N2 + 3H2 → 2NH3. I coefficienti indicano che 1 mole di azoto reagisce con 3 moli di idrogeno per produrre 2 moli di ammoniaca. Conoscendo le masse molari di N2, H2 e NH3, possiamo calcolare le masse relative che reagiscono e si formano.
"La chimica è un'avventura, non un ostacolo." - Marie Curie
Ricordate, la chimica non è solo una serie di calcoli. È un modo di vedere il mondo che ci circonda con occhi nuovi. Capire come calcolare la massa in chimica è un passo importante per svelare i segreti della materia e apprezzare la bellezza e la complessità della natura. Non abbiate paura di chiedere aiuto, di fare errori e di imparare da essi. Ogni piccolo passo vi porterà più vicino alla comprensione di questo affascinante mondo. Buon studio!