Come Si Definisce Il Numero Atomico Z

Quante volte ti sei trovato a fissare la tavola periodica, sentendoti sopraffatto da simboli e numeri apparentemente senza senso? Non sei solo. Molti studenti di chimica, e anche appassionati di scienza, si scontrano con lo stesso ostacolo: comprendere appieno il significato e l'importanza del numero atomico Z. In questo articolo, supereremo insieme questa sfida, svelandone il segreto in modo chiaro e accessibile.
Cos'è il Numero Atomico Z? Una Definizione Chiara
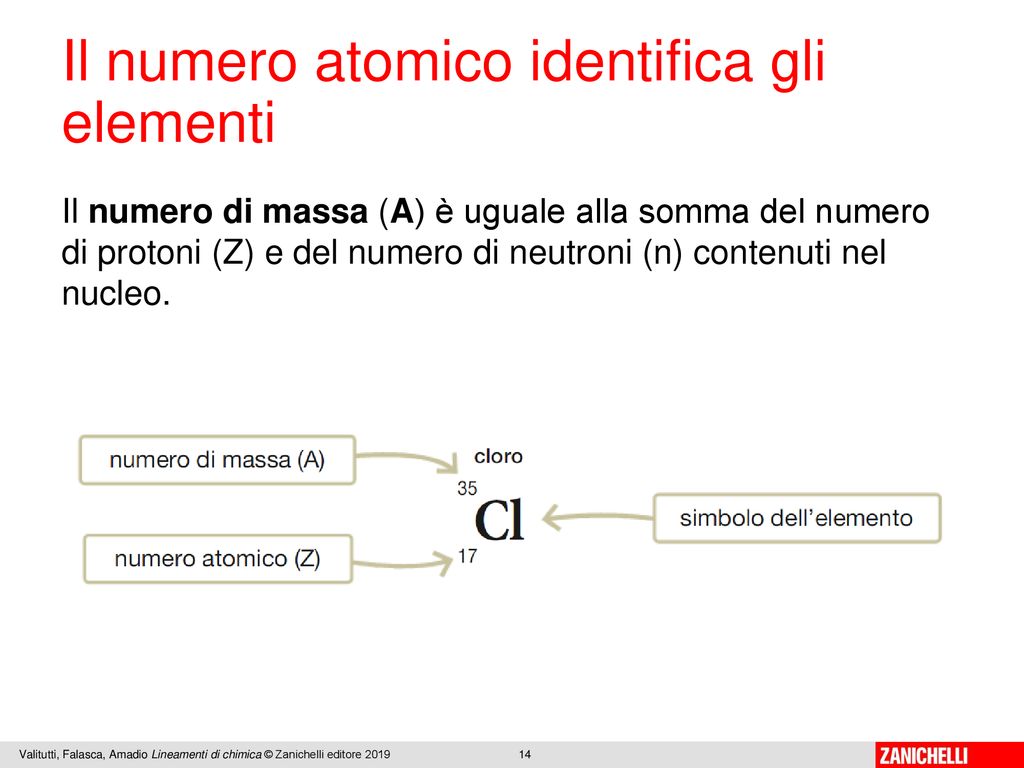
Il numero atomico (Z) è una delle pietre angolari della chimica. Rappresenta il numero di protoni presenti nel nucleo di un atomo. Questo numero è unico per ogni elemento e lo identifica in modo univoco. Pensa al numero atomico come al codice fiscale di un elemento: è ciò che lo distingue inequivocabilmente dagli altri.
"The atomic number (Z) is the number of protons found in the nucleus of an atom and therefore identical to the charge number of the nucleus." - IUPAC Compendium of Chemical Terminology
Must Read
Perché il Numero di Protoni è Così Importante?
Il numero di protoni determina l'identità chimica di un elemento. Cambiare il numero di protoni significa trasformare un elemento in un altro (un processo che avviene nelle reazioni nucleari, non in quelle chimiche ordinarie!). Ad esempio:
- L'idrogeno (H), con un solo protone, ha Z = 1.
- L'elio (He), con due protoni, ha Z = 2.
- Il carbonio (C), con sei protoni, ha Z = 6.
Immagina di aggiungere un protone al nucleo di un atomo di idrogeno. Istantaneamente, non avrai più idrogeno, ma elio! Questo dimostra quanto sia cruciale il numero di protoni per definire la natura di un elemento.
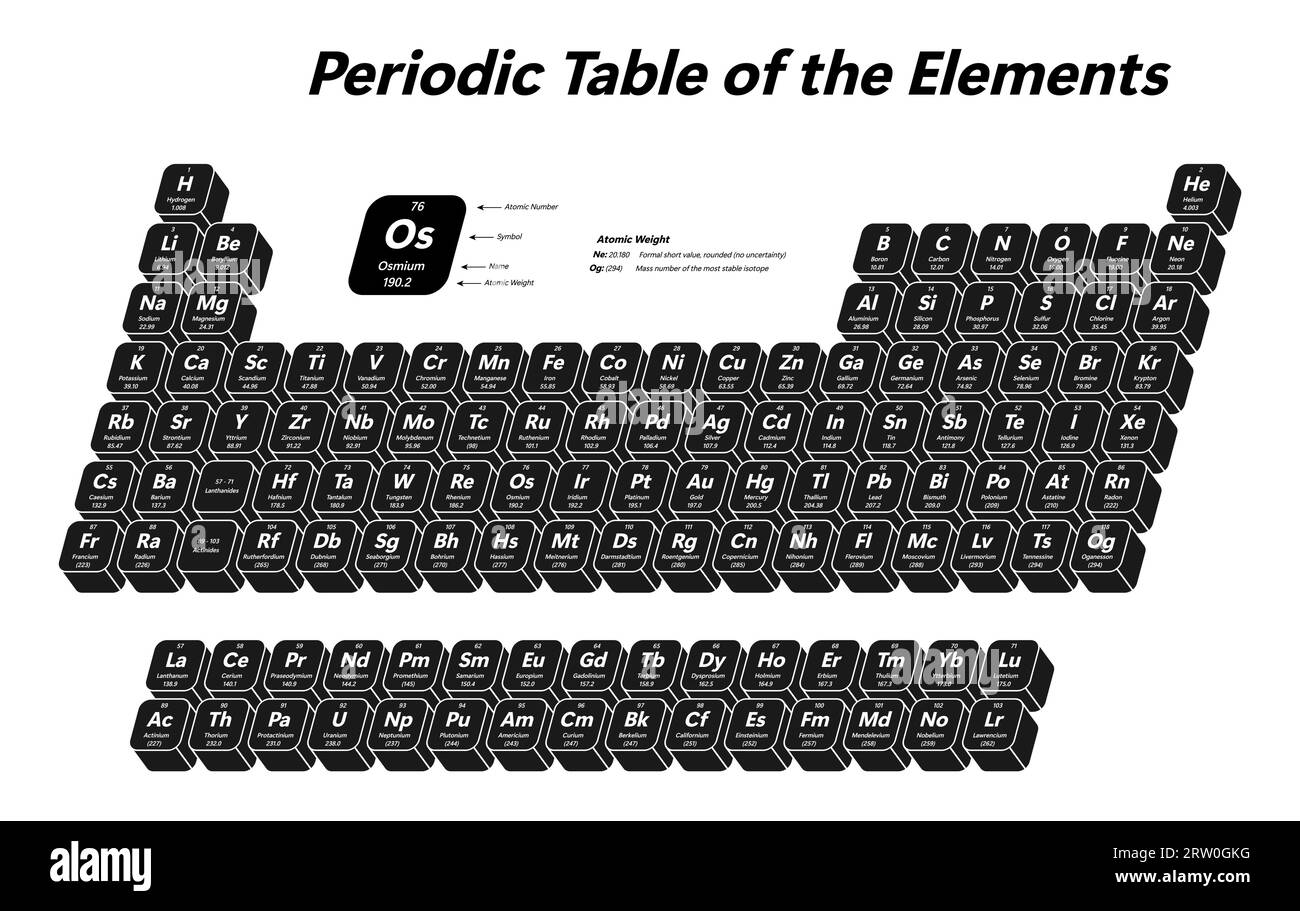
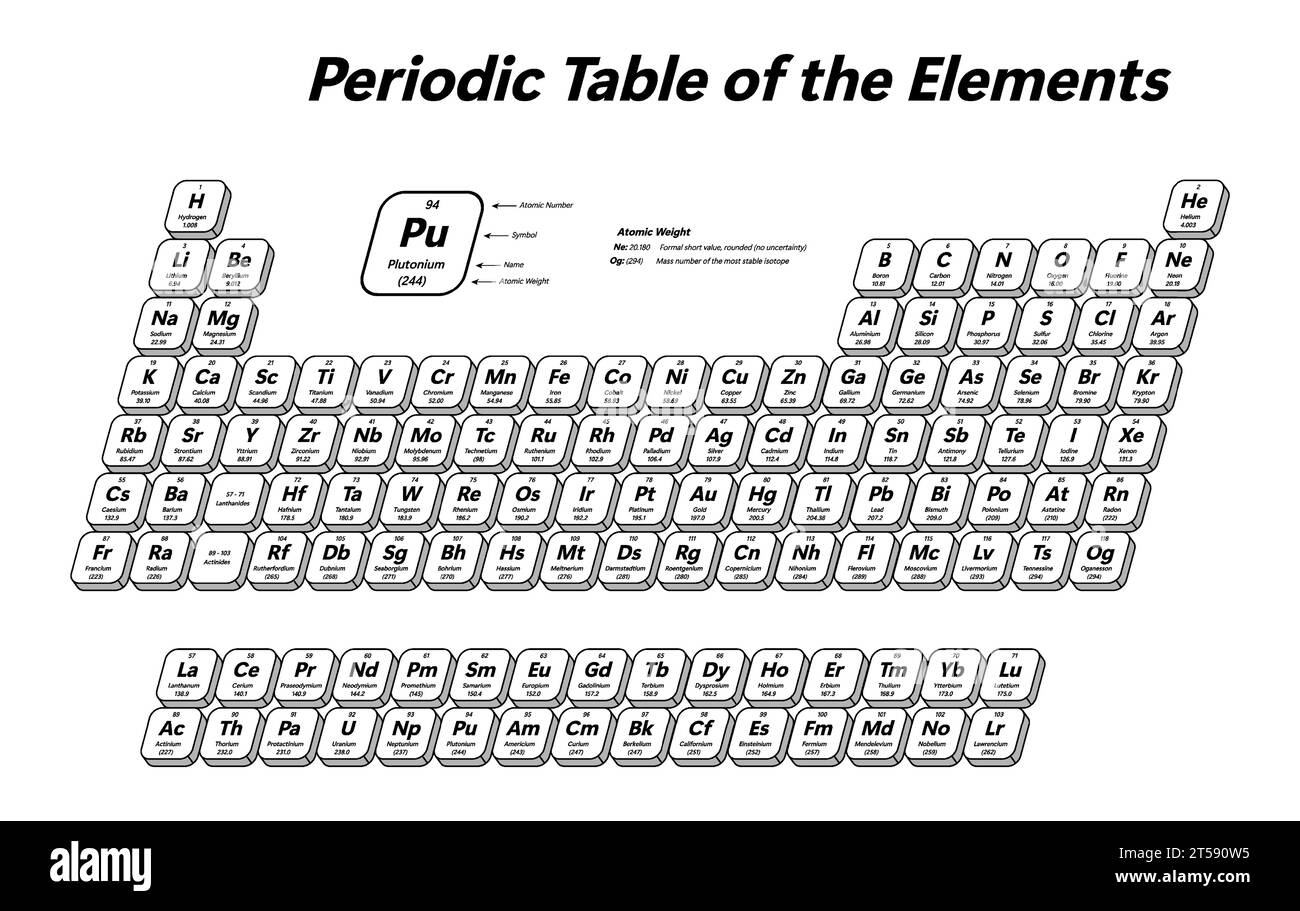
Il Numero Atomico Z e la Tavola Periodica
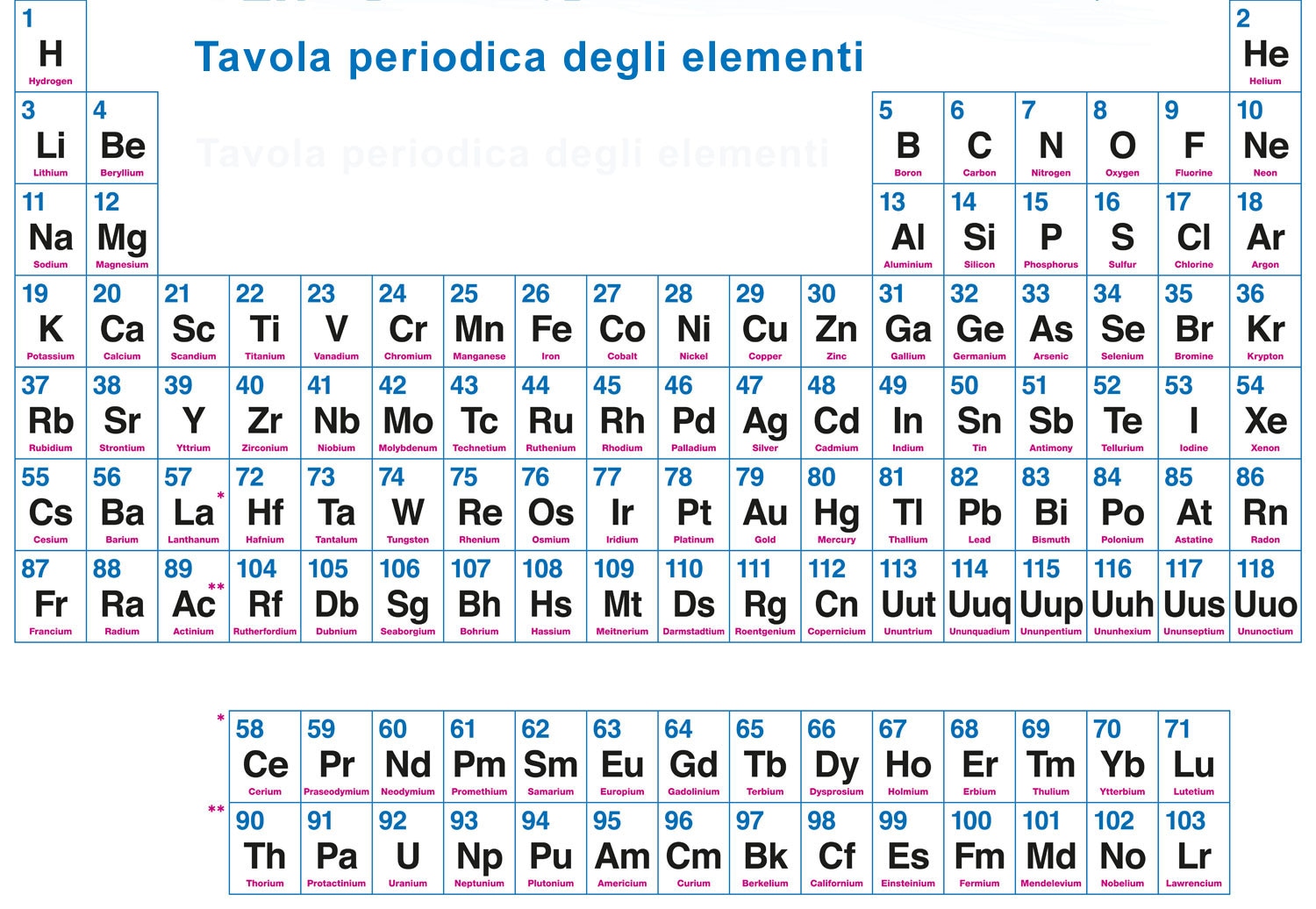
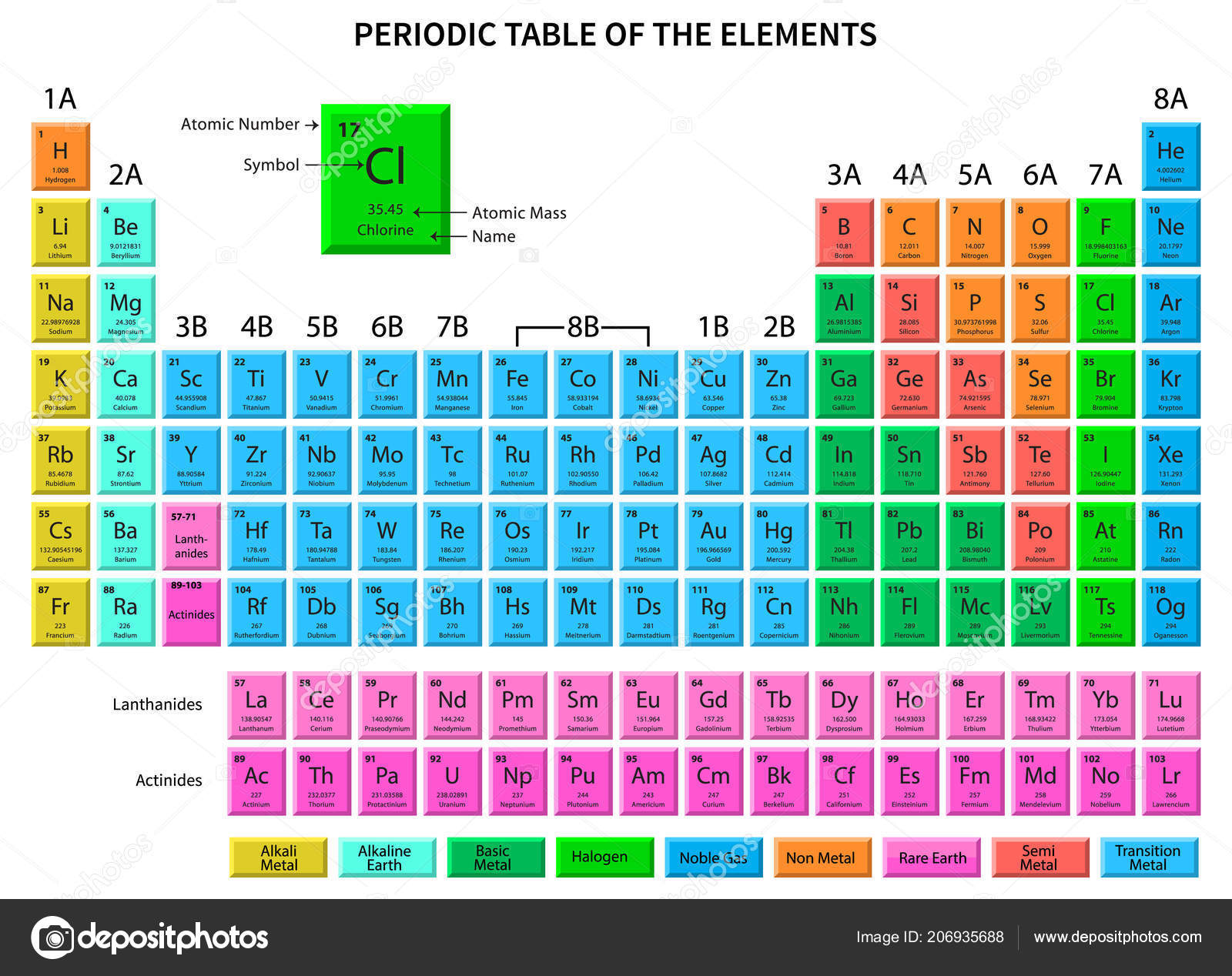
La tavola periodica è organizzata proprio in base al numero atomico crescente. Questo significa che gli elementi sono disposti in ordine di Z, partendo da sinistra verso destra e dall'alto verso il basso. Questa organizzazione non è casuale: riflette le proprietà chimiche degli elementi, che derivano dalla loro configurazione elettronica (a sua volta determinata dal numero di protoni).
"The periodic table is arguably the most important concept in chemistry. It is a roadmap to understanding the behavior of matter." - Theodore Gray, autore di "The Elements"
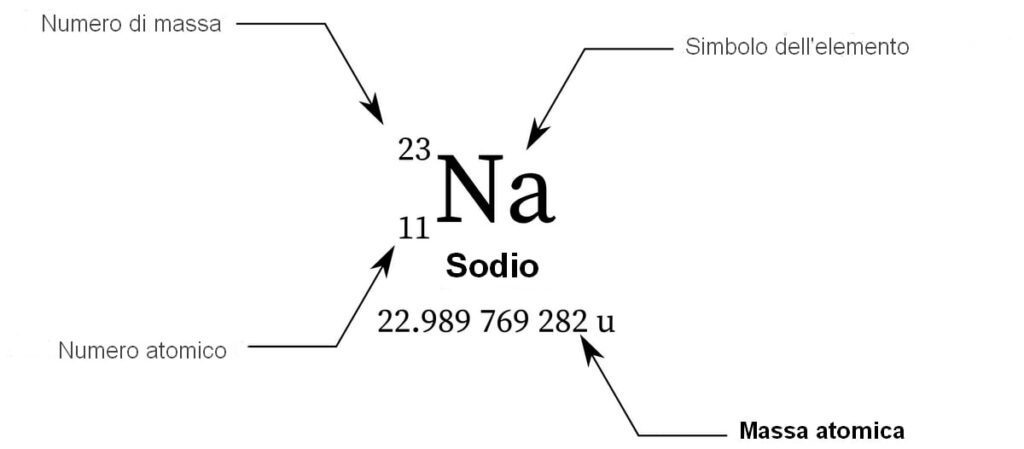
Osserva la tavola periodica: noterai che ogni elemento ha un numero intero ben definito. Questo è il suo numero atomico Z. Ad esempio, il sodio (Na) ha Z = 11 e si trova dopo il neon (Ne), che ha Z = 10.
Come Trovare il Numero Atomico di un Elemento
Trovare il numero atomico di un elemento è semplicissimo: basta consultare la tavola periodica! Di solito, il numero atomico è indicato sopra il simbolo chimico dell'elemento.
Ad esempio, prendiamo l'oro (Au):

- Cerca il simbolo "Au" sulla tavola periodica.
- Sopra il simbolo, troverai il numero 79. Questo è il numero atomico dell'oro (Z = 79).
Il Numero Atomico Z e la Configurazione Elettronica
Il numero atomico non solo definisce l'elemento, ma influenza anche la sua configurazione elettronica. In un atomo neutro (cioè con carica elettrica complessiva zero), il numero di elettroni è uguale al numero di protoni (Z). Gli elettroni si dispongono attorno al nucleo in orbitali specifici, seguendo regole ben precise (principio di Aufbau, regola di Hund, ecc.).
La configurazione elettronica determina le proprietà chimiche di un elemento, cioè il modo in cui reagisce con altri elementi. Ad esempio, gli elementi del gruppo 1 (metalli alcalini) hanno un solo elettrone nel loro guscio esterno (elettroni di valenza), il che li rende altamente reattivi.
"The electronic configuration of an atom is the arrangement of electrons in its electron shells or subshells." - Chemistry LibreTexts

Un Esempio: L'Ossigeno (O)
L'ossigeno (O) ha Z = 8. Questo significa che ha 8 protoni nel nucleo e, in un atomo neutro, 8 elettroni. La sua configurazione elettronica è 1s² 2s² 2p⁴. I suoi 6 elettroni di valenza (2s² 2p⁴) gli conferiscono una forte tendenza ad acquisire altri due elettroni per raggiungere una configurazione stabile, come quella del neon (Ne).
Il Numero Atomico Z e gli Isotopi
Gli isotopi sono atomi dello stesso elemento (stesso numero atomico Z) ma con un diverso numero di neutroni nel nucleo. Poiché il numero di protoni è lo stesso, si tratta sempre dello stesso elemento, ma con una massa atomica differente.
Ad esempio, il carbonio (C) ha due isotopi stabili principali:
- Carbonio-12 (¹²C): 6 protoni e 6 neutroni.
- Carbonio-13 (¹³C): 6 protoni e 7 neutroni.
Entrambi sono carbonio, perché hanno 6 protoni (Z = 6), ma hanno masse diverse a causa del diverso numero di neutroni.

Il carbonio-14 (¹⁴C), un isotopo radioattivo, ha 6 protoni e 8 neutroni. È utilizzato nella datazione al radiocarbonio per determinare l'età di materiali organici antichi.
Strumenti e Metodi Pratici per Comprendere il Numero Atomico Z
Ecco alcuni suggerimenti e strumenti per consolidare la tua comprensione del numero atomico:
- Usa la tavola periodica interattiva: Esistono molte tavole periodiche online che forniscono informazioni dettagliate su ogni elemento, incluso il numero atomico, la configurazione elettronica e gli isotopi.
- Crea schede mnemoniche: Scrivi il simbolo chimico, il nome e il numero atomico di ciascun elemento su una scheda. Rivedile regolarmente per memorizzarle.
- Risolvi esercizi: Cerca esercizi online o nel tuo libro di testo che richiedono di identificare un elemento in base al suo numero atomico o di determinare il numero di protoni, elettroni e neutroni in un atomo o ione.
- Visualizza modelli atomici: Utilizza software di modellazione molecolare o disegna diagrammi per visualizzare la struttura degli atomi e la disposizione degli elettroni attorno al nucleo.
Esercizi Pratici:
- Qual è il numero atomico del potassio (K)?
- Quanti protoni ha un atomo di azoto (N)?
- Quale elemento ha un numero atomico di 26?
- Un atomo con 17 protoni è quale elemento?
Conclusione: Il Numero Atomico, Chiave per la Chimica
Il numero atomico Z è molto più di un semplice numero sulla tavola periodica. È la chiave per comprendere l'identità, la configurazione elettronica, le proprietà chimiche e il comportamento degli elementi. Comprendere il numero atomico è fondamentale per padroneggiare i concetti fondamentali della chimica.
Non scoraggiarti se all'inizio ti sembra complicato. Con la pratica e l'utilizzo degli strumenti giusti, diventerai un esperto nel decifrare il linguaggio della chimica. Ricorda: "The important thing is not to stop questioning." - Albert Einstein. Continua a esplorare e a porre domande, e scoprirai la bellezza e l'eleganza della scienza che ci circonda.

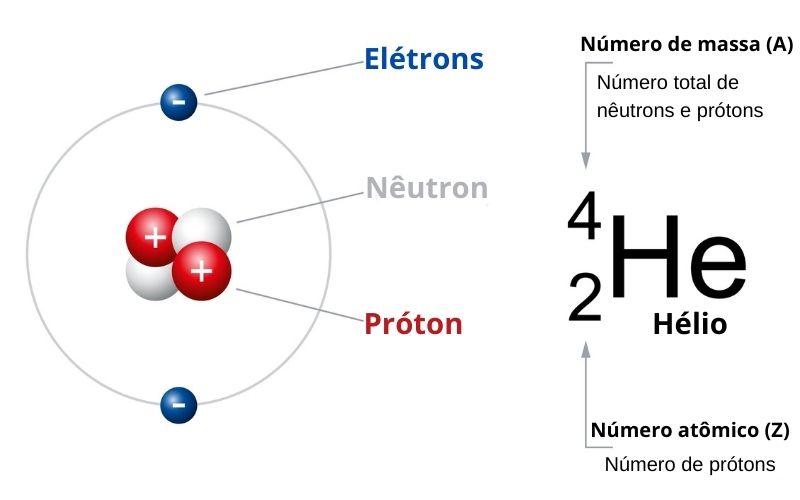


+che+si+differenziano+per+il+diverso+numero+di+protoni(%3Delettroni)+da+1+a+92+il+numero+di+protoni(o+elettroni)+è+tipico+per+ogni+diverso+elemento+e+si+definisce+numero+atomico+Z+ogni+atomo+possiede+un+nucleo(protoni%2Bneutroni)+e+un+perinucleo+con+elettroni+disposti+secondo+particolari+configurazioni+energetiche+5-elementi+identici(stesso+Z)+possono+differire+per+il+numero+di+neutroni+presenti+nel+nucleo(isotopi):il+numero+di+protoni+e+di+neutroni+si+definisce+numero+di+massa+A.jpg)



+Símbolo+Nombre.jpg)