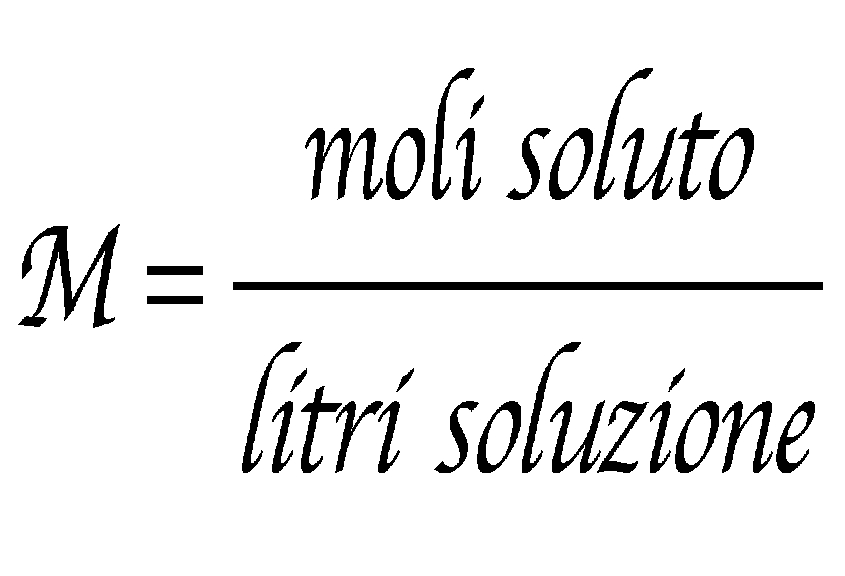Come Si Trova Il Numero Di Moli

Quante volte ti sei trovato di fronte a un problema di chimica, fissando numeri e simboli senza avere la minima idea di come iniziare? La chimica può sembrare un labirinto intricato, soprattutto quando si tratta di concetti come le moli. Ma non disperare! Comprendere come trovare il numero di moli è una competenza fondamentale, la chiave per sbloccare molti misteri della chimica. Non si tratta solo di superare un esame; questa conoscenza è essenziale per capire il mondo che ci circonda, dalla preparazione di una torta alla comprensione dei processi industriali.
Immagina di voler preparare una torta. La ricetta ti dice di usare una certa quantità di farina, zucchero e uova. Se non misuri correttamente gli ingredienti, il risultato finale potrebbe non essere quello desiderato. Allo stesso modo, in chimica, le moli fungono da "unità di misura" per le sostanze chimiche. Conoscere il numero di moli ti permette di combinare le sostanze chimiche nelle giuste proporzioni, ottenendo la reazione desiderata e evitando sprechi o, peggio, reazioni pericolose.
Perché le Moli Sono Importanti?
Le moli sono importanti perché ci forniscono un modo per collegare il mondo microscopico degli atomi e delle molecole al mondo macroscopico che possiamo vedere e misurare. Non possiamo contare direttamente gli atomi, sono troppo piccoli! Ma possiamo pesare una sostanza e, utilizzando la massa molare, calcolare il numero di moli presenti.
Must Read
Pensa a una fabbrica che produce farmaci. La precisa quantità di ogni ingrediente è cruciale per l'efficacia e la sicurezza del farmaco. Gli scienziati in laboratorio utilizzano le moli per garantire che le reazioni chimiche avvengano correttamente, producendo il farmaco con la composizione desiderata. Oppure, immagina un agricoltore che deve fertilizzare il suo terreno. La quantità di fertilizzante necessaria dipende dalla composizione del suolo e dalle esigenze delle piante. Conoscere le moli di nutrienti presenti nel fertilizzante permette all'agricoltore di applicare la giusta quantità, massimizzando la resa del raccolto e minimizzando l'impatto ambientale.
Come Calcolare il Numero di Moli: Diversi Approcci
Esistono diversi modi per calcolare il numero di moli, a seconda delle informazioni che hai a disposizione. Vediamo i metodi più comuni:
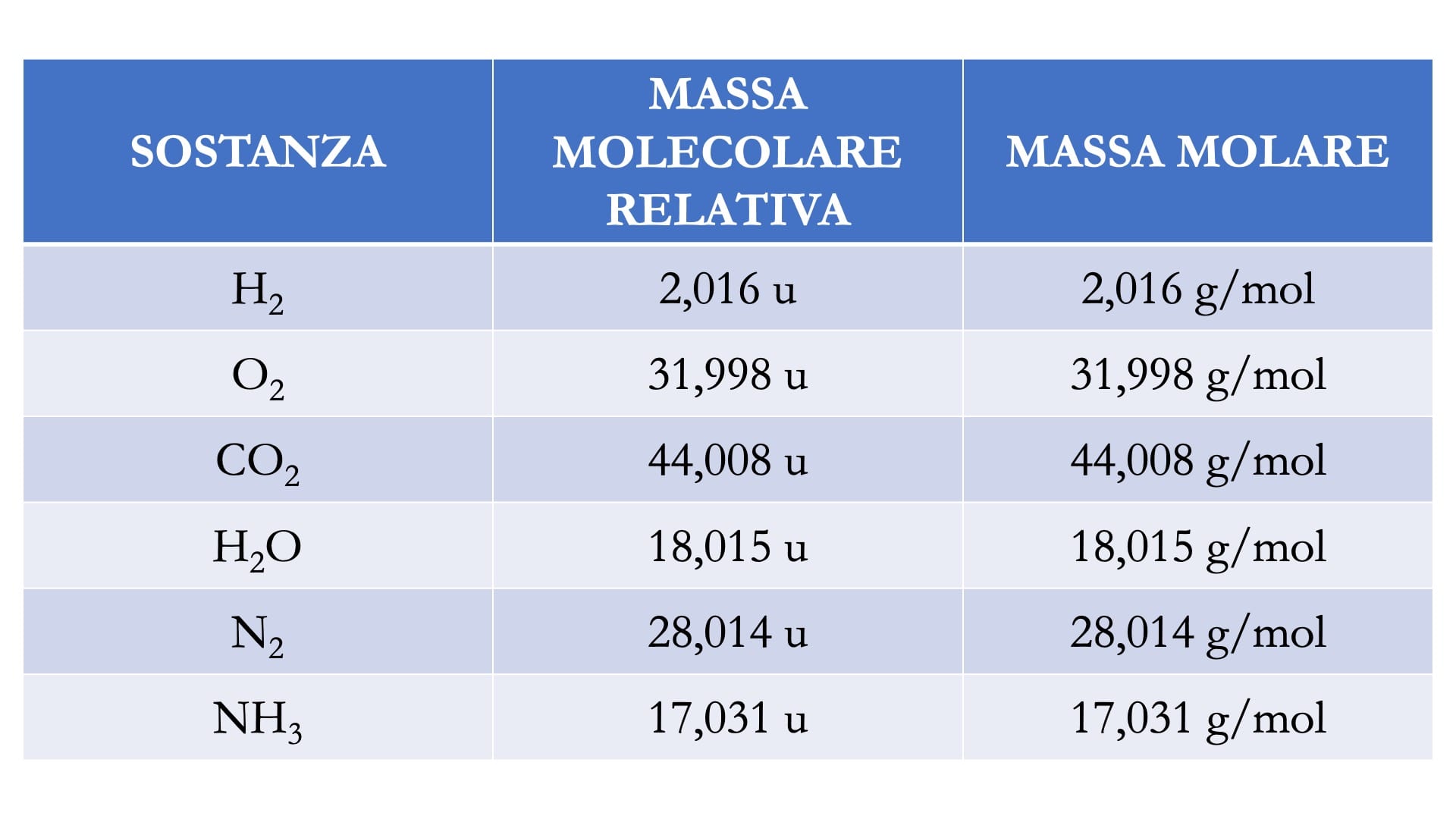
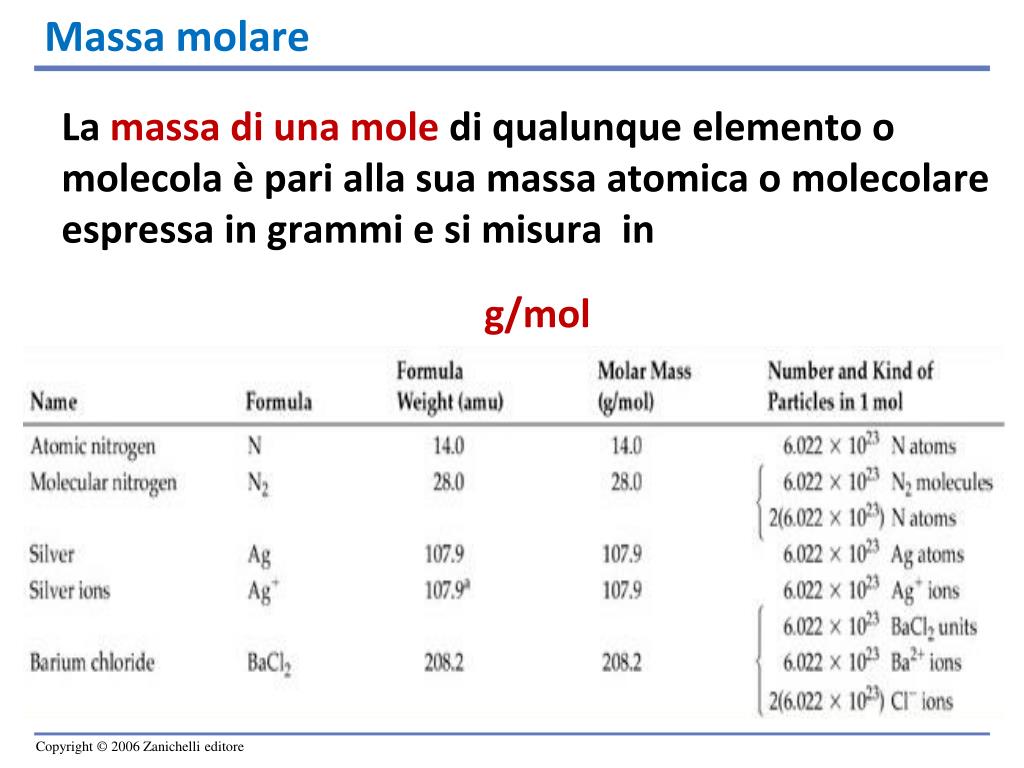
1. Utilizzando la Massa Molare
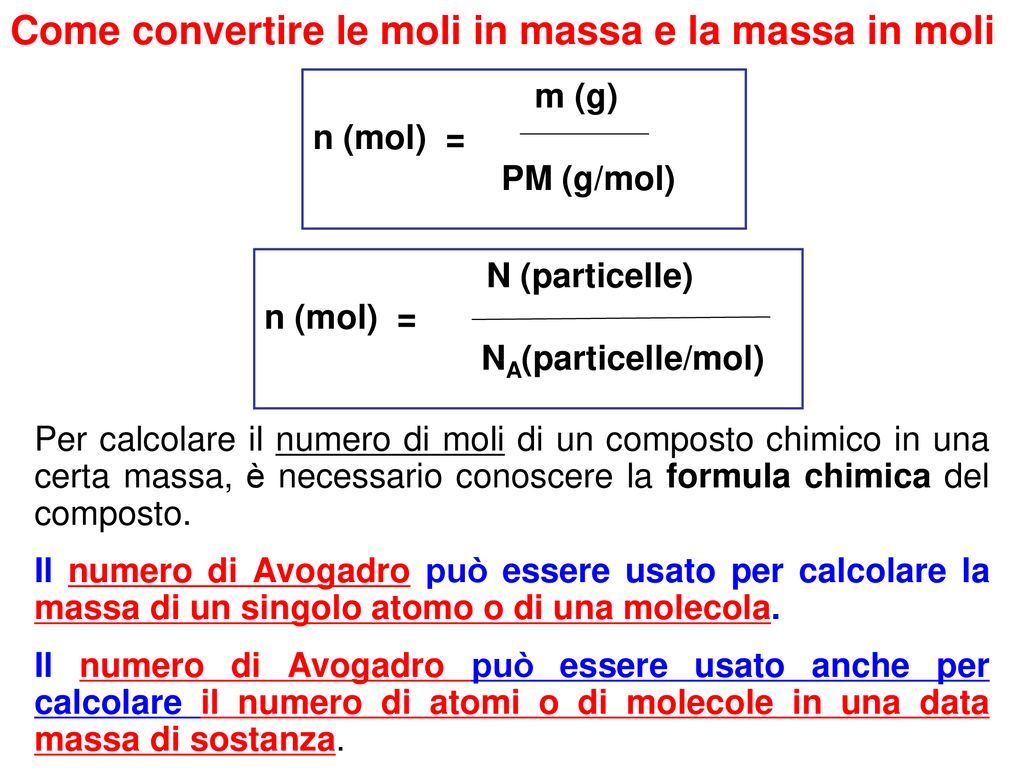
Questo è il metodo più frequentemente utilizzato. La massa molare è la massa di una mole di una sostanza, espressa in grammi per mole (g/mol). Puoi trovare la massa molare di un elemento sulla tavola periodica. Per una molecola, devi sommare le masse molari di tutti gli atomi che la compongono.
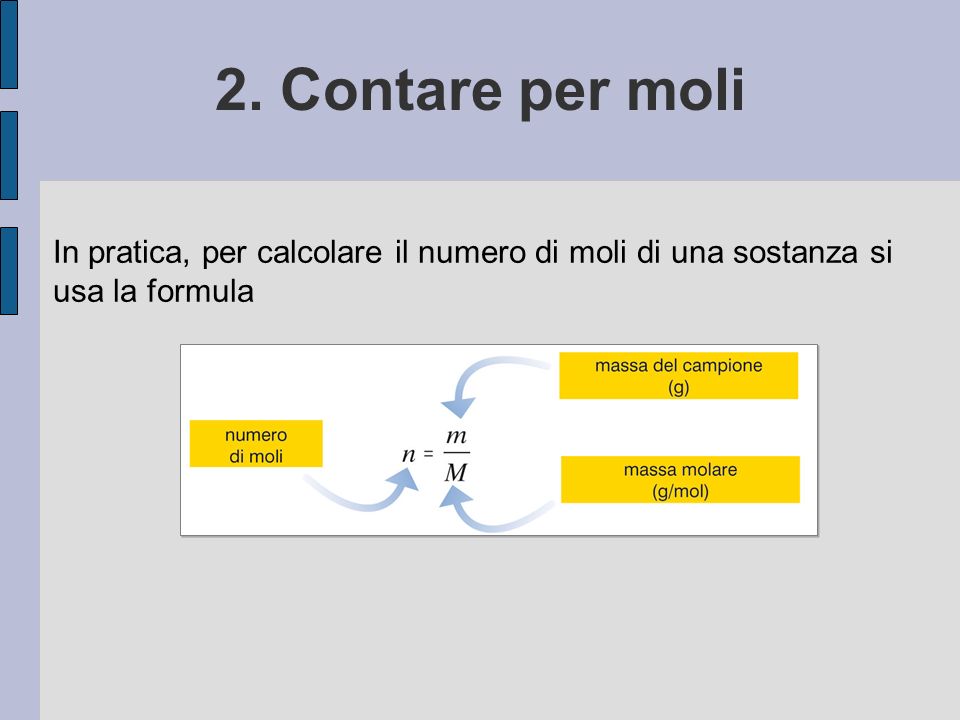
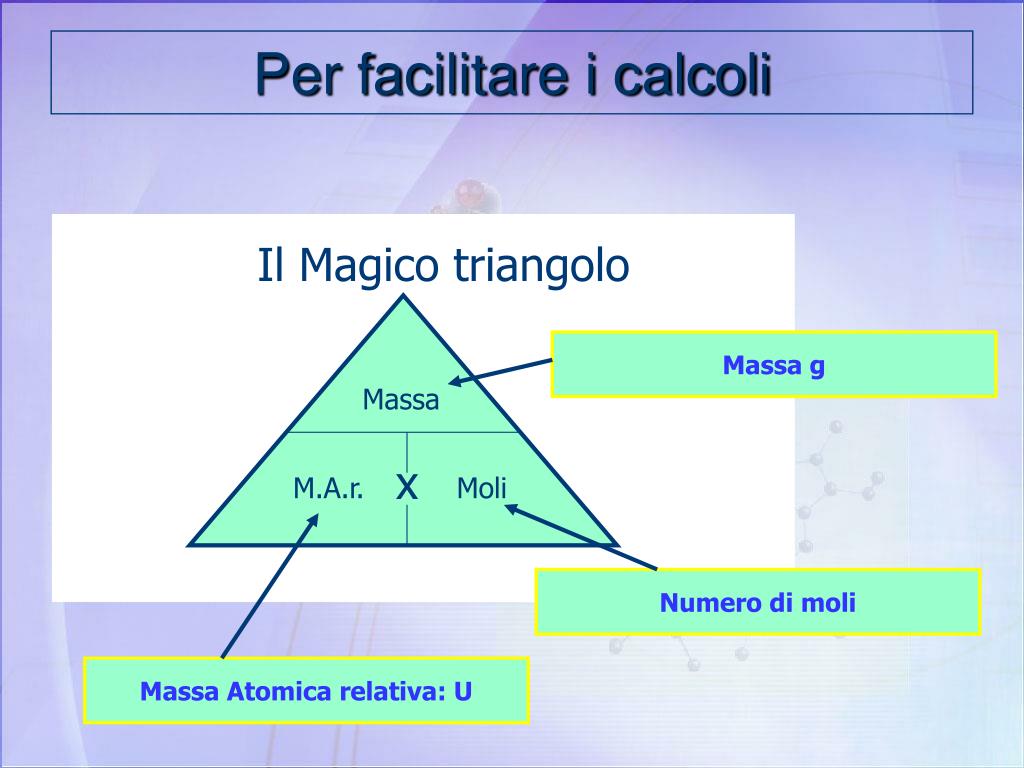
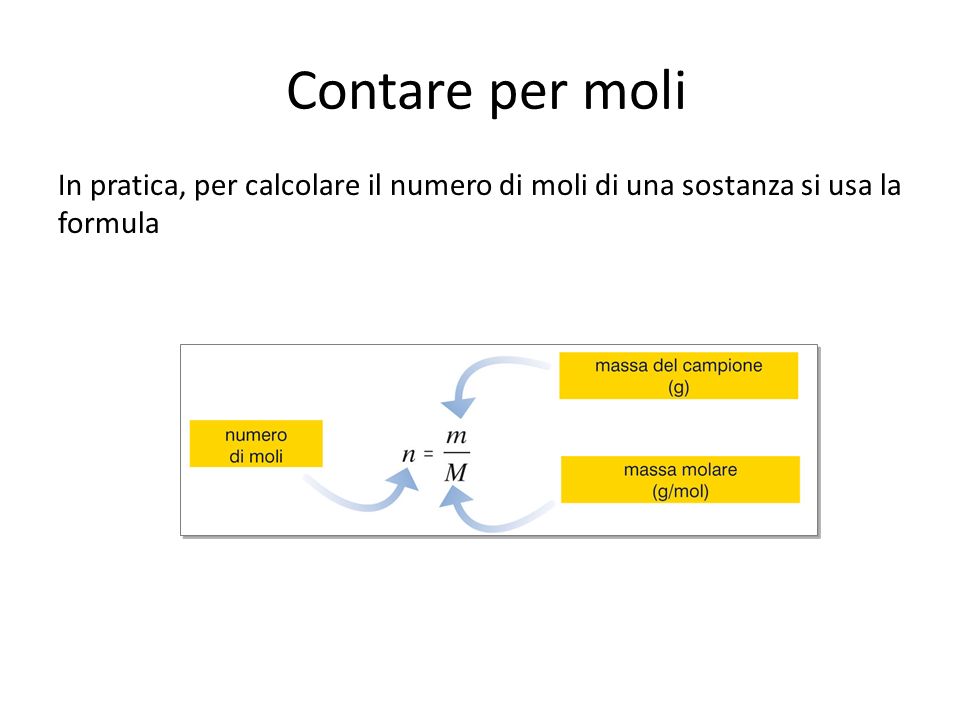
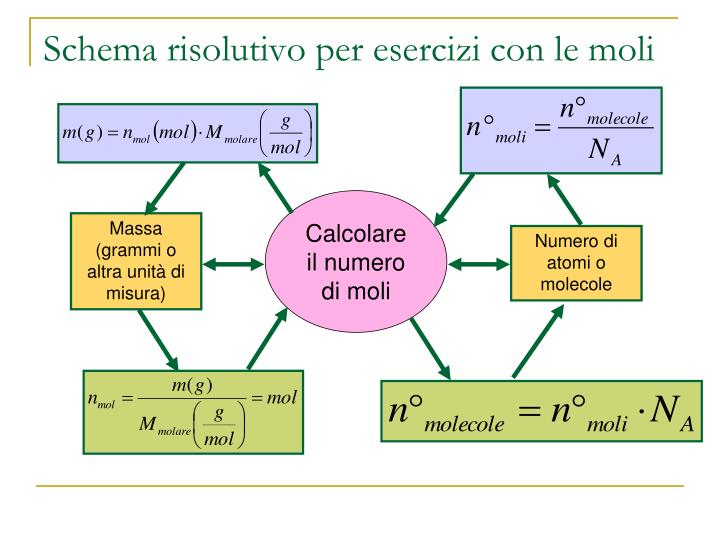
La formula per calcolare il numero di moli (n) utilizzando la massa molare (M) e la massa (m) del campione è:
n = m / M

Esempio: Quante moli ci sono in 50 grammi di acqua (H2O)?
- La massa molare dell'idrogeno (H) è circa 1 g/mol.
- La massa molare dell'ossigeno (O) è circa 16 g/mol.
- Quindi, la massa molare dell'acqua (H2O) è (2 * 1) + 16 = 18 g/mol.
- Usando la formula: n = 50 g / 18 g/mol = 2.78 moli.
2. Utilizzando il Volume di un Gas (a condizioni standard)
A condizioni standard di temperatura e pressione (STP), che sono 0°C (273.15 K) e 1 atmosfera (101.325 kPa), una mole di qualsiasi gas occupa un volume di 22.4 litri. Questo è noto come volume molare.
La formula per calcolare il numero di moli (n) utilizzando il volume (V) di un gas a STP è:
n = V / 22.4 L/mol
Esempio: Quante moli ci sono in 11.2 litri di ossigeno gassoso (O2) a STP?
- Usando la formula: n = 11.2 L / 22.4 L/mol = 0.5 moli.
Importante: Questa formula funziona solo a condizioni standard. Se la temperatura e la pressione sono diverse da STP, devi utilizzare l'equazione dei gas ideali (PV = nRT).

3. Utilizzando l'Equazione dei Gas Ideali
L'equazione dei gas ideali è un'equazione di stato che descrive il comportamento dei gas ideali. È una delle equazioni più importanti in chimica e fisica. L'equazione è:
PV = nRT
Dove:
- P = Pressione (in Pascal o atmosfere)
- V = Volume (in metri cubi o litri)
- n = Numero di moli
- R = Costante dei gas ideali (8.314 J/(molK) o 0.0821 Latm/(molK))
- T = Temperatura (in Kelvin)
Per calcolare il numero di moli (n), riarrangiamo l'equazione:
n = PV / RT
Esempio: Quante moli ci sono in un gas che occupa un volume di 10 litri a una pressione di 2 atmosfere e una temperatura di 300 K?
- Usando la formula: n = (2 atm * 10 L) / (0.0821 Latm/(mol*K) * 300 K) = 0.81 moli.
4. Utilizzando la Concentrazione Molare (Molarità)
La concentrazione molare, o molarità (M), è definita come il numero di moli di soluto per litro di soluzione.
La formula per calcolare il numero di moli (n) utilizzando la molarità (M) e il volume (V) della soluzione (in litri) è:
n = M * V
Esempio: Quante moli di NaCl ci sono in 500 ml di una soluzione 0.2 M?
- Converti il volume in litri: 500 ml = 0.5 L.
- Usando la formula: n = 0.2 mol/L * 0.5 L = 0.1 moli.
Controindicazioni e Potenziali Errori
È importante essere consapevoli dei potenziali errori che si possono commettere nel calcolo delle moli. Uno degli errori più comuni è confondere la massa molare con la massa atomica. Ricorda, la massa molare si riferisce a una mole di sostanza, mentre la massa atomica si riferisce a un singolo atomo.

Un altro errore comune è l'utilizzo di unità di misura errate. Assicurati di utilizzare le unità corrette per pressione, volume e temperatura quando utilizzi l'equazione dei gas ideali. Se usi l'equazione PV=nRT, assicurati di utilizzare le unità corrette per R (la costante dei gas ideali) in base alle unità di P, V e T.
Alcuni potrebbero obiettare che i calcoli stechiometrici sono troppo astratti e lontani dalla vita reale. Tuttavia, come abbiamo visto negli esempi precedenti, la comprensione delle moli è fondamentale in molti settori, dalla medicina all'agricoltura, e ci aiuta a comprendere e manipolare il mondo che ci circonda.
Risoluzione dei Problemi e Consigli Pratici
Ecco alcuni consigli pratici per risolvere i problemi di stechiometria:
- Leggi attentamente il problema: Assicurati di capire cosa ti viene chiesto di calcolare.
- Identifica le informazioni che hai a disposizione: Quali sono la massa, il volume, la pressione, la temperatura o la concentrazione che ti vengono forniti?
- Scegli la formula appropriata: In base alle informazioni che hai, scegli la formula corretta per calcolare il numero di moli.
- Converti le unità di misura: Assicurati che tutte le unità di misura siano coerenti (ad esempio, litri invece di millilitri, Kelvin invece di gradi Celsius).
- Risolvi l'equazione: Inserisci i valori nella formula e calcola il numero di moli.
- Verifica la tua risposta: Assicurati che la tua risposta abbia senso in termini di grandezza e unità di misura.
La pratica rende perfetti! Più problemi di stechiometria risolvi, più diventerai bravo a calcolare il numero di moli. Non aver paura di chiedere aiuto al tuo insegnante o ai tuoi compagni di classe se hai difficoltà. Ci sono anche molte risorse online che possono aiutarti a capire meglio questo concetto.
In definitiva, padroneggiare il concetto di moli non è solo un requisito per superare un esame di chimica. È un potente strumento che ti permette di comprendere e prevedere il comportamento delle sostanze chimiche, svelando i segreti del mondo che ci circonda. È un passo fondamentale verso una comprensione più profonda della scienza e delle sue applicazioni pratiche.
Ora che hai imparato come calcolare il numero di moli, qual è la prossima reazione chimica che vorresti esplorare?