Cos è Il Numero Di Massa

Ti sei mai sentito sopraffatto cercando di capire la tavola periodica degli elementi? Tutti quei numeri, simboli... sembra quasi un codice segreto! Molti studenti, e non solo, si trovano in difficoltà di fronte a concetti come il numero di massa. Ma non preoccuparti, non sei solo. La chimica può sembrare complessa all'inizio, ma con la giusta guida e un po' di chiarezza, anche gli argomenti più ostici diventano accessibili.
Cos'è il Numero di Massa? Un'Introduzione Semplice
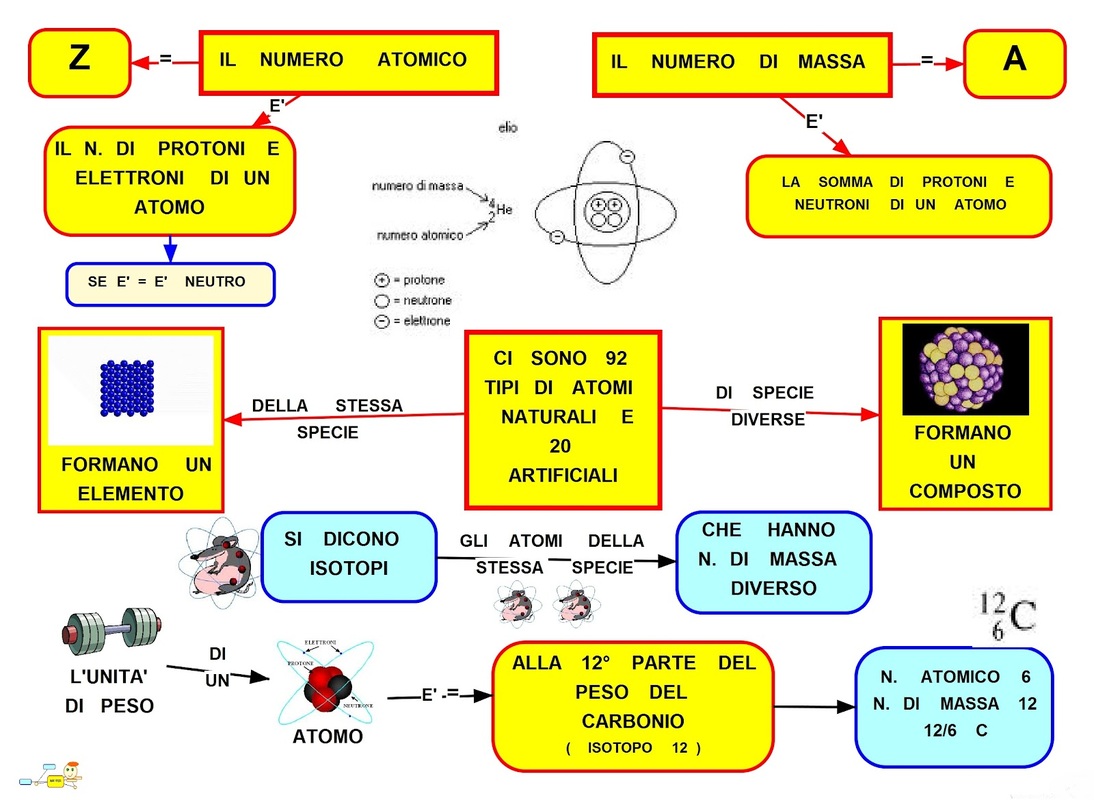
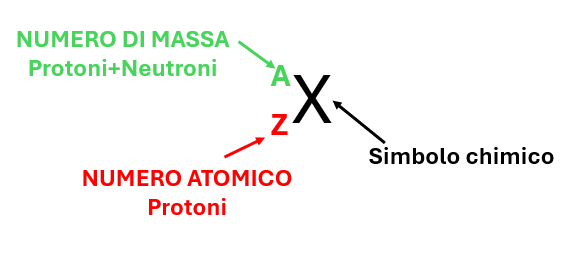
Il numero di massa, spesso indicato con la lettera A, è un concetto fondamentale in chimica e fisica. In termini semplici, il numero di massa di un atomo rappresenta il numero totale di protoni e neutroni presenti nel suo nucleo. Ricorda che il nucleo atomico è la parte centrale dell'atomo, dove si concentra quasi tutta la sua massa.
Come afferma il Prof. Alessandro Volta (ovviamente, un riferimento fittizio a un grande scienziato italiano!): "Comprendere il numero di massa è come avere la chiave per sbloccare molti misteri dell'atomo. Senza di esso, la nostra comprensione della materia rimane incompleta."
Must Read
Perché i Protoni e i Neutroni sono Importanti?
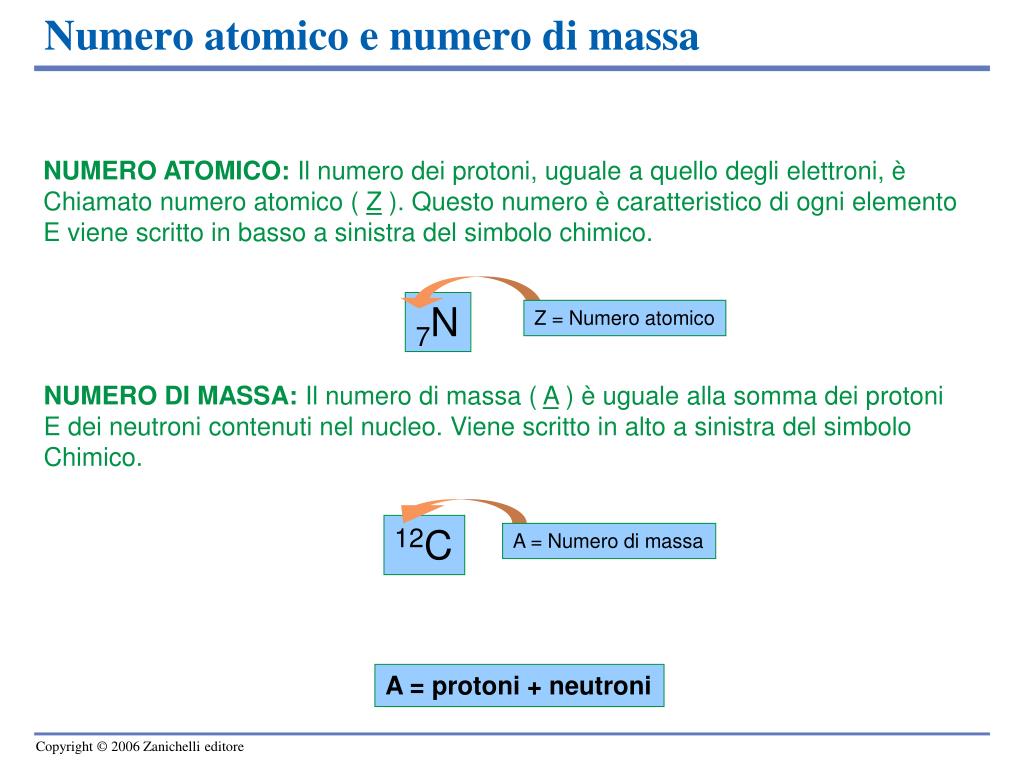
- Protoni: I protoni sono particelle con carica positiva. Il numero di protoni determina l'elemento chimico a cui l'atomo appartiene. Ad esempio, tutti gli atomi con 1 protone sono idrogeno, quelli con 6 protoni sono carbonio e così via. Questo numero di protoni è anche noto come numero atomico (simbolo Z).
- Neutroni: I neutroni sono particelle neutre (senza carica). I neutroni contribuiscono alla massa dell'atomo e contribuiscono a stabilizzare il nucleo. Il numero di neutroni può variare anche per atomi dello stesso elemento, dando origine agli isotopi.
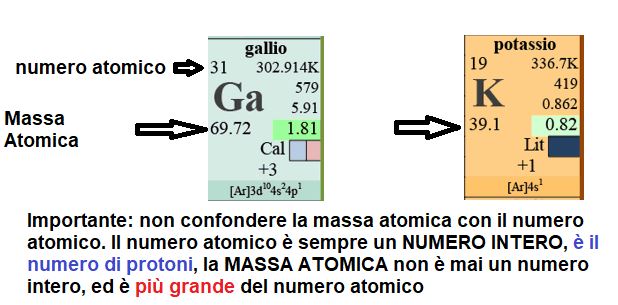
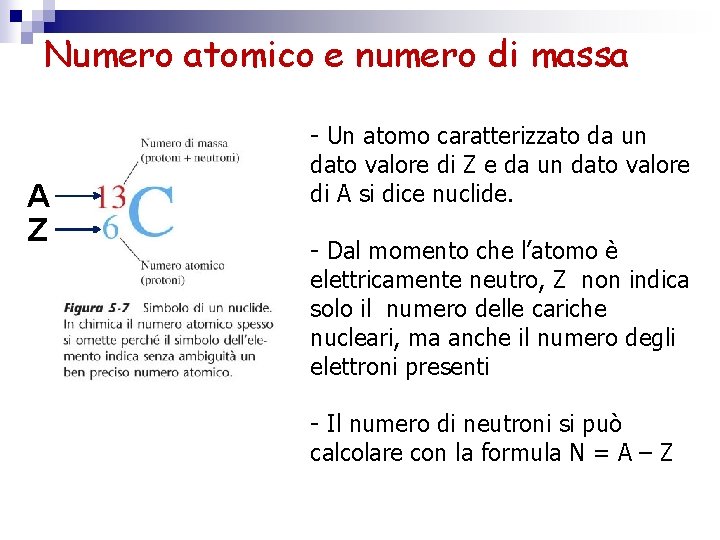
È cruciale distinguere tra il numero di massa (A) e il numero atomico (Z). Il numero atomico identifica l'elemento, mentre il numero di massa indica la massa approssimativa del nucleo.
Come Calcolare il Numero di Massa
Il calcolo del numero di massa è piuttosto semplice:
Numero di Massa (A) = Numero di Protoni (Z) + Numero di Neutroni (N)

Quindi, per trovare il numero di massa, devi solo sommare il numero di protoni e il numero di neutroni in un dato atomo. Vediamo alcuni esempi:
Esempi Pratici
- Carbonio-12 (12C): Il carbonio ha sempre 6 protoni (numero atomico Z = 6). Il carbonio-12 ha 6 neutroni. Quindi, il suo numero di massa è A = 6 (protoni) + 6 (neutroni) = 12.
- Ossigeno-16 (16O): L'ossigeno ha sempre 8 protoni (numero atomico Z = 8). L'ossigeno-16 ha 8 neutroni. Quindi, il suo numero di massa è A = 8 (protoni) + 8 (neutroni) = 16.
- Uranio-238 (238U): L'uranio ha sempre 92 protoni (numero atomico Z = 92). L'uranio-238 ha 146 neutroni. Quindi, il suo numero di massa è A = 92 (protoni) + 146 (neutroni) = 238.
Questi esempi dimostrano come il numero di massa è strettamente legato all'isotopo specifico di un elemento.
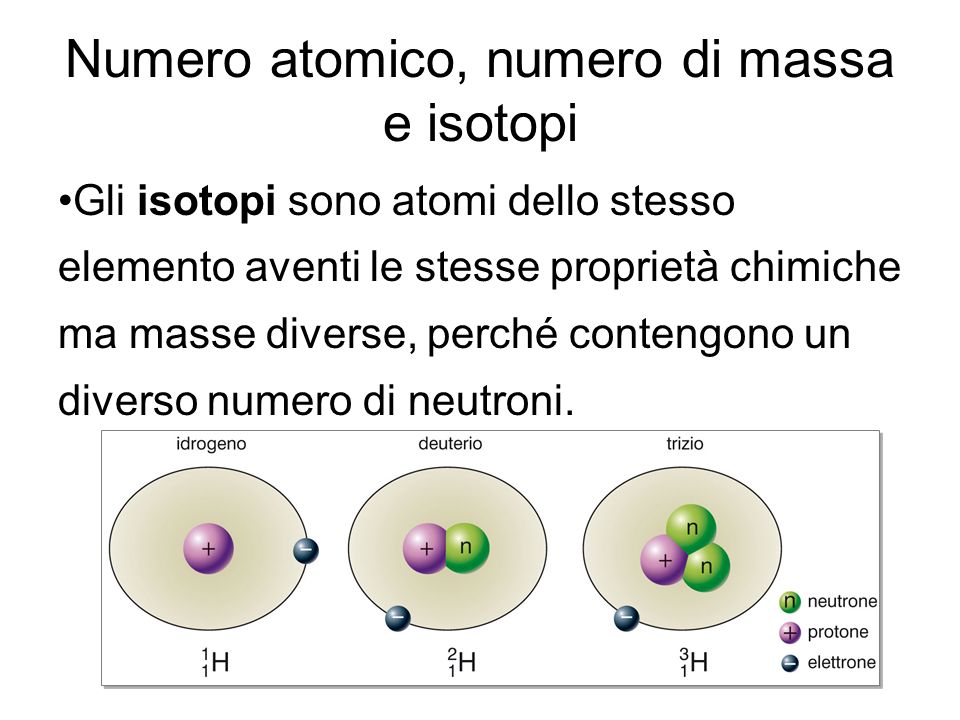
Isotopi: Variazioni dello Stesso Elemento
Come accennato in precedenza, gli isotopi sono atomi dello stesso elemento (stesso numero di protoni) ma con un diverso numero di neutroni. Questo significa che gli isotopi hanno lo stesso numero atomico ma diverso numero di massa.

Ad esempio, il carbonio ha diversi isotopi, tra cui:
- Carbonio-12 (12C): 6 protoni, 6 neutroni, A = 12 (abbondanza naturale: circa 98.9%)
- Carbonio-13 (13C): 6 protoni, 7 neutroni, A = 13 (abbondanza naturale: circa 1.1%)
- Carbonio-14 (14C): 6 protoni, 8 neutroni, A = 14 (è un isotopo radioattivo usato nella datazione al radiocarbonio)
Sebbene gli isotopi abbiano proprietà chimiche simili (perché dipendono dal numero di elettroni, che è lo stesso), possono avere proprietà fisiche diverse, come la massa, e alcuni possono essere radioattivi.
L'Importanza degli Isotopi
Gli isotopi hanno un'importanza cruciale in diverse aree della scienza e della tecnologia, tra cui:

- Datazione Radiometrica: Isotopi radioattivi come il carbonio-14 e l'uranio-238 sono utilizzati per datare reperti archeologici e geologici.
- Medicina: Alcuni isotopi radioattivi sono utilizzati in diagnostica per immagini (es. scintigrafia) e terapia (es. radioterapia).
- Chimica: Gli isotopi stabili (non radioattivi) sono utilizzati come traccianti per studiare meccanismi di reazione e per determinare la composizione di molecole.
- Energia Nucleare: L'uranio-235 è un isotopo fissile utilizzato nelle centrali nucleari per produrre energia.
Come il Numero di Massa Influenza le Proprietà degli Elementi
Anche se il numero di massa non determina direttamente l'elemento (questo è il compito del numero atomico), influenza diverse proprietà fisiche e, indirettamente, chimiche.
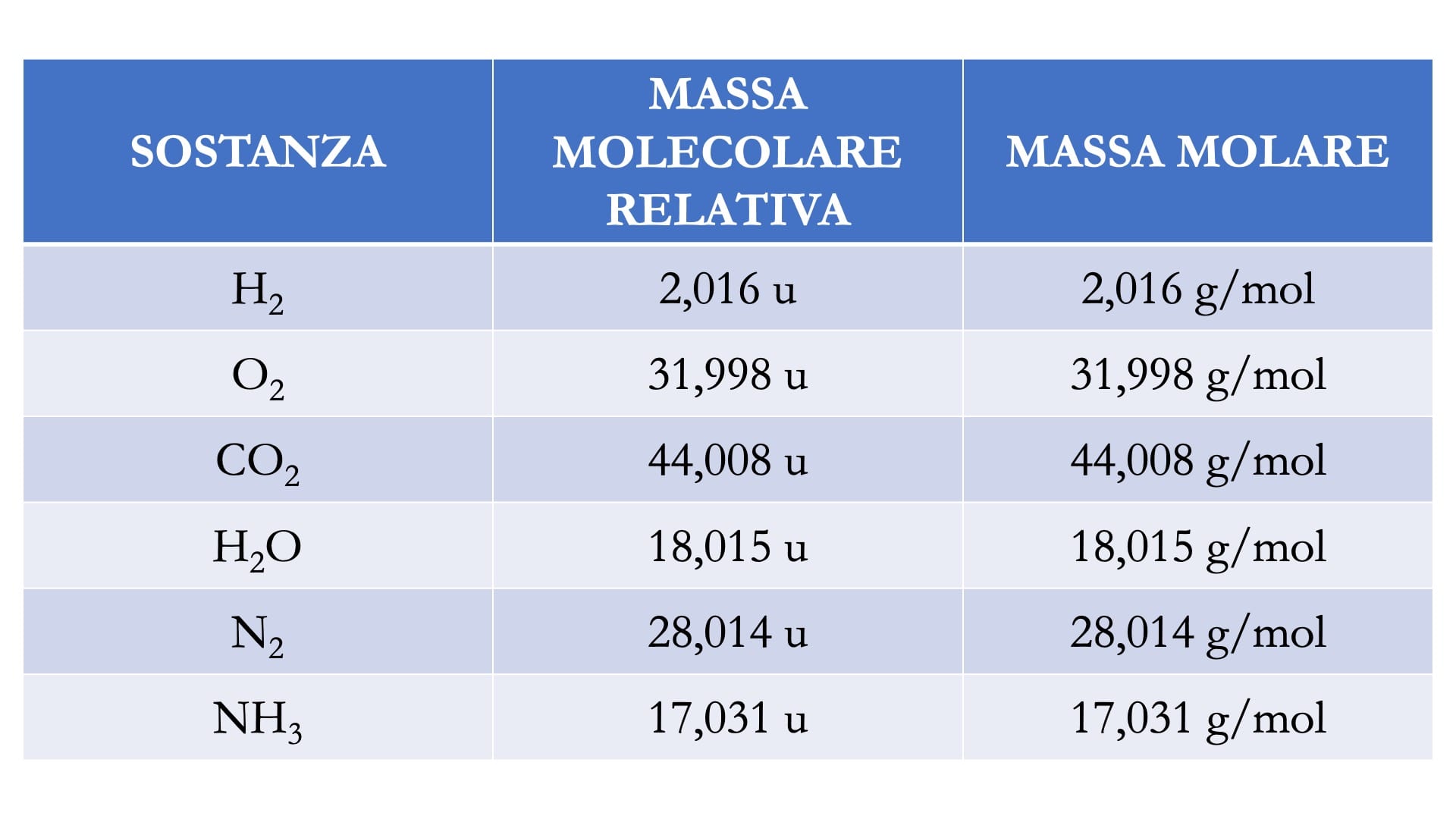
Massa Atomica: Il numero di massa fornisce un'approssimazione della massa atomica di un atomo. La massa atomica effettiva, espressa in unità di massa atomica (u.m.a. o Dalton), è leggermente diversa dal numero di massa a causa del difetto di massa, un effetto relativistico legato all'energia di legame nucleare. Tuttavia, il numero di massa è un ottimo punto di partenza per stimare la massa atomica.
Densità: La densità di un elemento o di un composto è influenzata dalla massa dei suoi atomi. Isotopi più pesanti di un elemento tenderanno a formare sostanze leggermente più dense.

Reazioni Nucleari: Il numero di massa è fondamentale per bilanciare le equazioni nelle reazioni nucleari. La somma dei numeri di massa dei reagenti deve essere uguale alla somma dei numeri di massa dei prodotti.
Strumenti e Metodi per Comprendere Meglio il Numero di Massa
Ecco alcuni strumenti e metodi che possono aiutarti a consolidare la tua comprensione del numero di massa:
- Tavola Periodica Interattiva: Utilizza una tavola periodica online interattiva che mostri il numero atomico, il numero di massa e gli isotopi per ciascun elemento. Ci sono molte risorse gratuite disponibili.
- Esercizi di Calcolo: Fai esercizi di calcolo del numero di massa a partire dal numero di protoni e neutroni, e viceversa. Questo ti aiuterà a familiarizzare con la formula.
- Modelli Atomici: Costruisci modelli atomici (anche semplici, con palline e stuzzicadenti) per visualizzare il nucleo e il numero di protoni e neutroni.
- Flashcard: Crea flashcard con domande sul numero di massa, gli isotopi e la loro importanza.
- Risorse Online: Utilizza video esplicativi, articoli e quiz online per approfondire la tua conoscenza. Siti come Khan Academy offrono ottimi materiali gratuiti.
Conclusione: Il Numero di Massa, una Chiave per Comprendere l'Atomo
Capire il numero di massa è un passo fondamentale nel tuo percorso di apprendimento della chimica. Non scoraggiarti se all'inizio sembra complicato. Con un po' di pratica e gli strumenti giusti, sarai in grado di padroneggiare questo concetto e di apprezzare la bellezza e la complessità del mondo atomico.
Ricorda le parole di Marie Curie: "Non c'è bisogno di avere paura di niente nella vita, bisogna solo capire. Ora è il momento di capire di più, in modo da aver meno paura." Quindi, continua a esplorare, a imparare e a porre domande. Il numero di massa è solo l'inizio di un'avventura entusiasmante nel mondo della chimica!






..jpg)