Cos è L Energia Di Ionizzazione
Ti sei mai chiesto cosa tiene insieme la materia che ci circonda? Come fanno gli atomi a formare molecole stabili, e cosa serve per separarli? La risposta a queste domande si trova, in parte, in un concetto fondamentale della chimica e della fisica: l'energia di ionizzazione. Questo articolo è pensato per chiunque voglia comprendere meglio questo concetto, dagli studenti di scuola superiore agli appassionati di scienze. Cercheremo di spiegarlo in modo chiaro e accessibile, senza perdersi in tecnicismi eccessivi.
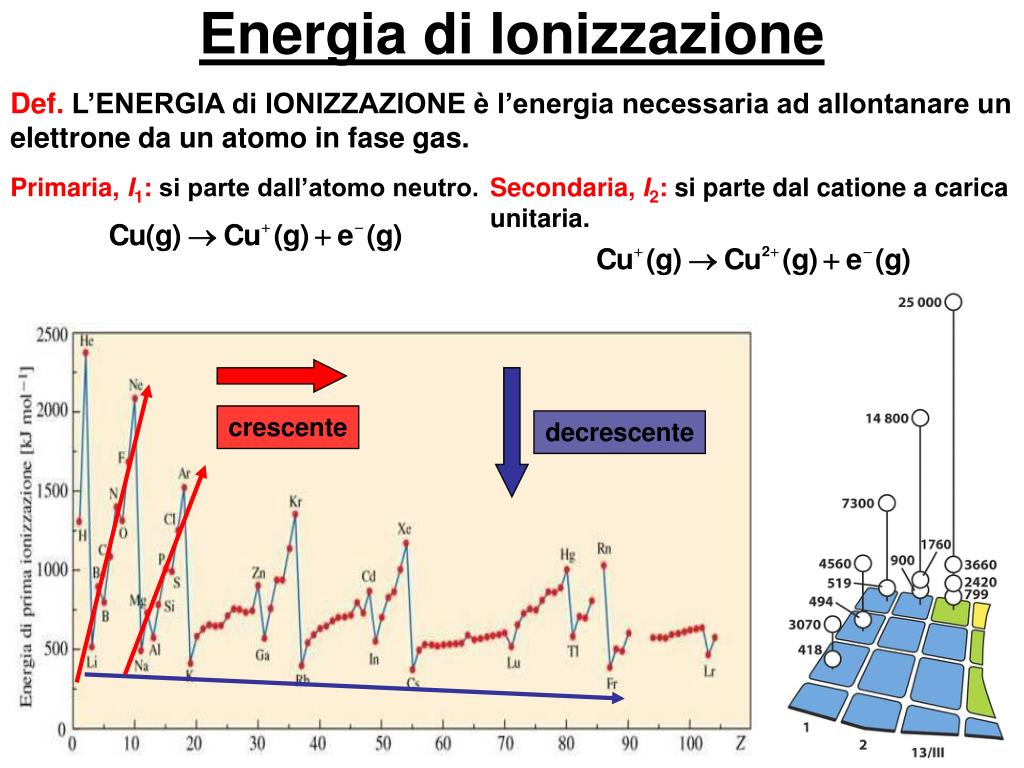
Immagina un atomo come un piccolo sistema solare, con il nucleo al centro (come il sole) e gli elettroni che orbitano intorno (come i pianeti). Questi elettroni sono tenuti "in orbita" da una forza di attrazione elettromagnetica. L'energia di ionizzazione è la quantità di energia necessaria per strappare l'elettrone più esterno da questo atomo, trasformandolo in uno ione positivo.
Cos'è esattamente l'Energia di Ionizzazione?
L'energia di ionizzazione, a volte chiamata anche potenziale di ionizzazione, è definita come l'energia minima richiesta per rimuovere un elettrone da un atomo o ione gassoso nel suo stato fondamentale. Matematicamente, possiamo rappresentare il processo per un atomo neutro (X) come:
Must Read
X(g) + Energia → X+(g) + e-
Dove:
- X(g) rappresenta l'atomo neutro in fase gassosa.
- X+(g) rappresenta lo ione positivo in fase gassosa.
- e- rappresenta l'elettrone rimosso.
L'energia di ionizzazione è espressa tipicamente in kilojoule per mole (kJ/mol) o in elettronvolt (eV). Un valore elevato di energia di ionizzazione indica che è difficile rimuovere un elettrone dall'atomo, mentre un valore basso indica che l'elettrone è più facilmente rimovibile.

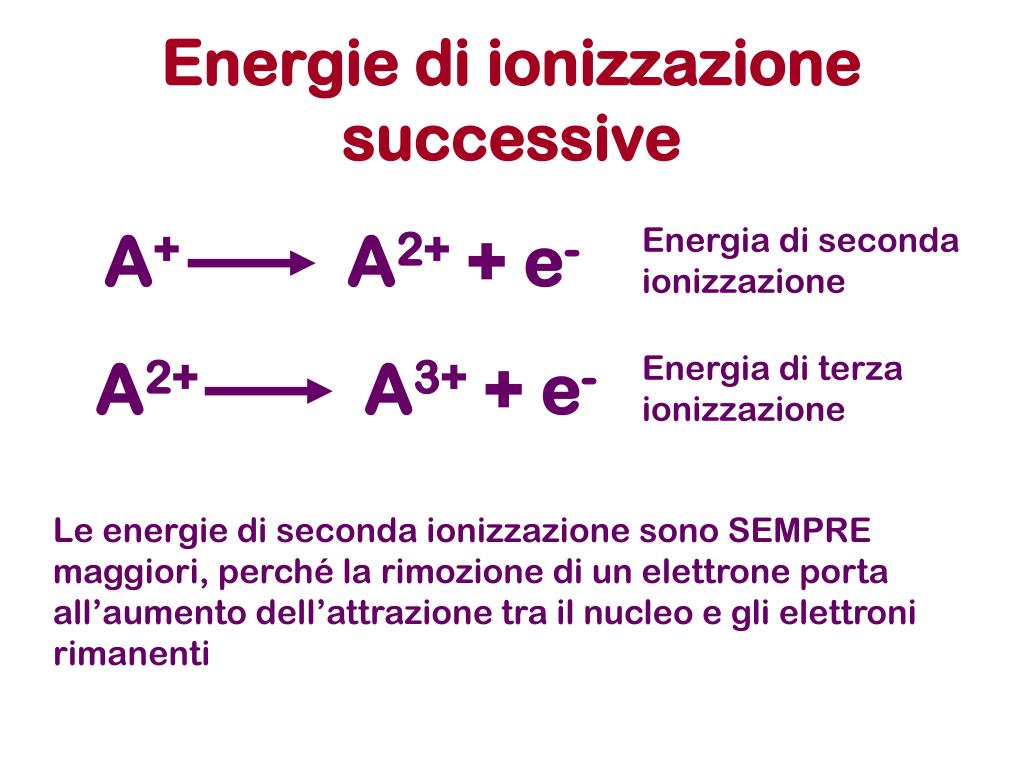
Energia di Ionizzazione Successiva
Non bisogna dimenticare che un atomo possiede più elettroni. Dopo aver rimosso il primo elettrone, possiamo rimuoverne un secondo, un terzo, e così via. L'energia necessaria per rimuovere il secondo elettrone è detta seconda energia di ionizzazione, quella per il terzo è la terza energia di ionizzazione, e così via. Generalmente, l'energia di ionizzazione aumenta con la rimozione successiva degli elettroni. Questo perché, dopo ogni rimozione, l'attrazione del nucleo sugli elettroni rimanenti diventa più forte, rendendo più difficile la successiva rimozione.
Ad esempio, considera l'alluminio (Al). La sua prima energia di ionizzazione è relativamente bassa, perché rimuovere il primo elettrone è abbastanza facile. La seconda energia di ionizzazione è più alta, ma ancora relativamente gestibile. Tuttavia, la terza energia di ionizzazione è molto più alta delle prime due. Questo perché l'alluminio tende a formare ioni Al3+, e la rimozione di un quarto elettrone richiederebbe rompere una configurazione elettronica stabile.
Fattori che influenzano l'Energia di Ionizzazione
Diversi fattori influenzano l'energia di ionizzazione di un elemento:

- Carica nucleare effettiva: Maggiore è la carica positiva effettiva che un elettrone "sente" dal nucleo, maggiore sarà l'attrazione e quindi maggiore l'energia necessaria per rimuoverlo. La carica nucleare effettiva è la carica positiva del nucleo diminuita dall'effetto di schermatura degli elettroni interni.
- Distanza dal nucleo: Gli elettroni più vicini al nucleo sono più fortemente attratti e richiedono più energia per essere rimossi. Gli elettroni più esterni, trovandosi a una distanza maggiore, sono meno attratti e più facili da rimuovere.
- Schermatura elettronica: Gli elettroni interni schermano parzialmente gli elettroni esterni dalla carica positiva del nucleo. Maggiore è la schermatura, minore è l'energia di ionizzazione.
- Configurazione elettronica: Gli atomi con configurazioni elettroniche stabili (come quelle dei gas nobili, con l'ottetto completo) hanno energie di ionizzazione molto elevate. Questo perché la rimozione di un elettrone distruggerebbe questa configurazione stabile.
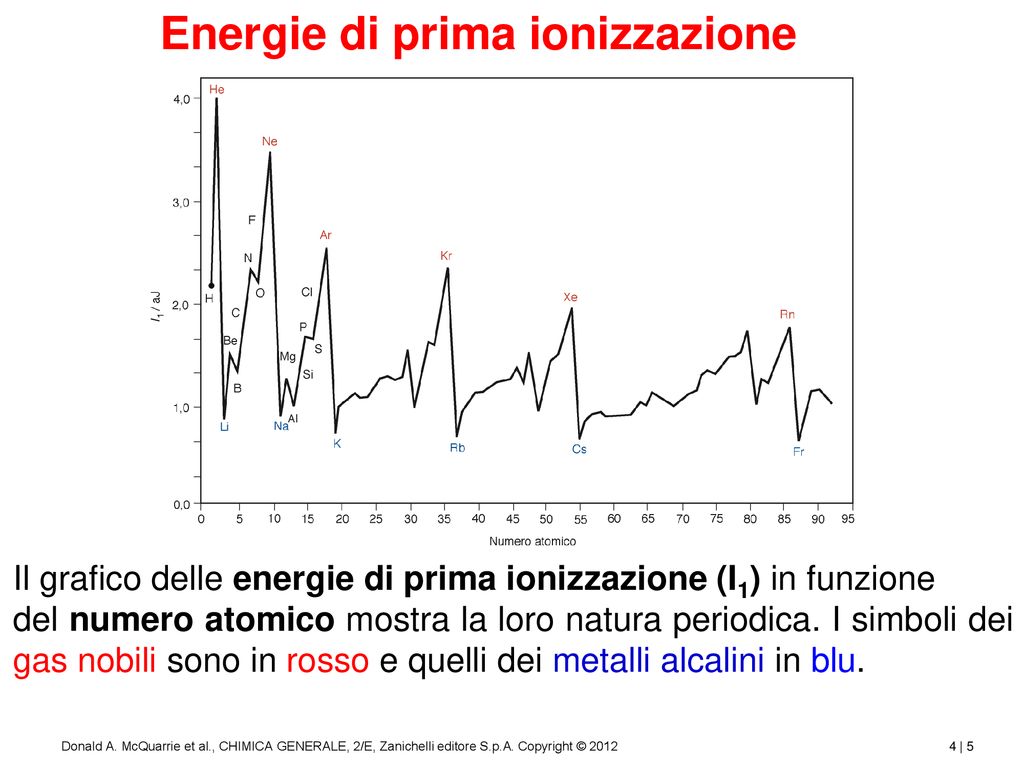
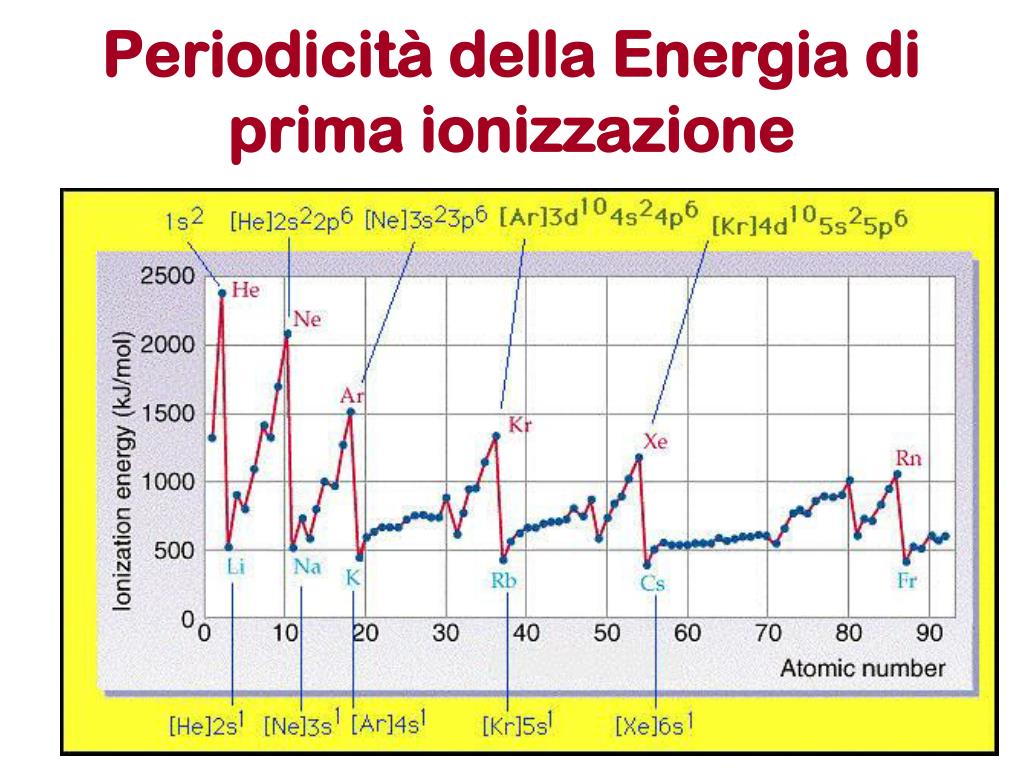
Trend periodici dell'Energia di Ionizzazione
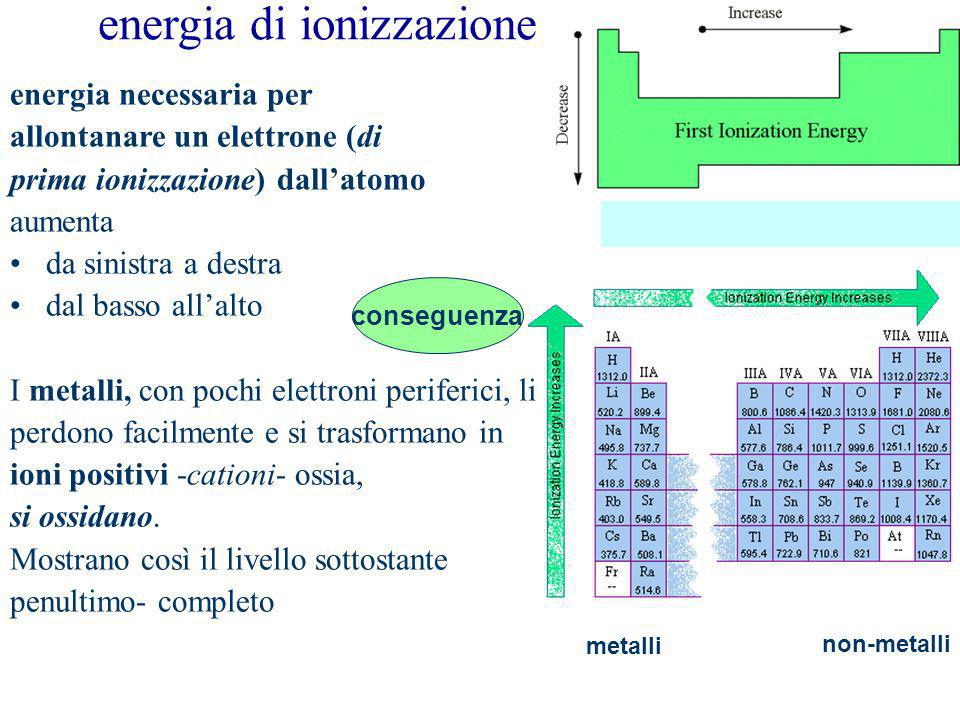
L'energia di ionizzazione mostra dei trend ben definiti nella tavola periodica:
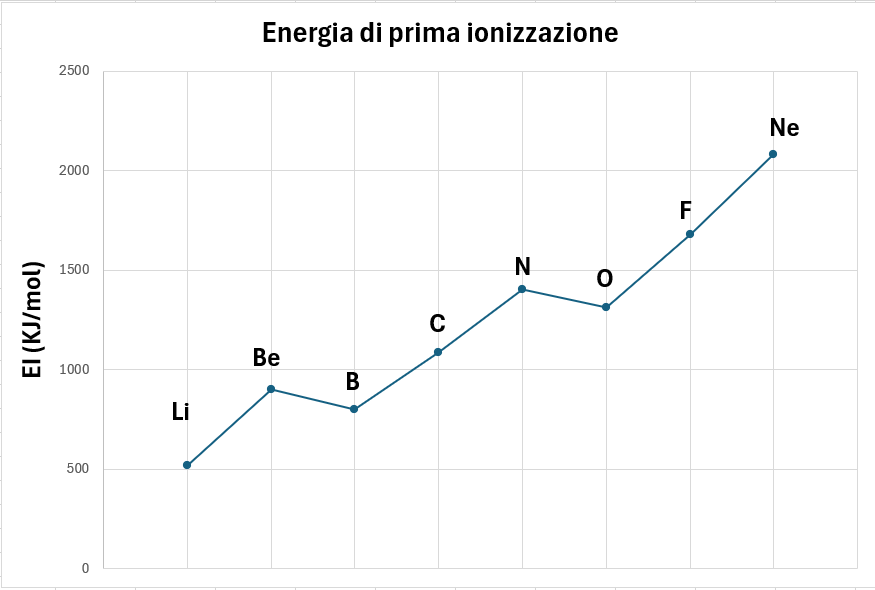
- Lungo un periodo (da sinistra a destra): L'energia di ionizzazione generalmente aumenta. Questo perché, lungo un periodo, la carica nucleare effettiva aumenta, attirando gli elettroni più fortemente.
- Lungo un gruppo (dall'alto verso il basso): L'energia di ionizzazione generalmente diminuisce. Questo perché, lungo un gruppo, gli elettroni più esterni si trovano a distanze sempre maggiori dal nucleo, e l'effetto schermante degli elettroni interni aumenta.
Esistono alcune eccezioni a questi trend generali, dovute a particolari configurazioni elettroniche.
Importanza dell'Energia di Ionizzazione
L'energia di ionizzazione è un concetto fondamentale per diverse ragioni:
- Prevedere la reattività chimica: Gli elementi con basse energie di ionizzazione tendono a perdere elettroni facilmente e formare ioni positivi (cationi), comportandosi come metalli. Gli elementi con alte energie di ionizzazione tendono a guadagnare elettroni o a condividere elettroni, comportandosi come non metalli.
- Comprendere i legami chimici: La differenza di energia di ionizzazione tra due atomi che si legano può indicare il tipo di legame che si formerà. Ad esempio, una grande differenza suggerisce un legame ionico, mentre una piccola differenza suggerisce un legame covalente.
- Spettroscopia: L'energia di ionizzazione può essere misurata sperimentalmente tramite tecniche spettroscopiche, fornendo informazioni sulla struttura elettronica degli atomi e delle molecole.
In parole povere, l'energia di ionizzazione ci aiuta a capire come gli atomi interagiscono tra loro, formando la miriade di sostanze che conosciamo. Pensiamo, ad esempio, alla formazione del cloruro di sodio (sale da cucina). Il sodio (Na) ha una bassa energia di ionizzazione, mentre il cloro (Cl) ha un'elevata affinità elettronica (la tendenza ad acquistare un elettrone). Il sodio perde facilmente un elettrone, formando uno ione Na+, mentre il cloro acquista l'elettrone, formando uno ione Cl-. L'attrazione elettrostatica tra questi ioni opposti porta alla formazione del legame ionico nel cloruro di sodio.
Anche i legami covalenti, come quelli che tengono insieme le molecole d'acqua (H2O), sono influenzati indirettamente dall'energia di ionizzazione. Sebbene in questo caso gli elettroni siano condivisi anziché trasferiti completamente, l'energia di ionizzazione degli atomi coinvolti influenza la polarità del legame e, di conseguenza, le proprietà della molecola.
Esempi Pratici e Applicazioni
Oltre alle applicazioni teoriche, l'energia di ionizzazione trova impiego in diverse tecnologie:
- Spettrometria di massa: Questa tecnica analitica utilizza l'energia di ionizzazione per ionizzare le molecole di un campione, separando poi gli ioni in base al loro rapporto massa/carica. Questo permette di identificare e quantificare i diversi componenti del campione.
- Fotoelettronica spettroscopia (PES): PES è una tecnica sensibile alla superficie che utilizza l'effetto fotoelettrico (l'emissione di elettroni da un materiale quando viene colpito da fotoni) per studiare la struttura elettronica dei materiali. L'energia cinetica degli elettroni emessi è direttamente correlata all'energia di ionizzazione degli orbitali da cui provengono.
- Laser a gas ionizzato: Alcuni tipi di laser utilizzano gas ionizzati come mezzo attivo. L'energia di ionizzazione degli atomi del gas è un parametro cruciale per determinare la lunghezza d'onda e la potenza del laser.
Inoltre, la conoscenza dell'energia di ionizzazione è fondamentale nella progettazione di nuovi materiali con proprietà specifiche. Ad esempio, nello sviluppo di celle solari, è importante scegliere materiali con energie di ionizzazione appropriate per massimizzare l'efficienza di conversione dell'energia solare in energia elettrica.
In conclusione, l'energia di ionizzazione è un concetto chiave per comprendere la chimica e la fisica degli atomi e delle molecole. Ci permette di prevedere la reattività chimica, capire i legami chimici e sviluppare nuove tecnologie. Speriamo che questo articolo ti abbia fornito una panoramica chiara e accessibile di questo importante concetto.
Ora, la prossima volta che sentirai parlare di energia di ionizzazione, potrai visualizzare un atomo e immaginare quanta energia serve per strappargli via un elettrone, aprendo la porta a un intero mondo di reazioni e trasformazioni chimiche. Capire questo concetto ci aiuta ad apprezzare la complessità e l'eleganza della natura che ci circonda.

.jpg)







.jpg)