Da Cosa è Composto Un Atomo
Ciao a tutti! Se siete qui, probabilmente siete curiosi di sapere di cosa è fatto un atomo. Magari siete genitori che cercano di aiutare i propri figli con i compiti di scienze, oppure studenti che vogliono capire meglio questo argomento fondamentale. Qualunque sia la vostra ragione, spero di rendere questo viaggio nel mondo dell'atomo il più semplice e interessante possibile. So che la chimica e la fisica possono sembrare un po' spaventose all'inizio, ma vi assicuro che con un po' di pazienza e le giuste spiegazioni, tutto diventa più chiaro.
Un Atomo: Il Mattoncino Fondamentale della Materia
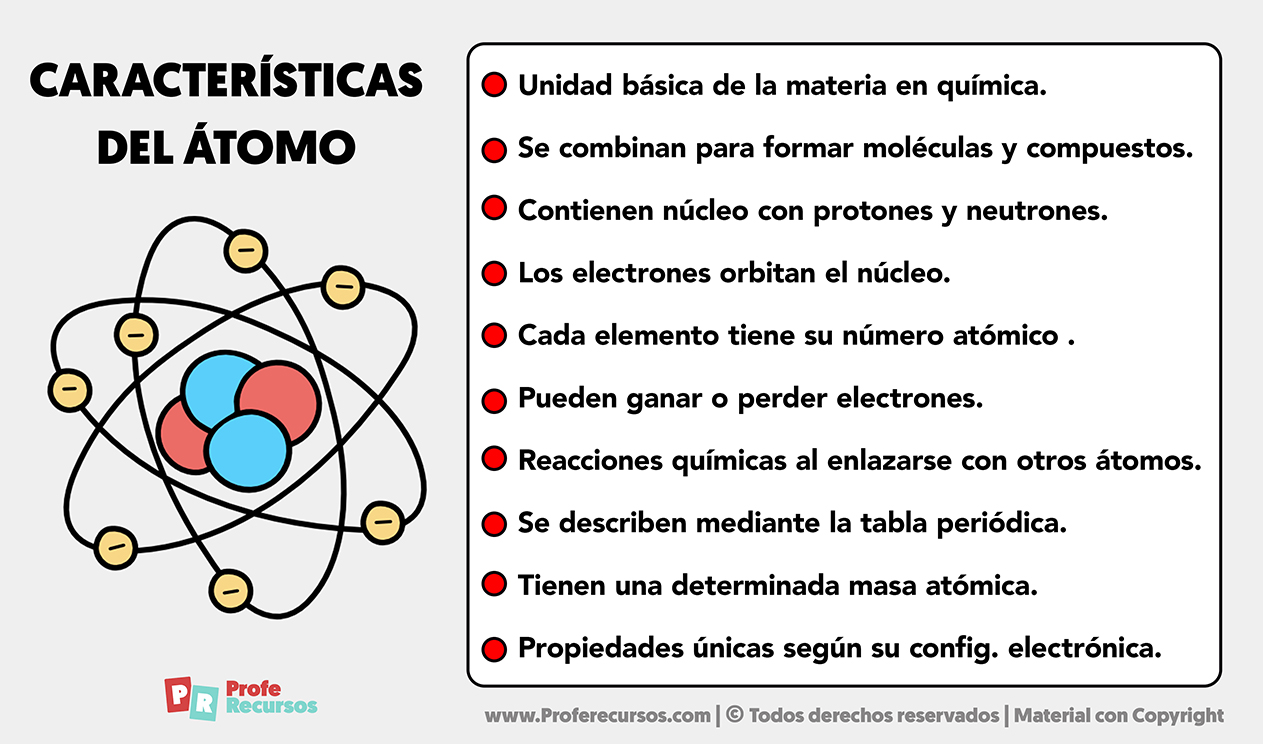
Immaginate di costruire una casa. Avrete bisogno di mattoni, giusto? Ecco, l'atomo è un po' come il mattone fondamentale con cui è costruita tutta la materia che ci circonda. Tutto, dal tavolo su cui state leggendo questo articolo, all'aria che respirate, fino a voi stessi, è fatto di atomi. Ma cosa c'è dentro questo "mattone" così speciale?
Per capire bene, partiamo da un'analogia. Immaginate un piccolo sistema solare. Al centro c'è il Sole, attorno al quale ruotano i pianeti. L'atomo è un po' simile, ma invece del Sole e dei pianeti, abbiamo altre particelle.
Must Read
Le Parti dell'Atomo: Un Viaggio al Microscopic
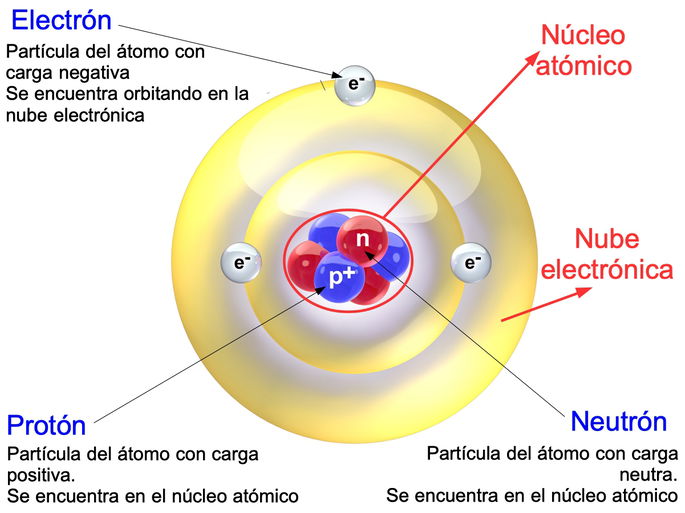
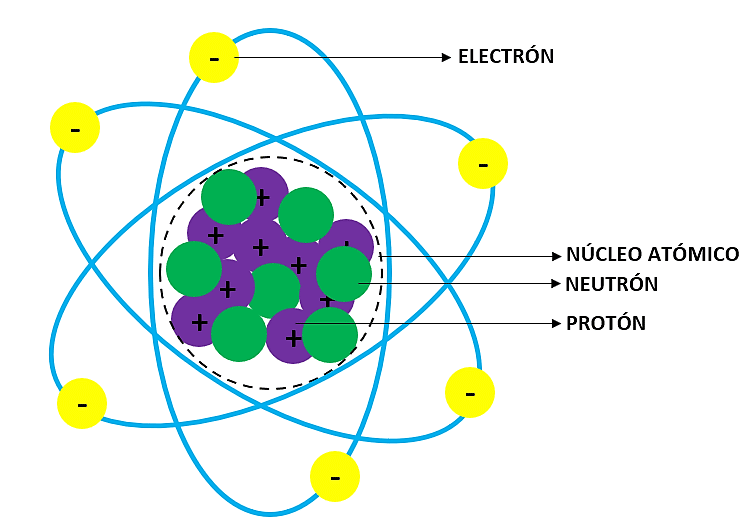
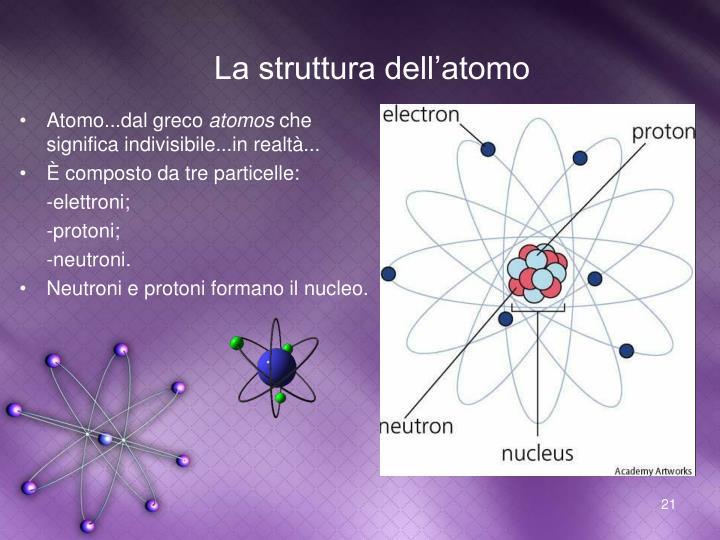
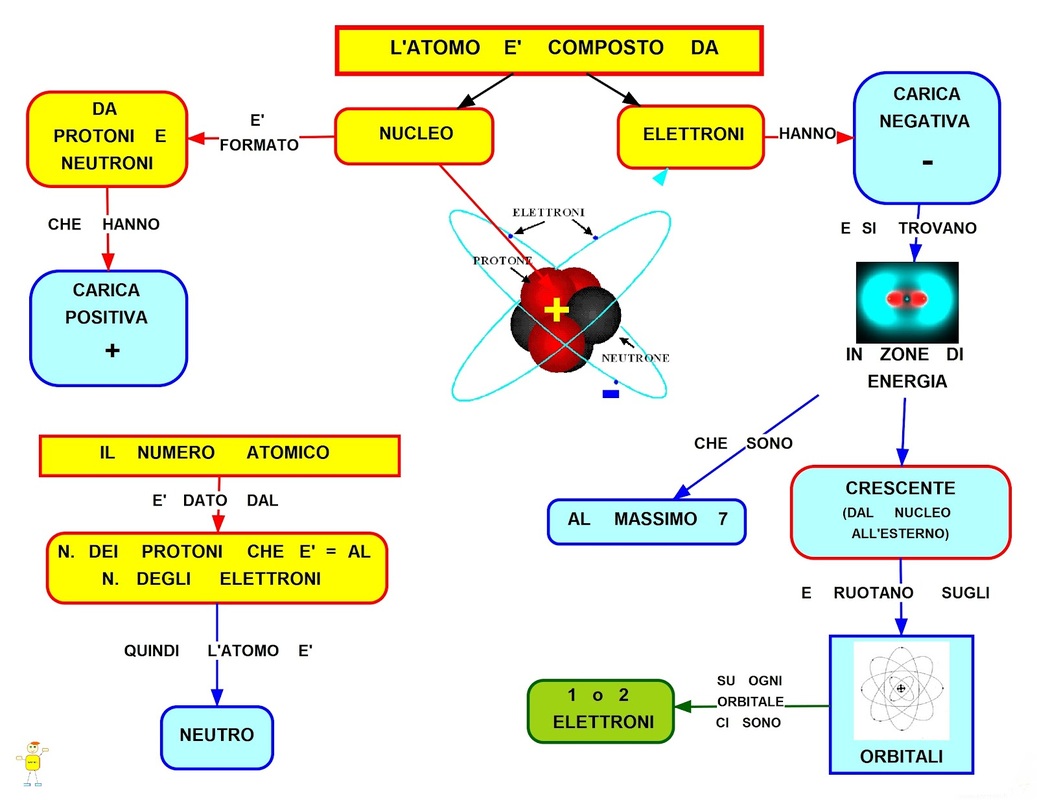
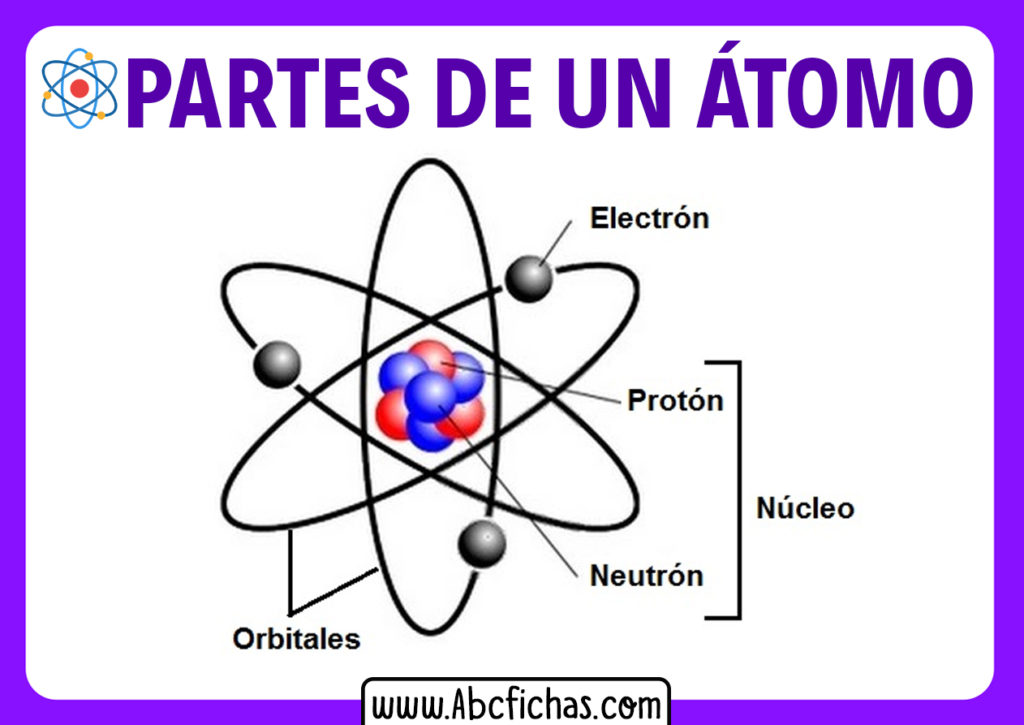
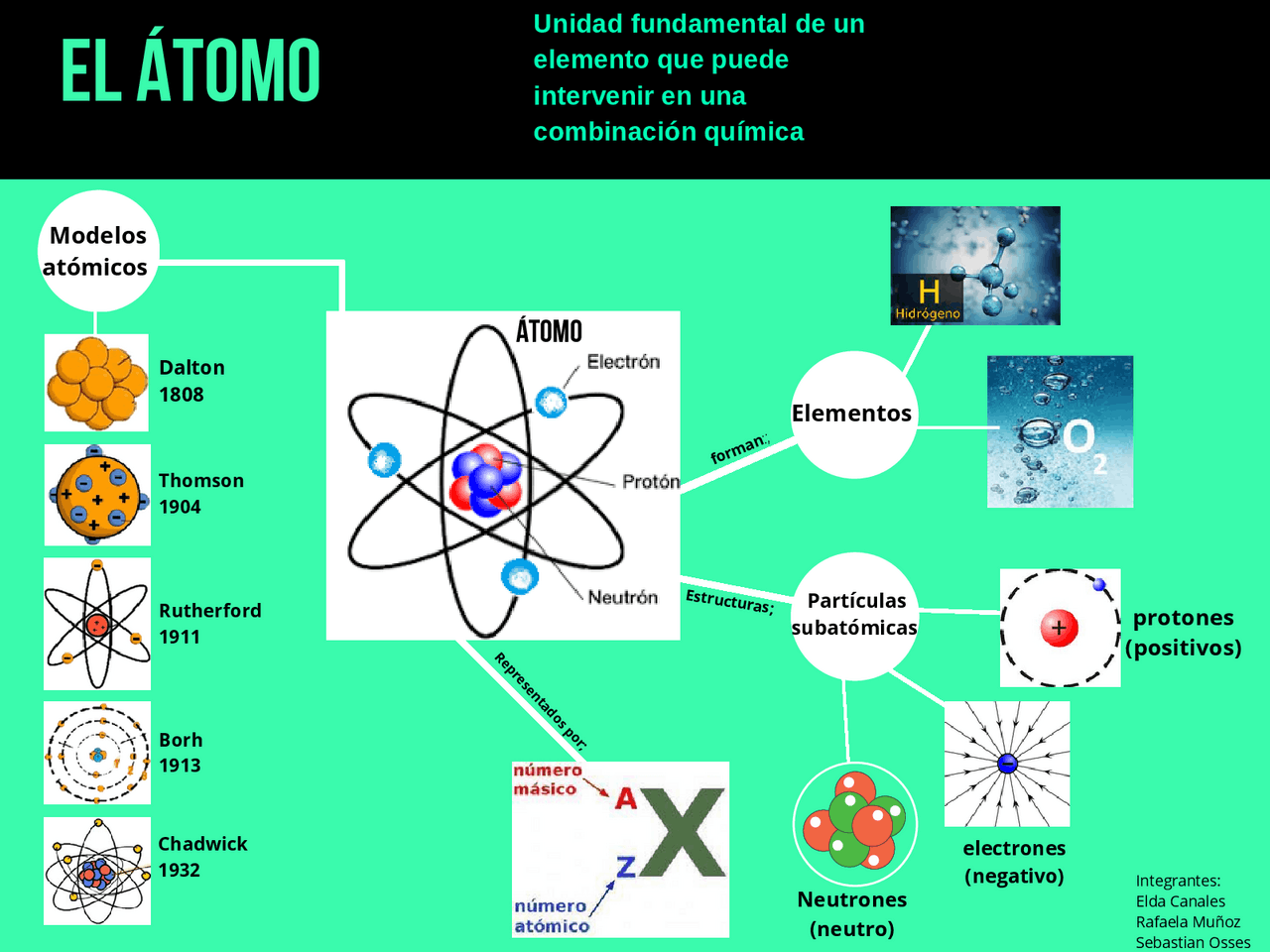
Un atomo è composto principalmente da tre tipi di particelle subatomiche:
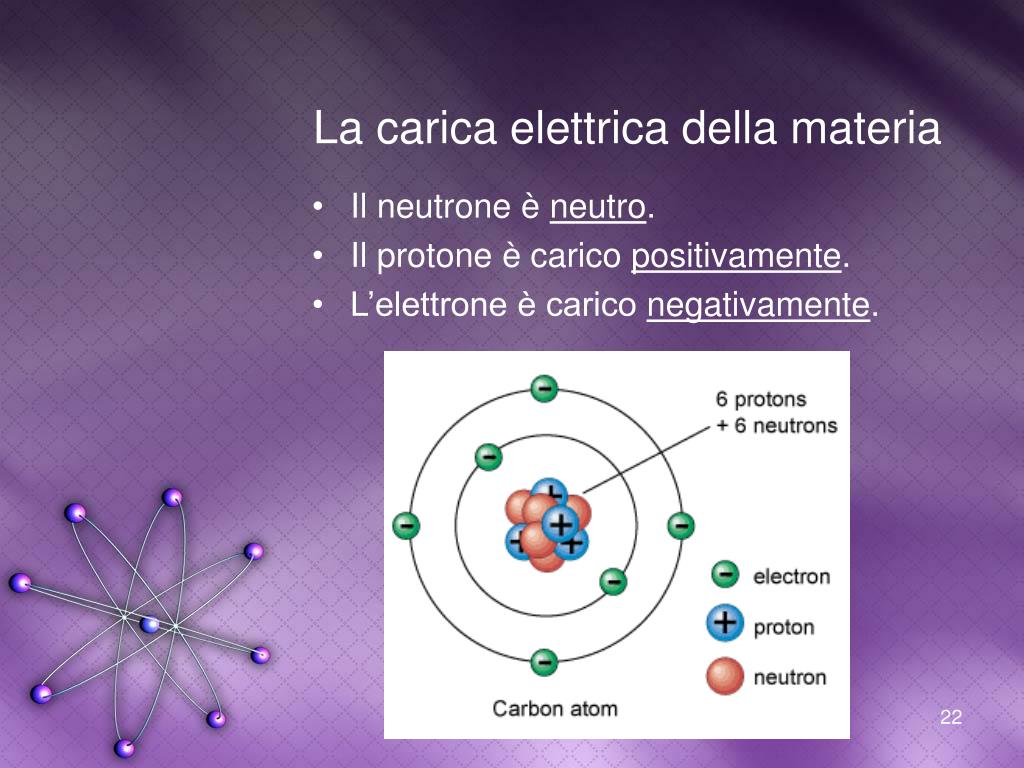
- Protoni: Hanno una carica elettrica positiva. Si trovano nel nucleo dell'atomo. Pensate al nucleo come al Sole del nostro sistema solare atomico. Il numero di protoni determina l'elemento chimico a cui l'atomo appartiene. Ad esempio, tutti gli atomi con un protone sono atomi di idrogeno, tutti quelli con sei protoni sono atomi di carbonio, e così via.
- Neutroni: Non hanno carica elettrica (sono neutri, appunto). Anche loro si trovano nel nucleo, insieme ai protoni. I neutroni contribuiscono alla massa dell'atomo e aiutano a stabilizzare il nucleo.
- Elettroni: Hanno una carica elettrica negativa. A differenza dei protoni e dei neutroni, gli elettroni non si trovano nel nucleo. Ruotano attorno al nucleo in "orbite" o "gusci" specifici, proprio come i pianeti attorno al Sole.
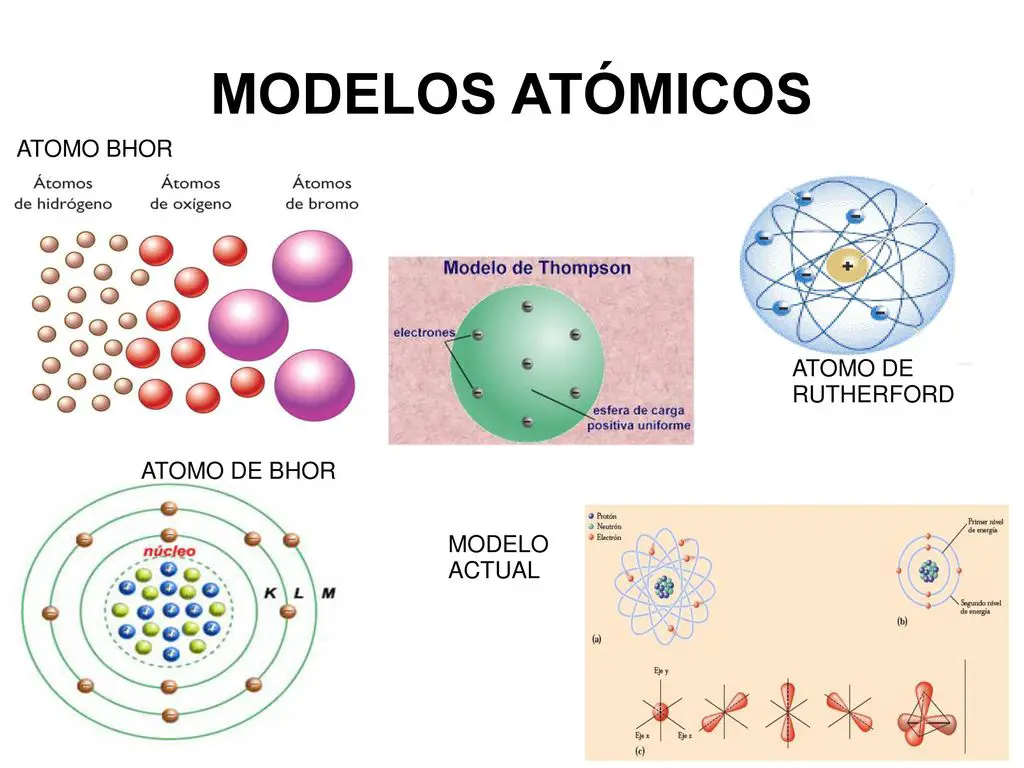
Ricordate l'analogia del sistema solare? Beh, anche se è utile per iniziare, è importante sapere che gli elettroni non ruotano attorno al nucleo in orbite perfettamente definite come i pianeti. Piuttosto, si muovono in regioni di spazio chiamate orbitali, dove è più probabile trovarli. Immaginate gli orbitali come nuvole di probabilità che circondano il nucleo.

Un insegnante di chimica del liceo, la professoressa Rossi, mi ha detto una volta: "Spiego sempre ai miei studenti che è come cercare di fotografare un colibrì. Sai che è lì, ma non sai esattamente dove sarà nel prossimo istante. Gli elettroni sono un po' così!".
Carica Elettrica e Numero Atomico
Gli atomi sono, nella maggior parte dei casi, elettricamente neutri. Questo significa che il numero di protoni (cariche positive) è uguale al numero di elettroni (cariche negative). Quando un atomo guadagna o perde elettroni, diventa uno ione: se perde elettroni diventa uno ione positivo (catione), se guadagna elettroni diventa uno ione negativo (anione).
Il numero atomico di un elemento è il numero di protoni che si trovano nel nucleo di un atomo di quell'elemento. È un numero unico per ogni elemento e lo trovate nella tavola periodica. Ad esempio, l'idrogeno ha numero atomico 1 (un protone), l'elio ha numero atomico 2 (due protoni), e così via.

Massa Atomica
La massa atomica è la massa di un atomo, misurata in unità di massa atomica (u). La maggior parte della massa di un atomo è concentrata nel nucleo, dove si trovano protoni e neutroni. Gli elettroni hanno una massa molto piccola, quindi il loro contributo alla massa atomica totale è trascurabile.
Per calcolare approssimativamente la massa atomica, si somma il numero di protoni e il numero di neutroni nel nucleo. Ad esempio, un atomo di carbonio-12 ha 6 protoni e 6 neutroni, quindi la sua massa atomica è approssimativamente 12 u.
Perché è Importante Capire la Composizione dell'Atomo?
Capire come è fatto un atomo è fondamentale per diverse ragioni:
- Chimica: La composizione dell'atomo determina le proprietà chimiche di un elemento e come questo reagisce con altri elementi per formare composti.
- Fisica: Lo studio dell'atomo è alla base della fisica nucleare e della comprensione delle forze fondamentali della natura.
- Scienza dei Materiali: La comprensione della struttura atomica dei materiali ci permette di sviluppare nuovi materiali con proprietà specifiche, come materiali più resistenti, leggeri o conduttivi.
- Medicina: La conoscenza dell'atomo è cruciale per la diagnostica medica (ad esempio, la risonanza magnetica) e per la terapia (ad esempio, la radioterapia).
Attività Pratiche per Imparare di Più
Ecco alcune attività che potete fare per consolidare la vostra comprensione della composizione dell'atomo:
- Modello dell'Atomo: Costruite un modello di un atomo usando materiali di riciclo, come palline di polistirolo, stuzzicadenti e cartoncino colorato. Assegnate colori diversi ai protoni, neutroni ed elettroni.
- Tavola Periodica Interattiva: Esplorate una tavola periodica interattiva online. Molte tavole periodiche vi permettono di cliccare su un elemento per vedere informazioni dettagliate sulla sua struttura atomica.
- Quiz Online: Cercate quiz online sulla composizione dell'atomo. Mettere alla prova le vostre conoscenze è un ottimo modo per imparare e ricordare concetti chiave.
- Video Esplicativi: Guardate video esplicativi su YouTube o altre piattaforme di video learning. Molti video usano animazioni per rendere più facile la comprensione dei concetti.
Conclusione: Un Mondo Microscopico da Esplorare
Spero che questo viaggio all'interno dell'atomo vi sia piaciuto! Capire di cosa è fatto un atomo è un passo fondamentale per comprendere il mondo che ci circonda. Non abbiate paura di porre domande, esplorare e sperimentare. La scienza è un'avventura continua, e l'atomo è solo l'inizio!

Ricordate: anche gli scienziati più brillanti hanno iniziato con domande semplici. Continuate a curiosare, a imparare e a scoprire. Il mondo dell'atomo è affascinante e pieno di sorprese!
Un consiglio pratico: Se vi sentite sopraffatti, fate un passo indietro. Dividete l'argomento in piccoli pezzi e concentratevi su uno alla volta. E non dimenticate di chiedere aiuto se ne avete bisogno! Insegnanti, tutor e amici sono lì per supportarvi nel vostro percorso di apprendimento.
Forza e coraggio! La scienza è alla portata di tutti, basta un po' di curiosità e impegno. E chissà, magari un giorno sarete voi a fare nuove scoperte nel mondo dell'atomo!