Da Un Acqua A Temperatura Elevata
Capita a tutti. Ci si siede davanti al compito di fisica, si legge la consegna, e si sente un brivido lungo la schiena. La domanda: "Calcola il calore necessario per portare un litro d'acqua da temperatura ambiente a temperatura di ebollizione" sembra un muro invalicabile. Non disperare! Respiro profondo, e affrontiamo insieme questo "mostro" che in realtà è molto più amichevole di quanto sembri.
Comprendere gli Ingredienti: Cosa Serve Sapere
Prima di tutto, scomponiamo il problema. Abbiamo bisogno di alcuni ingredienti fondamentali, come in una ricetta. Immagina di dover cucinare qualcosa di delizioso: senza gli ingredienti giusti, il risultato non sarà quello sperato!
Il Calore Specifico dell'Acqua: Un Valore Fondamentale
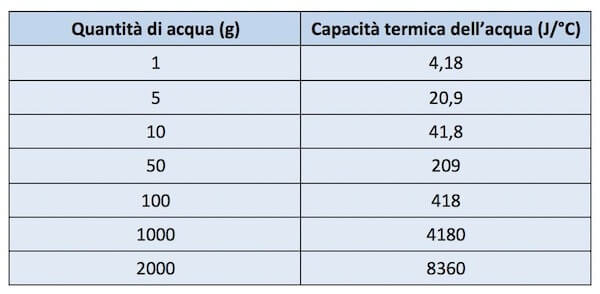
Il primo ingrediente è il calore specifico dell'acqua. Questo valore ci dice quanta energia (calore) serve per aumentare la temperatura di 1 grammo di acqua di 1 grado Celsius (o Kelvin, è la stessa cosa!). Il calore specifico dell'acqua è circa 4.186 J/g°C (Joule per grammo per grado Celsius). Ricordatelo, è un po' come il numero di telefono di un amico, utile da avere a portata di mano!
Must Read
La Massa dell'Acqua: Quanto Ce N'è
Il secondo ingrediente è la massa dell'acqua. Nel nostro caso, abbiamo un litro d'acqua. Dobbiamo trasformare questo volume in massa. Sappiamo che la densità dell'acqua è circa 1 kg/L (chilogrammo per litro). Quindi, un litro d'acqua pesa circa 1 kg, ovvero 1000 grammi. Perfetto! Abbiamo la massa.
La Variazione di Temperatura: Quanto Deve Scaldare
Il terzo ingrediente è la variazione di temperatura. Dobbiamo capire di quanto dobbiamo aumentare la temperatura dell'acqua. Supponiamo che la temperatura ambiente sia di 20°C e che l'acqua debba bollire a 100°C. La variazione di temperatura è quindi 100°C - 20°C = 80°C.
La Ricetta Magica: La Formula del Calore
Ora che abbiamo tutti gli ingredienti, possiamo usare la ricetta! La formula per calcolare il calore (Q) è molto semplice:
Q = m * c * ΔT
Dove:
- Q è il calore necessario (in Joule)
- m è la massa (in grammi)
- c è il calore specifico (in J/g°C)
- ΔT è la variazione di temperatura (in °C)
Mettiamoci all'Opera: Calcoliamo Insieme
Sostituiamo i valori che abbiamo trovato nella formula:

Q = 1000 g * 4.186 J/g°C * 80°C
Q = 334880 J

Quindi, per portare un litro d'acqua da 20°C a 100°C, sono necessari circa 334880 Joule di energia. Possiamo anche esprimere questo valore in Kilojoule (kJ) dividendo per 1000: 334.88 kJ. Ecco fatto!
Trucchi del Mestiere e Consigli Utili
Ecco alcuni trucchi per affrontare problemi simili con più sicurezza:
- Controlla sempre le unità di misura. Assicurati che siano coerenti (grammi, Celsius, Joule, ecc.). Se sono diverse, convertile prima di usare la formula.
- Fai degli esercizi! Più ti eserciti, più diventerai bravo. Prova a cambiare i valori (temperatura iniziale, volume dell'acqua) e ricalcola il calore necessario.
- Usa risorse online. Ci sono tantissimi siti web e video che spiegano questi concetti in modo ancora più dettagliato.
- Non aver paura di chiedere aiuto. Se hai difficoltà, chiedi aiuto al tuo insegnante, a un compagno di classe o a un tutor. Non c'è niente di male a chiedere!
Ricorda, la fisica è come un puzzle. All'inizio può sembrare difficile, ma con pazienza e metodo, ogni pezzo andrà al suo posto. Continua a sperimentare, a fare domande e a non arrenderti mai! La soddisfazione di risolvere un problema è impagabile.