Esercizi Sul Bilanciamento Delle Reazioni Chimiche
Ciao! Se sei qui, probabilmente stai lottando con il bilanciamento delle reazioni chimiche. Non preoccuparti, non sei solo! Molti studenti (e anche qualche genitore!) si sentono sopraffatti da questo argomento. Ma fidati di me, con la giusta guida e un po' di pratica, diventerà molto più semplice di quanto pensi.
Capisco la frustrazione. Vedere una serie di simboli e numeri che sembrano non avere un senso può scoraggiare. Ma pensa al bilanciamento delle reazioni chimiche come a un puzzle: ogni pezzo ha il suo posto, e una volta assemblato correttamente, l'immagine è completa e chiara.
Perché il Bilanciamento delle Reazioni Chimiche è Importante?
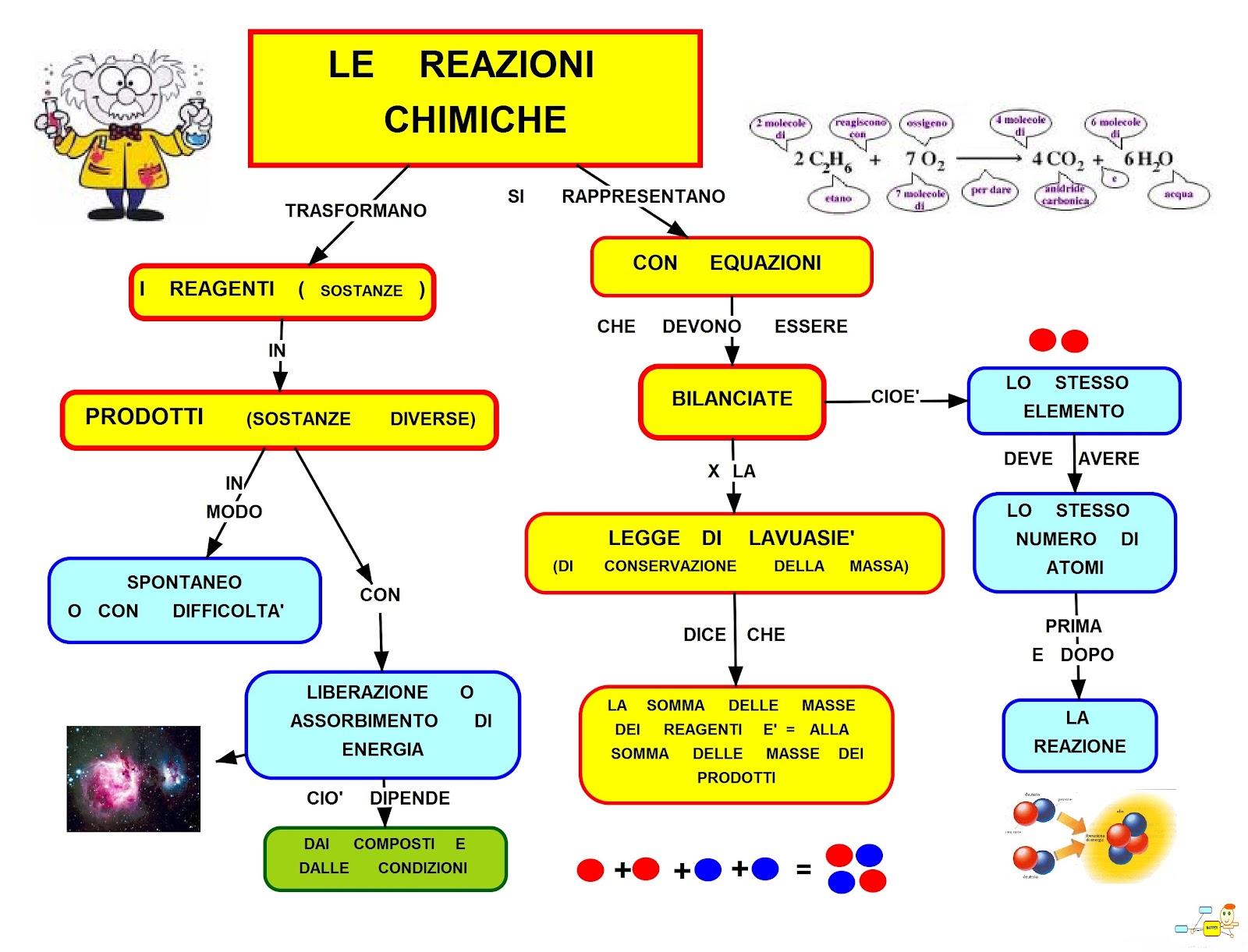
Ti starai chiedendo: "Perché devo imparare questa cosa?". Ottima domanda! Il bilanciamento delle reazioni chimiche è fondamentale perché riflette la Legge di Conservazione della Massa. Questa legge, una delle fondamenta della chimica, afferma che la materia non può essere creata né distrutta in una reazione chimica. In pratica, significa che il numero di atomi di ogni elemento deve essere lo stesso sia nei reagenti (le sostanze che reagiscono) che nei prodotti (le sostanze che si formano).
Must Read
Come ha detto una professoressa di chimica con cui ho parlato, la dottoressa Rossi: "Bilanciare le reazioni chimiche è come bilanciare un'equazione matematica. Se un lato non è uguale all'altro, l'equazione è sbagliata!".
Come Bilanciare le Reazioni Chimiche: Un Passo alla Volta
Ecco un metodo passo-passo che puoi utilizzare per bilanciare le reazioni chimiche. Cercheremo di renderlo il più semplice possibile.
Passo 1: Scrivere l'Equazione Sbilanciata
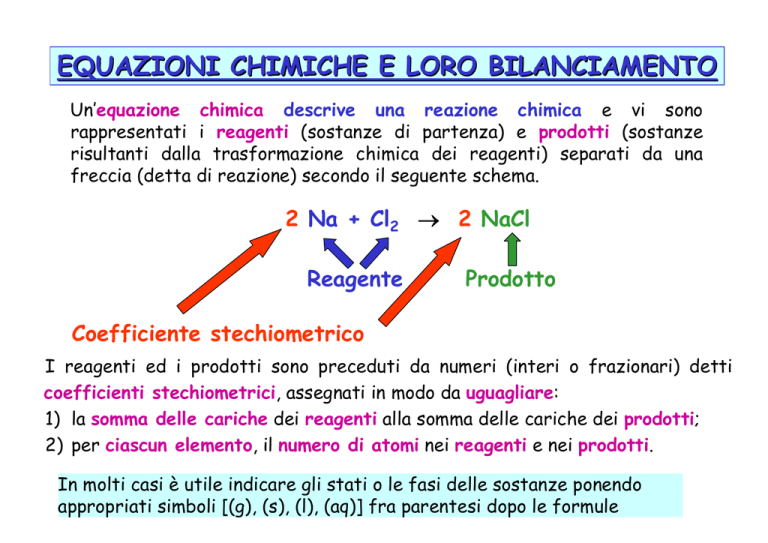
Per prima cosa, devi scrivere l'equazione chimica sbilanciata. Questo significa elencare tutti i reagenti e i prodotti, con le loro formule chimiche corrette. Ad esempio:
H2 + O2 → H2O

Questa equazione ci dice che l'idrogeno (H2) reagisce con l'ossigeno (O2) per formare l'acqua (H2O). Ma non è bilanciata!
Passo 2: Contare gli Atomi
Ora, conta il numero di atomi di ogni elemento presente sia nei reagenti che nei prodotti. Nell'esempio sopra:
- Reagenti: 2 atomi di idrogeno (H), 2 atomi di ossigeno (O)
- Prodotti: 2 atomi di idrogeno (H), 1 atomo di ossigeno (O)
Vediamo subito che l'ossigeno non è bilanciato: ci sono 2 atomi di ossigeno nei reagenti e solo 1 nei prodotti.
Passo 3: Aggiungere i Coefficienti
Per bilanciare l'equazione, aggiungiamo dei coefficienti davanti alle formule chimiche. Un coefficiente è un numero che moltiplica l'intera formula chimica. Non cambiare mai gli indici nelle formule! Cambiare gli indici altererebbe la sostanza chimica.
Nell'esempio, abbiamo bisogno di più ossigeno nei prodotti. Aggiungiamo un coefficiente "2" davanti all'H2O:

H2 + O2 → 2H2O
Ora abbiamo 2 atomi di ossigeno nei prodotti (2 x 1 = 2). Però, abbiamo anche cambiato il numero di atomi di idrogeno nei prodotti: ora ce ne sono 4 (2 x 2 = 4).
Passo 4: Continuare a Bilanciare
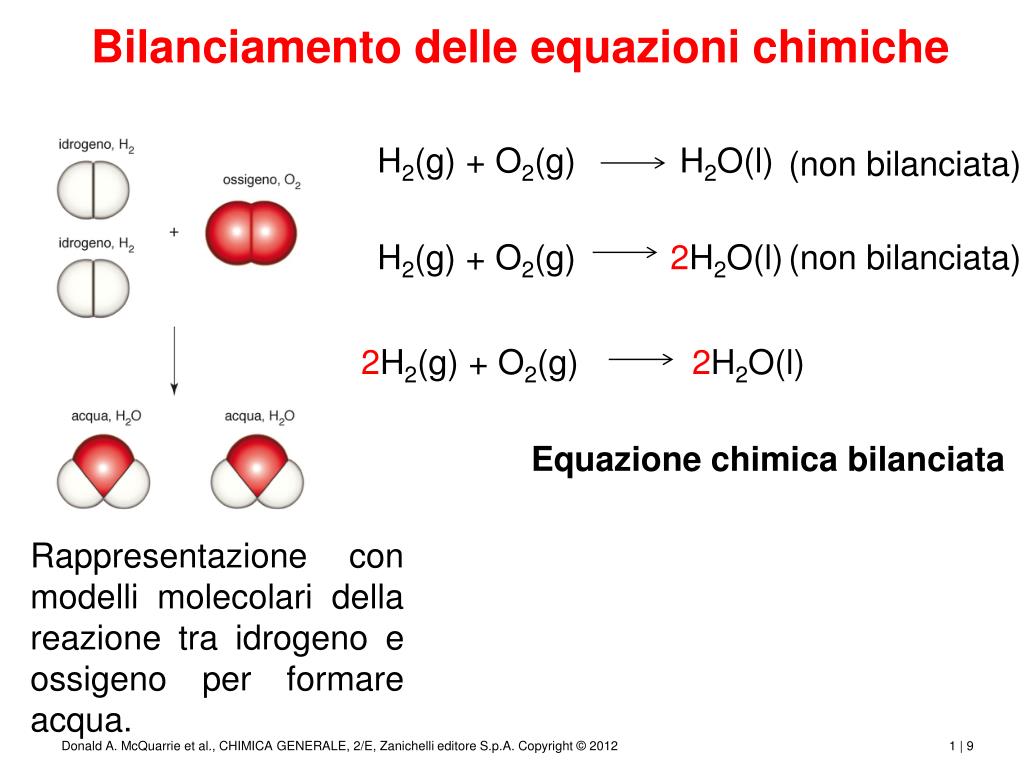
Dobbiamo bilanciare anche l'idrogeno. Aggiungiamo un coefficiente "2" davanti all'H2 nei reagenti:
2H2 + O2 → 2H2O

Ora, ricontrolliamo:
- Reagenti: 4 atomi di idrogeno (2 x 2 = 4), 2 atomi di ossigeno (O)
- Prodotti: 4 atomi di idrogeno (2 x 2 = 4), 2 atomi di ossigeno (2 x 1 = 2)
L'equazione è bilanciata!
Passo 5: Semplificare (Se Possibile)
In alcuni casi, i coefficienti possono essere semplificati. Ad esempio, se tutti i coefficienti sono numeri pari, puoi dividerli per 2 per ottenere i coefficienti più piccoli possibili. Nel nostro esempio, i coefficienti non possono essere semplificati ulteriormente.
Esercizi Pratici
Ecco alcuni esercizi per mettere in pratica quello che hai imparato. Non aver paura di sbagliare; l'importante è provare!
- Bilanciare l'equazione: N2 + H2 → NH3
- Bilanciare l'equazione: KClO3 → KCl + O2
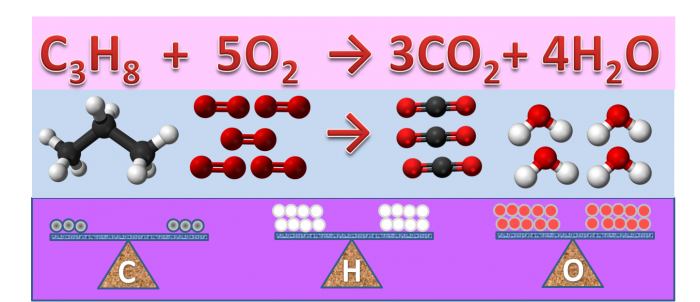
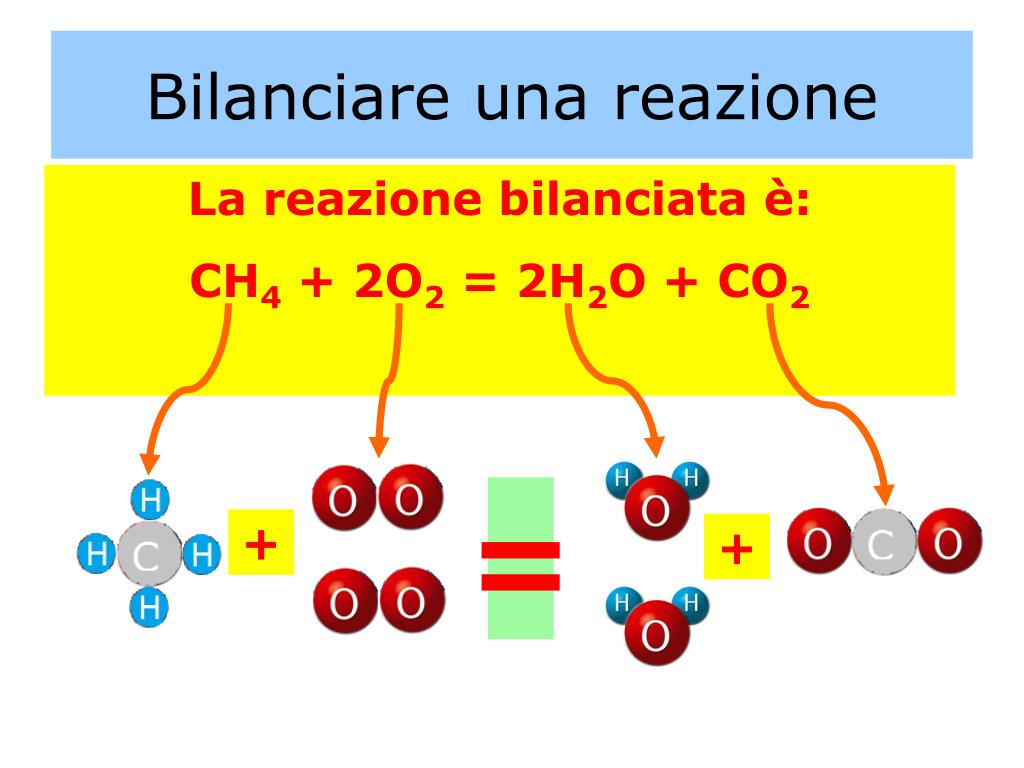
- Bilanciare l'equazione: CH4 + O2 → CO2 + H2O
Soluzioni:

- N2 + 3H2 → 2NH3
- 2KClO3 → 2KCl + 3O2
- CH4 + 2O2 → CO2 + 2H2O
Consigli Utili
- Inizia con gli elementi che compaiono solo una volta su ciascun lato dell'equazione. Questo semplifica il processo.
- Se vedi un gruppo poliatomico (come SO4), trattalo come un'unità. Questo può risparmiarti tempo.
- Se hai difficoltà, prova a usare una tabella per tenere traccia del numero di atomi. Questo può aiutarti a visualizzare il problema.
- Non aver paura di chiedere aiuto! Parla con il tuo insegnante, un tutor o un compagno di classe.
Applicazioni nella Vita Quotidiana
Potresti pensare che il bilanciamento delle reazioni chimiche sia qualcosa di astratto e irrilevante per la vita di tutti i giorni. Ma in realtà, la chimica è ovunque intorno a noi! Ad esempio, la combustione del gas in una stufa, la fotosintesi delle piante, la digestione del cibo nel tuo corpo – tutte queste sono reazioni chimiche che seguono le leggi del bilanciamento.
Capire come bilanciare le reazioni chimiche ti aiuta a comprendere meglio il mondo che ti circonda e a sviluppare un pensiero critico e analitico. Queste sono abilità preziose, non solo in chimica, ma in tutti gli aspetti della vita.
Risorse Utili
Oltre a questo articolo, ci sono molte altre risorse disponibili per aiutarti a imparare a bilanciare le reazioni chimiche:
- Video tutorial su YouTube: Cerca "bilanciamento reazioni chimiche" e troverai molti video che spiegano il processo passo-passo.
- Siti web interattivi: Alcuni siti web offrono esercizi interattivi che ti danno un feedback immediato.
- Libri di testo e quaderni di esercizi: Il tuo libro di testo di chimica è una risorsa preziosa. Cerca anche quaderni di esercizi con molti problemi da risolvere.
Un Ultimo Incoraggiamento
Ricorda, la pratica rende perfetti! Più ti eserciti, più facile diventerà il bilanciamento delle reazioni chimiche. Non arrenderti se all'inizio ti sembra difficile. Sii paziente, persevera, e presto sarai in grado di bilanciare le reazioni chimiche con facilità.
Credo in te! Affronta questa sfida con fiducia e determinazione. Buon divertimento con la chimica!