Numero Di Ossidazione Come Si Calcola

Quanti di voi, studenti, genitori alle prese con i compiti dei figli, o insegnanti in cerca di un modo efficace per spiegare concetti ostici, si sono trovati di fronte al numero di ossidazione e hanno pensato: "Da dove comincio?". Tranquilli, non siete soli! La chimica può sembrare un labirinto, ma con la giusta guida, anche il numero di ossidazione diventa un concetto accessibile e persino interessante.
In questo articolo, vi accompagnerò passo passo alla scoperta di come calcolare il numero di ossidazione, fornendo spiegazioni chiare, esempi pratici e strategie per affrontare gli esercizi senza paura. Dimenticate le formule complicate e i ragionamenti astrusi: puntiamo alla comprensione reale e all'applicazione pratica.
Cos'è il Numero di Ossidazione?
Immaginate il numero di ossidazione come un segnalibro che ci aiuta a tenere traccia degli elettroni in una molecola o in uno ione. Più precisamente, è una carica ipotetica che un atomo assumerebbe se tutti i legami che forma fossero ionici. È importante sottolineare che è una carica ipotetica, perché nella realtà molti legami sono covalenti, ovvero implicano la condivisione di elettroni, non il loro completo trasferimento.
Must Read
Perché è importante? Il numero di ossidazione ci fornisce informazioni preziose sul comportamento di un elemento in una reazione chimica, in particolare se si ossida (perde elettroni) o si riduce (acquista elettroni). Questo è fondamentale per capire le reazioni redox, pilastri della chimica e fondamentali in molti processi biologici e industriali.
Regole Fondamentali per Calcolare il Numero di Ossidazione
Il calcolo del numero di ossidazione si basa su alcune regole fondamentali, che funzionano come una bussola per orientarci in questo mondo. Memorizzarle è cruciale, ma capirne la logica lo è ancora di più. Cercheremo di fare entrambe le cose.
Regola 1: Elementi allo Stato Elementare
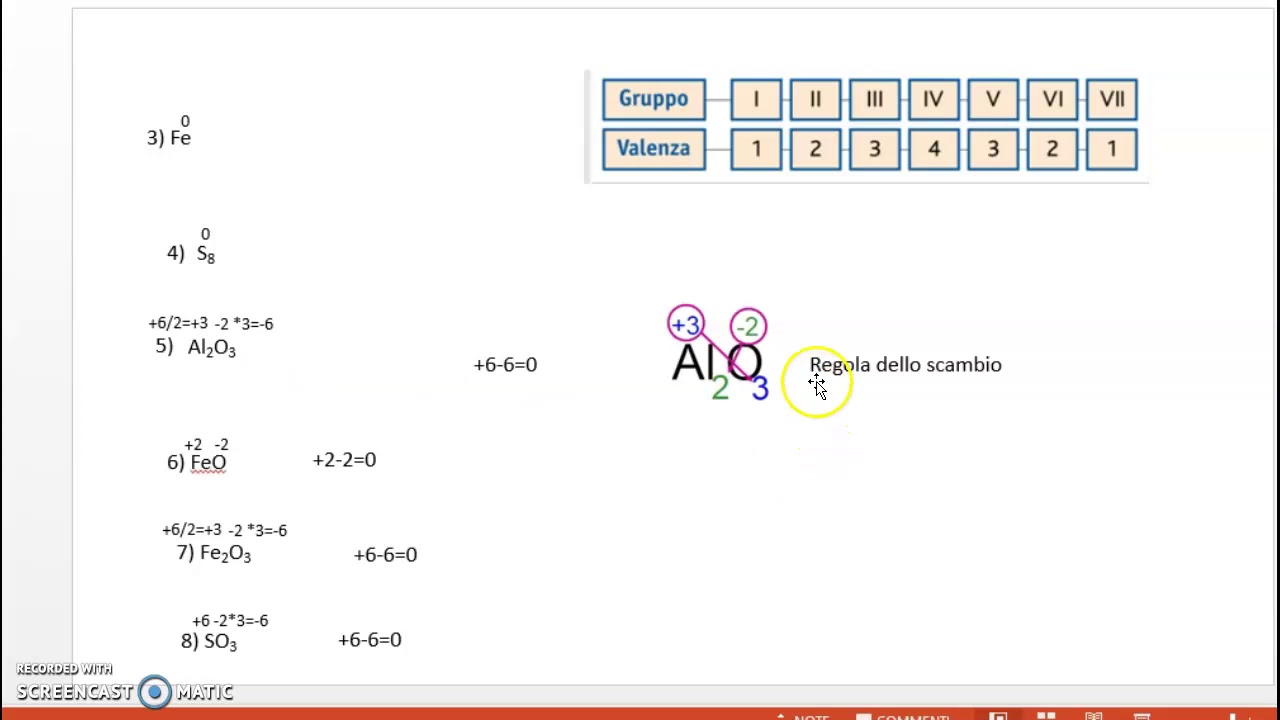
"L'oro è oro", potremmo dire. Un elemento allo stato elementare (ad esempio, Cu solido, O2 gassoso, N2 gassoso) ha sempre numero di ossidazione 0. Questo perché non ha né perso né acquistato elettroni.
Esempio pratico: In un filo di rame (Cu), il rame ha numero di ossidazione 0. Allo stesso modo, l'ossigeno molecolare (O2) che respiriamo ha numero di ossidazione 0.

Regola 2: Ioni Monoatomici
Un ione monoatomico ha numero di ossidazione uguale alla sua carica. Ad esempio, lo ione sodio (Na+) ha numero di ossidazione +1, mentre lo ione cloruro (Cl-) ha numero di ossidazione -1.
Esempio pratico: In una soluzione di cloruro di sodio (NaCl), lo ione sodio Na+ ha numero di ossidazione +1 e lo ione cloruro Cl- ha numero di ossidazione -1.
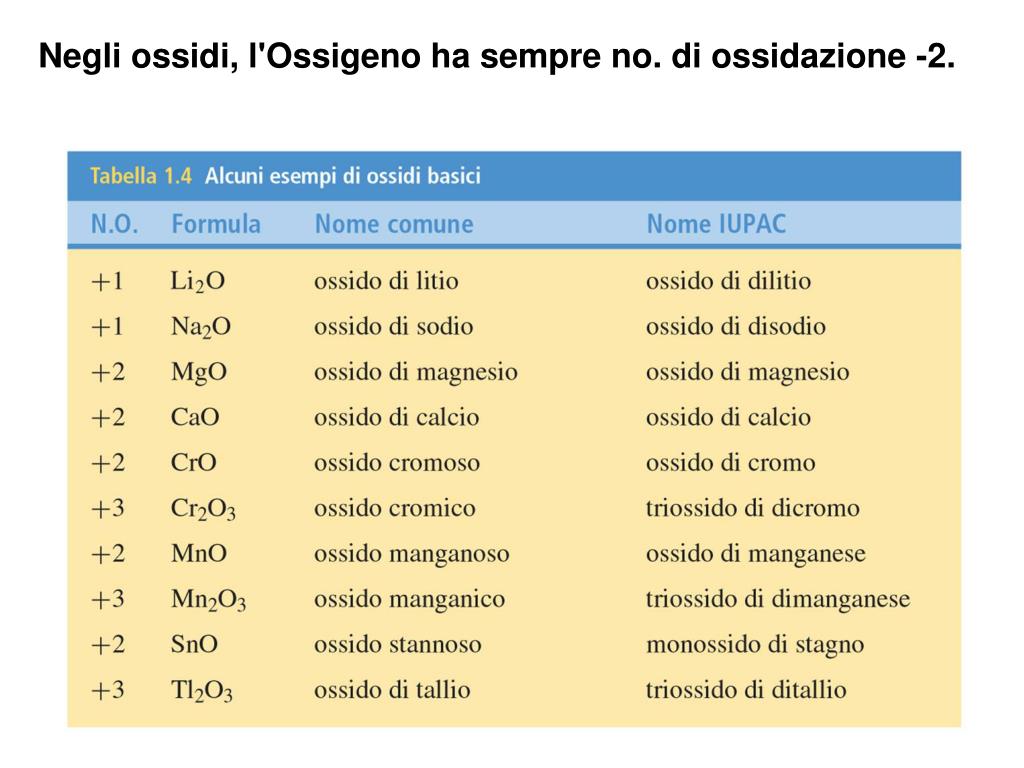
Regola 3: Ossigeno
Generalmente, l'ossigeno ha numero di ossidazione -2. Tuttavia, ci sono delle eccezioni importanti:
- Nei perossidi (come H2O2, acqua ossigenata), l'ossigeno ha numero di ossidazione -1.
- Quando è legato al fluoro (ad esempio, OF2), l'ossigeno ha numero di ossidazione positivo (in questo caso, +2). Questo perché il fluoro è l'elemento più elettronegativo.
Esempio pratico: Nell'acqua (H2O), l'ossigeno ha numero di ossidazione -2. Nell'acqua ossigenata (H2O2), ha numero di ossidazione -1.
Regola 4: Idrogeno
Generalmente, l'idrogeno ha numero di ossidazione +1. L'eccezione principale si verifica quando è legato a metalli, formando idruri metallici (ad esempio, NaH). In questo caso, l'idrogeno ha numero di ossidazione -1.

Esempio pratico: Nell'acido cloridrico (HCl), l'idrogeno ha numero di ossidazione +1. Nell'idruro di sodio (NaH), ha numero di ossidazione -1.
Regola 5: Fluoro
Il fluoro è l'elemento più elettronegativo e ha sempre numero di ossidazione -1 in tutti i suoi composti.
Regola 6: Metalli Alcalini (Gruppo 1)
I metalli alcalini (Li, Na, K, Rb, Cs) hanno sempre numero di ossidazione +1 nei loro composti.
Regola 7: Metalli Alcalino-Terrosi (Gruppo 2)
I metalli alcalino-terrosi (Be, Mg, Ca, Sr, Ba) hanno sempre numero di ossidazione +2 nei loro composti.

Regola 8: Somma dei Numeri di Ossidazione
La somma dei numeri di ossidazione di tutti gli atomi in una molecola neutra deve essere 0. La somma dei numeri di ossidazione di tutti gli atomi in uno ione poliatomico deve essere uguale alla carica dello ione.
Esempio pratico: Nell'acqua (H2O), abbiamo due atomi di idrogeno (ciascuno con numero di ossidazione +1) e un atomo di ossigeno (con numero di ossidazione -2). La somma è (2 * +1) + (-2) = 0.
Esempi Pratici di Calcolo del Numero di Ossidazione
Ora che abbiamo visto le regole, mettiamole in pratica con alcuni esempi.
Esempio 1: KClO3 (Clorato di Potassio)
- Sappiamo che K (potassio) è un metallo alcalino, quindi ha numero di ossidazione +1.
- Sappiamo che O (ossigeno) ha numero di ossidazione -2.
- Indichiamo con x il numero di ossidazione del Cl (cloro), che è l'elemento che vogliamo determinare.
- Applichiamo la regola 8: (+1) + x + (3 * -2) = 0
- Risolviamo l'equazione: 1 + x - 6 = 0 => x = +5
Quindi, il cloro nel KClO3 ha numero di ossidazione +5.
Esempio 2: SO42- (Ione Solfato)
- Sappiamo che O (ossigeno) ha numero di ossidazione -2.
- Indichiamo con x il numero di ossidazione del S (zolfo).
- Applichiamo la regola 8: x + (4 * -2) = -2 (ricordate, la somma deve essere uguale alla carica dello ione)
- Risolviamo l'equazione: x - 8 = -2 => x = +6
Quindi, lo zolfo nello ione solfato ha numero di ossidazione +6.

Esempio 3: Cr2O72- (Ione Dicromato)
- Sappiamo che O (ossigeno) ha numero di ossidazione -2.
- Indichiamo con x il numero di ossidazione del Cr (cromo).
- Applichiamo la regola 8: (2 * x) + (7 * -2) = -2
- Risolviamo l'equazione: 2x - 14 = -2 => 2x = 12 => x = +6
Quindi, il cromo nello ione dicromato ha numero di ossidazione +6.
Consigli e Strategie per Risolvere gli Esercizi
- Memorizzate le regole fondamentali. Sono la base di tutto.
- Identificate gli elementi con numero di ossidazione noto. Partite da quelli per semplificare il problema.
- Applicate la regola della somma. Impostate l'equazione e risolvetela per trovare l'incognita.
- Esercitatevi! Più esercizi fate, più diventerete bravi e veloci.
- Non abbiate paura di chiedere aiuto. Se vi bloccate, chiedete al vostro insegnante, a un compagno di classe o cercate online.
Errori Comuni da Evitare
- Confondere il numero di ossidazione con la carica ionica. Sono concetti correlati, ma non identici. Il numero di ossidazione è una carica ipotetica, mentre la carica ionica è una carica reale.
- Dimenticare le eccezioni alle regole. Ricordate i perossidi, gli idruri metallici e i composti con il fluoro.
- Non considerare la carica dello ione. Quando calcolate il numero di ossidazione in uno ione poliatomico, assicuratevi che la somma dei numeri di ossidazione sia uguale alla carica dello ione.
- Non semplificare le equazioni. Controllate sempre se i numeri di ossidazione calcolati sono ragionevoli nel contesto della molecola o dello ione.
Il Numero di Ossidazione nella Vita di Tutti i Giorni
Anche se può sembrare un concetto astratto, il numero di ossidazione è fondamentale in molti processi che avvengono intorno a noi. Ad esempio:
- La corrosione dei metalli: La ruggine è un processo di ossidazione del ferro, in cui il ferro perde elettroni e si trasforma in ossido di ferro.
- La combustione: Bruciare un combustibile (come il legno o il metano) è una reazione di ossidazione, in cui il combustibile reagisce con l'ossigeno.
- La respirazione cellulare: Le nostre cellule utilizzano l'ossigeno per ossidare il glucosio, producendo energia.
- Le batterie: Le batterie sfruttano reazioni redox per generare corrente elettrica.
Capire il numero di ossidazione ci permette quindi di comprendere meglio il mondo che ci circonda.
Conclusione
Spero che questo articolo vi abbia fornito una guida chiara e completa su come calcolare il numero di ossidazione. Ricordate che la pratica è fondamentale per padroneggiare questo concetto. Non scoraggiatevi se all'inizio incontrate delle difficoltà. Con un po' di impegno e la giusta guida, diventerete esperti nel calcolo del numero di ossidazione.
E ora, mettetevi alla prova con gli esercizi! Buon lavoro!