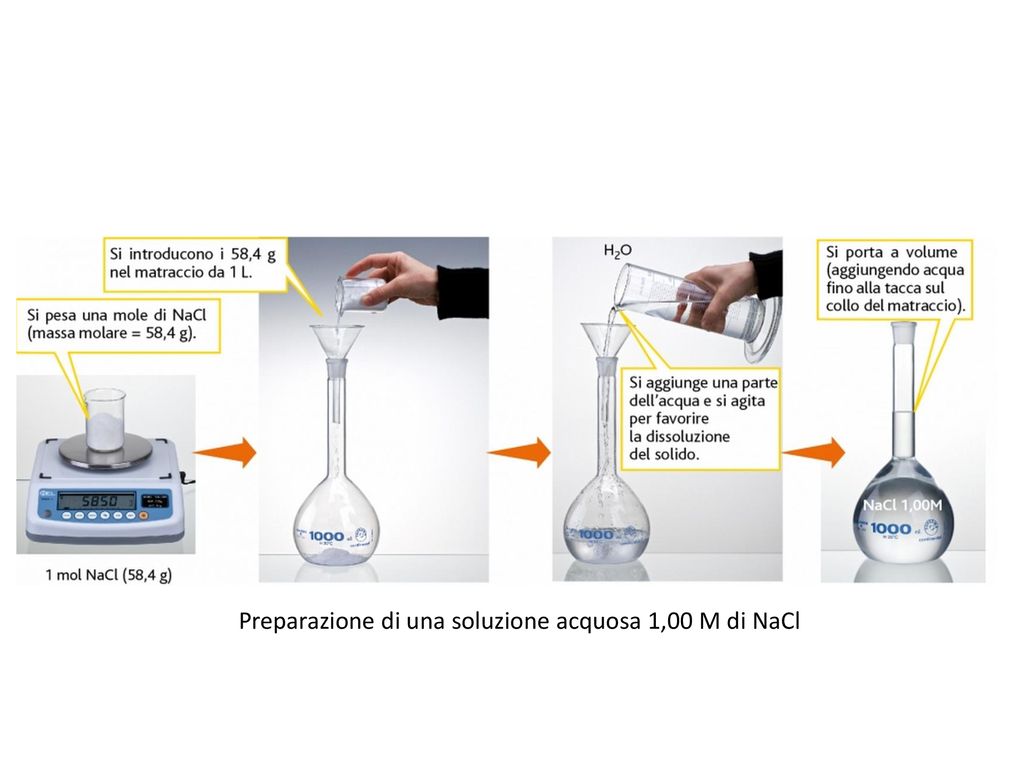
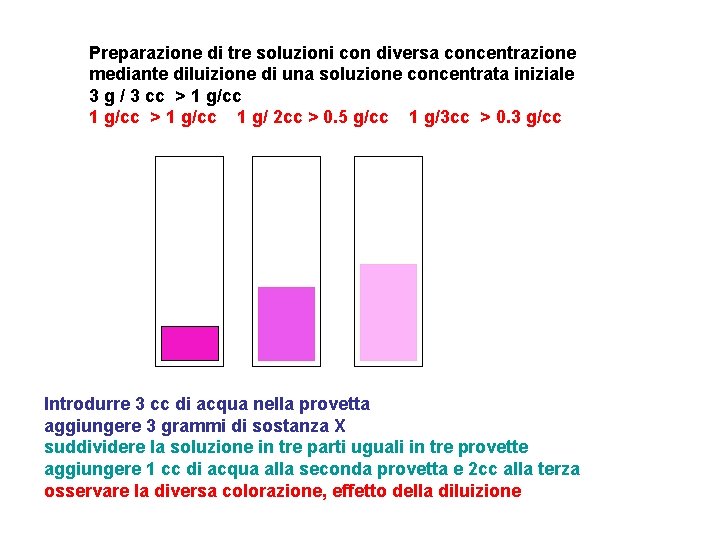
Preparazione Di Una Soluzione A Concentrazione Nota

Ti sei mai trovato a dover preparare una soluzione chimica precisa e ti sei sentito sopraffatto dalla complessità del processo? Non sei solo. Molti, sia studenti che professionisti, si trovano di fronte a questa sfida. L'accuratezza nella preparazione di una soluzione a concentrazione nota è fondamentale in moltissime applicazioni, dalla ricerca scientifica all'industria farmaceutica, dall'analisi ambientale al controllo qualità. Un piccolo errore può portare a risultati completamente sbagliati e costosi!
Perché è così Importante una Concentrazione Precisa?
Immagina di dover dosare un farmaco. Una concentrazione errata potrebbe renderlo inefficace o, peggio ancora, tossico. Secondo uno studio pubblicato sul Journal of Pharmaceutical Sciences, circa il 30% degli errori nei laboratori farmaceutici sono legati a imprecisioni nella preparazione delle soluzioni. Questo dato sottolinea l'importanza cruciale di seguire procedure accurate e standardizzate. La precisione non è solo una questione di correttezza scientifica, ma anche di sicurezza e affidabilità dei risultati.
Un altro esempio pratico lo troviamo nell'analisi ambientale. Per determinare la concentrazione di un inquinante in un campione d'acqua, è necessario utilizzare soluzioni standard con concentrazioni note. Se queste soluzioni standard sono preparate in modo impreciso, i risultati dell'analisi saranno inaffidabili, portando a valutazioni errate del rischio ambientale e, potenzialmente, a decisioni politiche inadeguate. Come afferma la EPA (Environmental Protection Agency), "La qualità dei dati ambientali dipende direttamente dalla qualità delle soluzioni utilizzate."
Must Read
Passo Dopo Passo: Come Preparare una Soluzione a Concentrazione Nota
Ecco una guida pratica e dettagliata per preparare una soluzione a concentrazione nota in modo corretto e sicuro:
1. Calcolare la Massa Necessaria
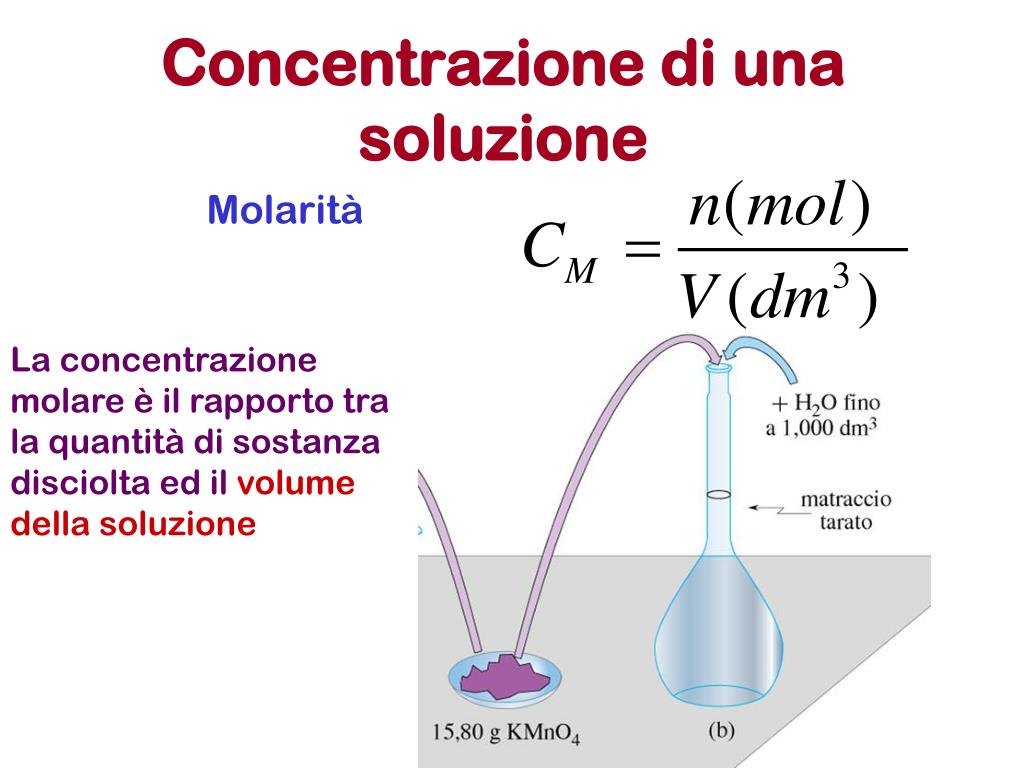
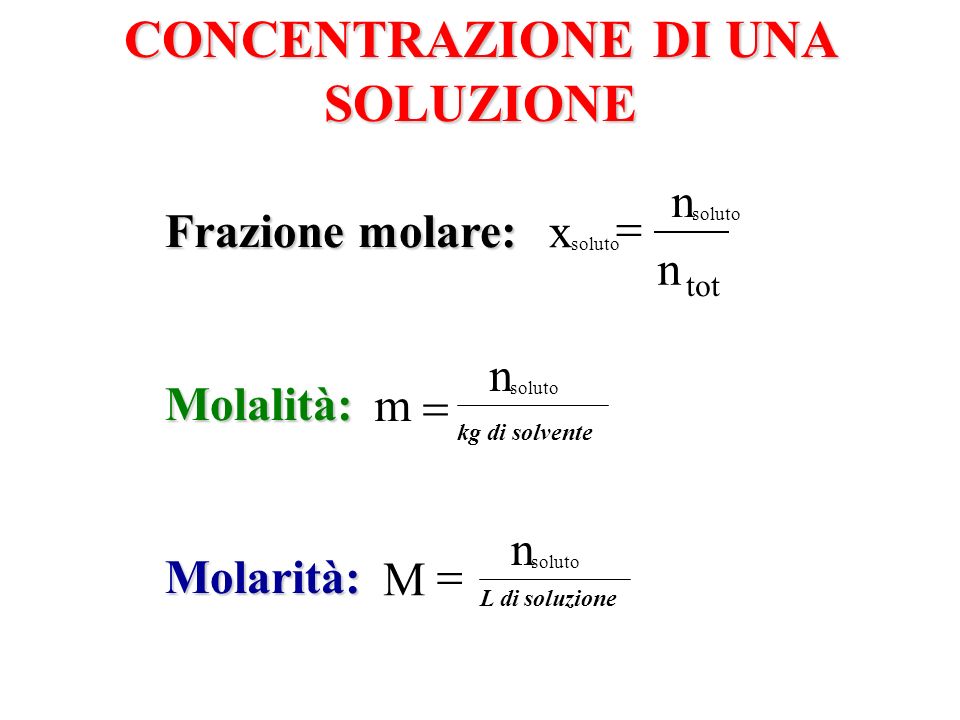
Il primo passo, e forse il più critico, è calcolare la massa di soluto necessaria per ottenere la concentrazione desiderata. Questo calcolo dipende dal tipo di concentrazione che si vuole ottenere (molarità, normalità, percentuale in peso/volume, ecc.). Molarità (M), definita come moli di soluto per litro di soluzione, è una delle unità di concentrazione più comuni. La formula fondamentale è:
M = moli di soluto / litri di soluzione
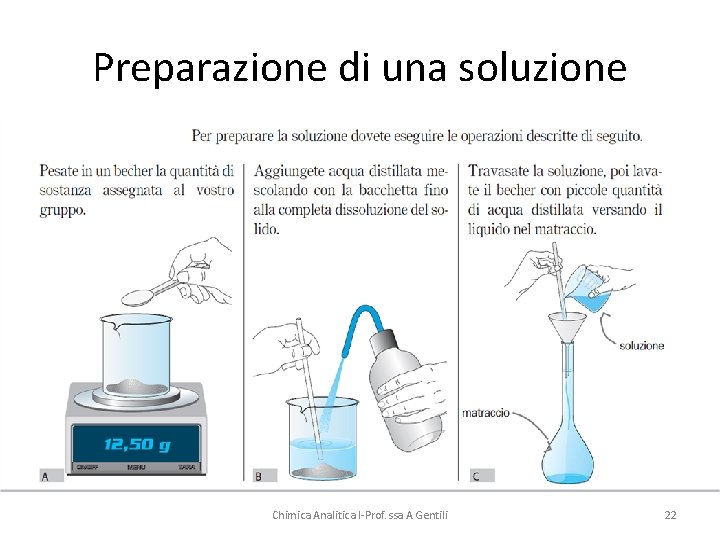
Quindi, per preparare una soluzione di molarità nota, è necessario:
- Definire la molarità desiderata (M).
- Definire il volume finale della soluzione (V, in litri).
- Calcolare le moli di soluto necessarie: moli = M x V.
- Calcolare la massa di soluto necessaria: massa (g) = moli x peso molecolare (g/mol).
Esempio: Vogliamo preparare 500 mL (0.5 L) di una soluzione di NaCl 0.1 M. Il peso molecolare di NaCl è circa 58.44 g/mol. Quindi:
moli di NaCl = 0.1 M x 0.5 L = 0.05 moli
massa di NaCl = 0.05 moli x 58.44 g/mol = 2.922 g

Dovremo quindi pesare 2.922 g di NaCl per preparare la nostra soluzione.
2. Pesare il Soluto con Precisione
Una volta calcolata la massa necessaria, è fondamentale pesare il soluto con la massima precisione possibile. Utilizza una bilancia analitica calibrata e pulita. Assicurati che la bilancia sia stabile e che non ci siano correnti d'aria che possano influenzare la misurazione. Utilizza una spatola pulita per trasferire il soluto dal contenitore originale al contenitore di pesata. Evita di contaminare il soluto o il contenitore di pesata. Registra con cura il peso esatto misurato.
Suggerimento pratico: Utilizza la tecnica della "pesata per differenza". Pesare un contenitore (es. becher) vuoto, poi aggiungere il soluto e pesare di nuovo. La differenza tra le due pesate rappresenta la massa del soluto.

3. Dissolvere il Soluto
Trasferisci con cura il soluto pesato in un matraccio tarato (o beuta tarata) di volume appropriato. Aggiungi una quantità di solvente (solitamente acqua distillata o deionizzata) inferiore al volume finale desiderato. Agita delicatamente la soluzione per favorire la dissoluzione completa del soluto. Se necessario, utilizza un agitatore magnetico per accelerare il processo. Assicurati che tutto il soluto si sia dissolto prima di procedere al passo successivo. Alcuni soluti possono richiedere riscaldamento per dissolversi completamente, ma assicurati che la soluzione si raffreddi a temperatura ambiente prima di portare a volume.
4. Portare a Volume
Dopo che il soluto si è completamente dissolto, aggiungi lentamente il solvente fino a raggiungere il segno di taratura del matraccio. L'occhio deve essere all'altezza del segno di taratura per evitare errori di parallasse. Utilizza una pipetta Pasteur o un contagocce per aggiungere le ultime gocce di solvente con precisione. Una volta raggiunto il segno di taratura, capovolgi il matraccio diverse volte per assicurarti che la soluzione sia omogenea. Questo è un passo cruciale per garantire una concentrazione uniforme in tutta la soluzione.
Importante: Il menisco del liquido (la superficie curva) deve toccare il segno di taratura. Per soluzioni acquose, il fondo del menisco deve essere allineato al segno.
5. Etichettare e Conservare Correttamente
Una volta preparata la soluzione, è essenziale etichettarla correttamente con le seguenti informazioni:

- Nome del soluto
- Concentrazione
- Data di preparazione
- Nome del preparatore
- Eventuali precauzioni di sicurezza
Conservare la soluzione in un contenitore appropriato, al riparo dalla luce e da temperature estreme. La durata di conservazione di una soluzione dipende dal tipo di soluto e dalle condizioni di conservazione. Alcune soluzioni possono degradarsi nel tempo, quindi è importante controllare la loro stabilità prima dell'uso. È buona norma preparare soluzioni fresche quando possibile, soprattutto se si richiedono alti livelli di accuratezza.
Errori Comuni da Evitare
Anche seguendo scrupolosamente i passaggi descritti, è possibile commettere errori che possono compromettere l'accuratezza della soluzione. Ecco alcuni errori comuni da evitare:
- Utilizzare vetreria non calibrata: Utilizzare solo vetreria tarata (matracci, pipette, burette) per preparare soluzioni a concentrazione nota.
- Pesare il soluto in modo impreciso: Utilizzare una bilancia analitica calibrata e pesare il soluto con la massima precisione.
- Non dissolvere completamente il soluto: Assicurarsi che il soluto si sia completamente dissolto prima di portare a volume.
- Portare a volume a temperatura diversa da quella di calibrazione del matraccio: I matracci tarati sono calibrati a una specifica temperatura (solitamente 20°C). Portare a volume a una temperatura diversa può introdurre errori.
- Contaminare la soluzione: Utilizzare solo vetreria pulita e solventi di elevata purezza.
Conclusione
Preparare una soluzione a concentrazione nota può sembrare complesso, ma seguendo attentamente i passaggi descritti e prestando attenzione ai dettagli, è possibile ottenere risultati accurati e affidabili. La chiave è la precisione, la cura e la comprensione dei principi chimici alla base del processo. Ricorda sempre che la qualità dei tuoi risultati dipende direttamente dalla qualità delle tue soluzioni!
Non scoraggiarti se i primi tentativi non sono perfetti. La pratica rende perfetti. Con l'esperienza, acquisirai familiarità con le tecniche e sarai in grado di preparare soluzioni a concentrazione nota con facilità e sicurezza. Buona preparazione!






.jpg)