Quanti Elettroni Possono Essere Contenuti Al Massimo In Un Orbitale
Ciao! Studiare la chimica, e in particolare la struttura atomica, può sembrare complicato all'inizio. Molti studenti si trovano spaesati di fronte a concetti come gli orbitali e la loro capacità di contenere elettroni. Non preoccuparti, è perfettamente normale! L'importante è affrontare l'argomento con metodo e chiarezza. Cercheremo di rendere tutto più semplice e comprensibile.
Comprendere gli Orbitali Atomici: Un'Introduzione
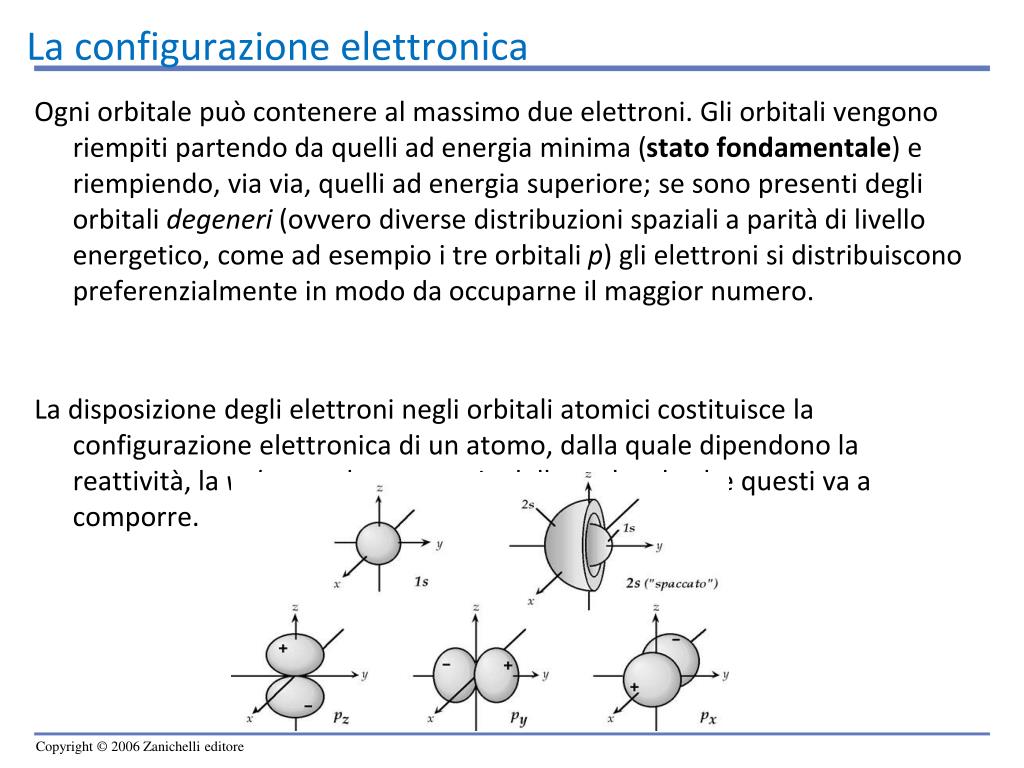
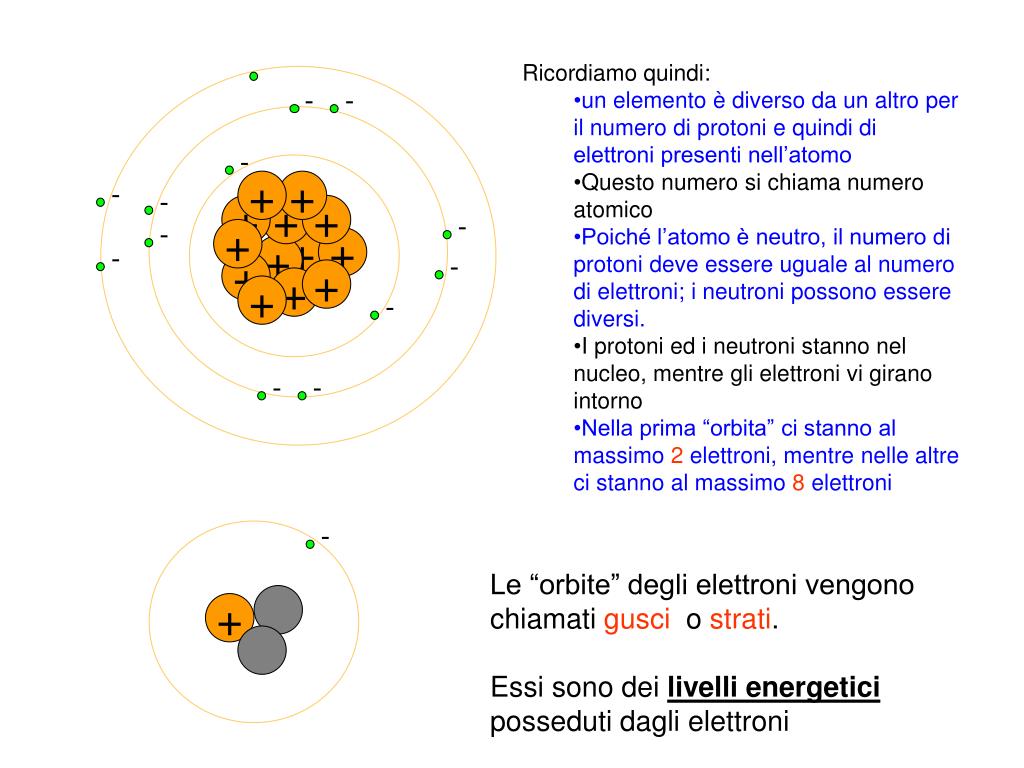
Innanzitutto, chiariamo cosa intendiamo con il termine "orbitale atomico". Immagina un atomo come una piccola galassia, con un nucleo centrale (come il sole) attorno al quale ruotano gli elettroni (come i pianeti). A differenza dei pianeti che seguono orbite definite, gli elettroni si trovano in regioni di spazio attorno al nucleo dove è più probabile trovarli. Queste regioni di spazio sono chiamate orbitali.
È importante sottolineare che un orbitale non è un percorso fisso che l'elettrone segue. Piuttosto, è una descrizione probabilistica della posizione dell'elettrone. Pensa a un ventilatore acceso: vedi le pale come una sfocatura, non come singole pale in posizioni precise. L'orbitale è simile: descrive dove è più probabile trovare l'elettrone in un dato momento.
Must Read
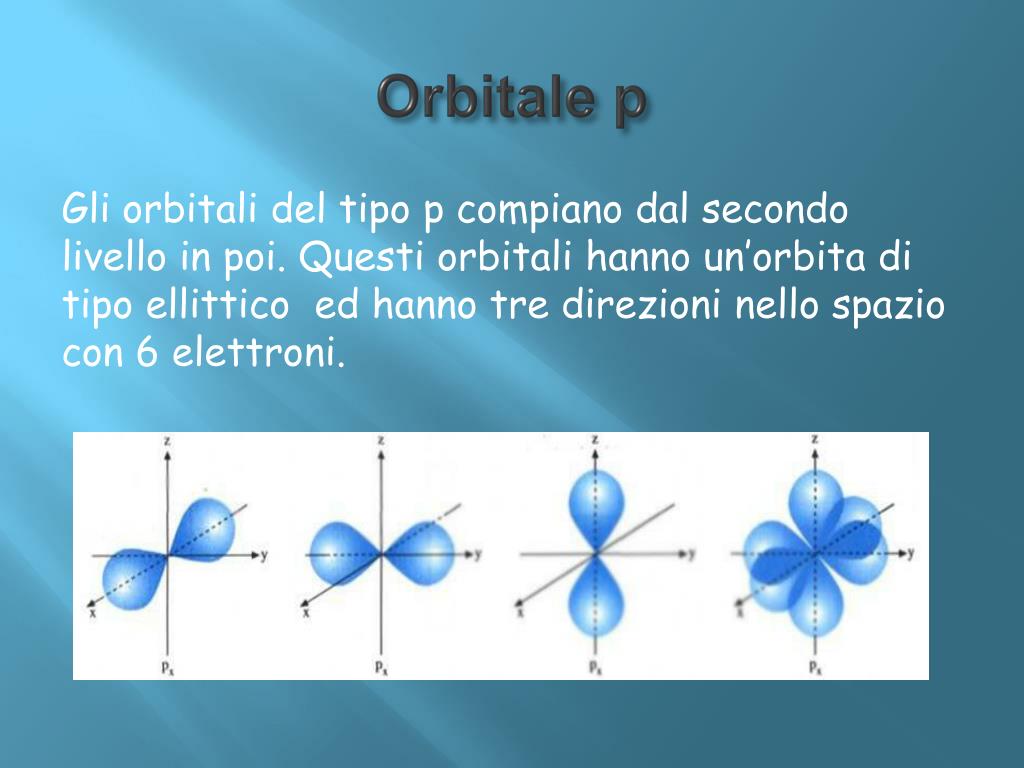
Esistono diversi tipi di orbitali, classificati in base alla loro forma e livello energetico. I principali sono gli orbitali s, p, d e f. Ognuno di questi ha una forma caratteristica: gli orbitali s sono sferici, gli orbitali p hanno una forma a "manubrio" (o a otto), e gli orbitali d e f hanno forme più complesse.
Il Principio di Esclusione di Pauli: La Chiave per Rispondere alla Domanda
Ora veniamo alla domanda principale: quanti elettroni possono essere contenuti al massimo in un orbitale? La risposta è dettata da un principio fondamentale della meccanica quantistica: il Principio di Esclusione di Pauli. Questo principio, formulato dal fisico Wolfgang Pauli, afferma che due elettroni in un atomo non possono avere tutti e quattro i numeri quantici uguali.
Cosa sono i numeri quantici? Sono un insieme di quattro numeri che descrivono lo stato di un elettrone in un atomo:
- Numero quantico principale (n): determina il livello energetico dell'elettrone (es. n=1, n=2, n=3, ...). Corrisponde al guscio elettronico (K, L, M, ecc.)
- Numero quantico angolare o azimutale (l): determina la forma dell'orbitale (es. l=0 per orbitale s, l=1 per orbitale p, l=2 per orbitale d, ...).
- Numero quantico magnetico (ml): determina l'orientamento spaziale dell'orbitale (es. per l=1 (orbitale p), ml può assumere i valori -1, 0, +1, che corrispondono ai tre orbitali p diretti lungo gli assi x, y e z).
- Numero quantico di spin (ms): descrive il momento angolare intrinseco dell'elettrone, chiamato spin. L'elettrone si comporta come se stesse ruotando, creando un campo magnetico. Lo spin può avere solo due valori: +1/2 (spin-up) e -1/2 (spin-down).
Il principio di esclusione di Pauli ci dice che se abbiamo un orbitale specifico (definito da n, l e ml), possiamo avere al massimo due elettroni al suo interno. Questi due elettroni avranno gli stessi valori di n, l e ml, ma dovranno avere valori diversi per il numero quantico di spin (uno con spin +1/2 e l'altro con spin -1/2). Si dice che abbiano spin opposti.
.+Un+elettrone+può+possedere+solo+due+valori+di+spin+(anche+lo+spin+è+quantizzato).+Gli+elettroni+negli+orbitali+vengono+rappresentati+con+delle+frecce+verticali+(che+rappresentano+il+vettore+spin)..jpg)
Conseguenze Pratiche: Orbitali e Sottolivelli
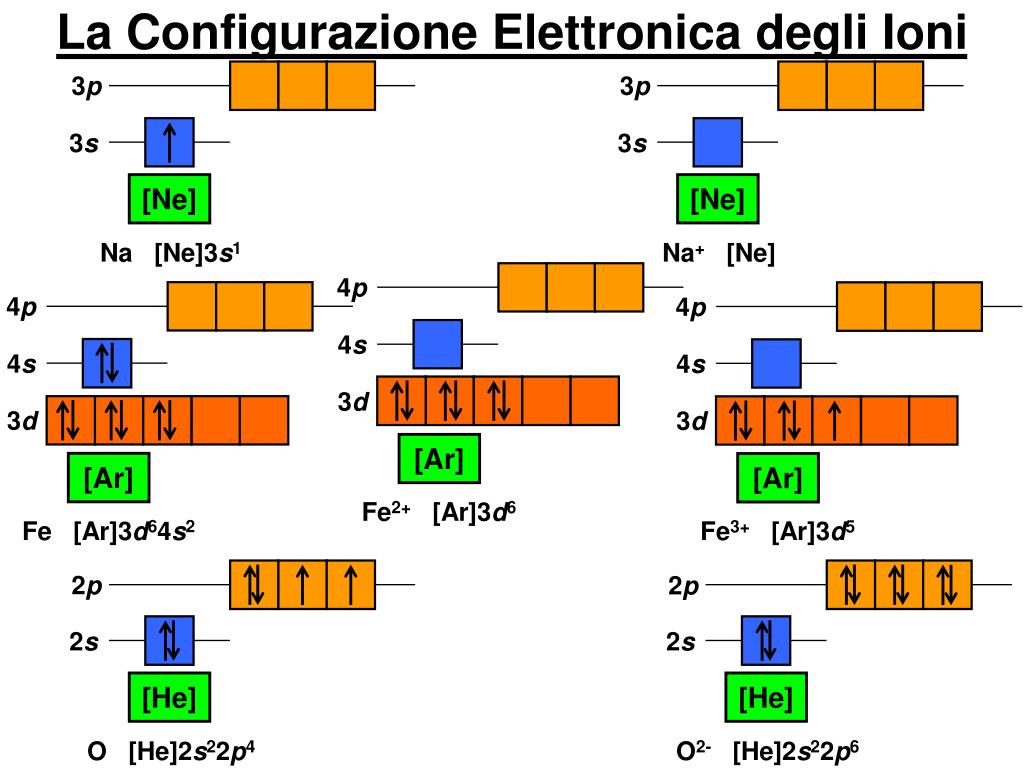
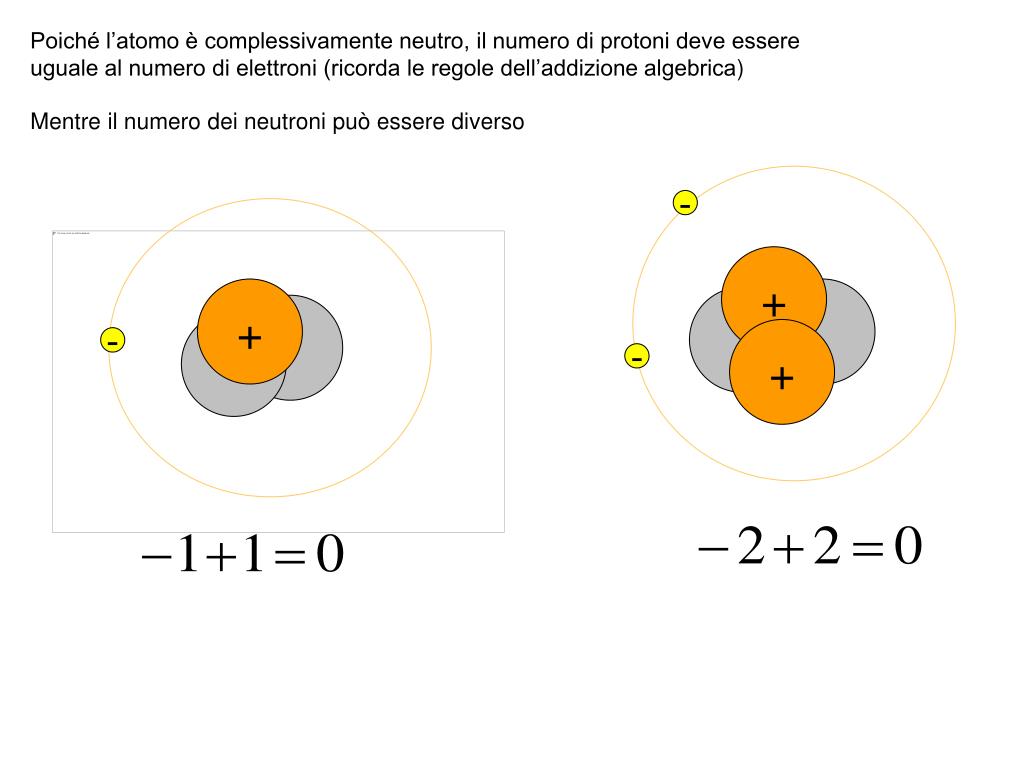
Quindi, la risposta alla nostra domanda è: un orbitale atomico può contenere al massimo due elettroni. Questo ha importanti conseguenze sulla configurazione elettronica degli atomi e sul numero di elettroni che possono essere presenti in ciascun sottolivello energetico.
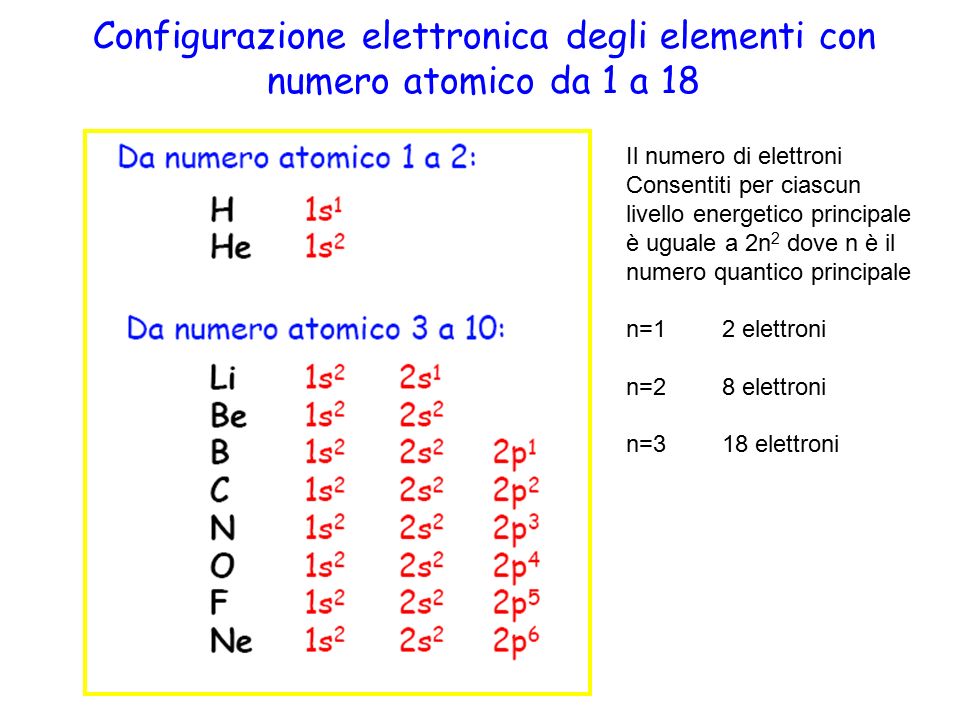
- Un orbitale s (l=0) è unico per ogni livello energetico e può contenere al massimo 2 elettroni.
- Un sottolivello p (l=1) è costituito da 3 orbitali p (px, py, pz), ognuno dei quali può contenere 2 elettroni, per un totale di 6 elettroni.
- Un sottolivello d (l=2) è costituito da 5 orbitali d, ognuno dei quali può contenere 2 elettroni, per un totale di 10 elettroni.
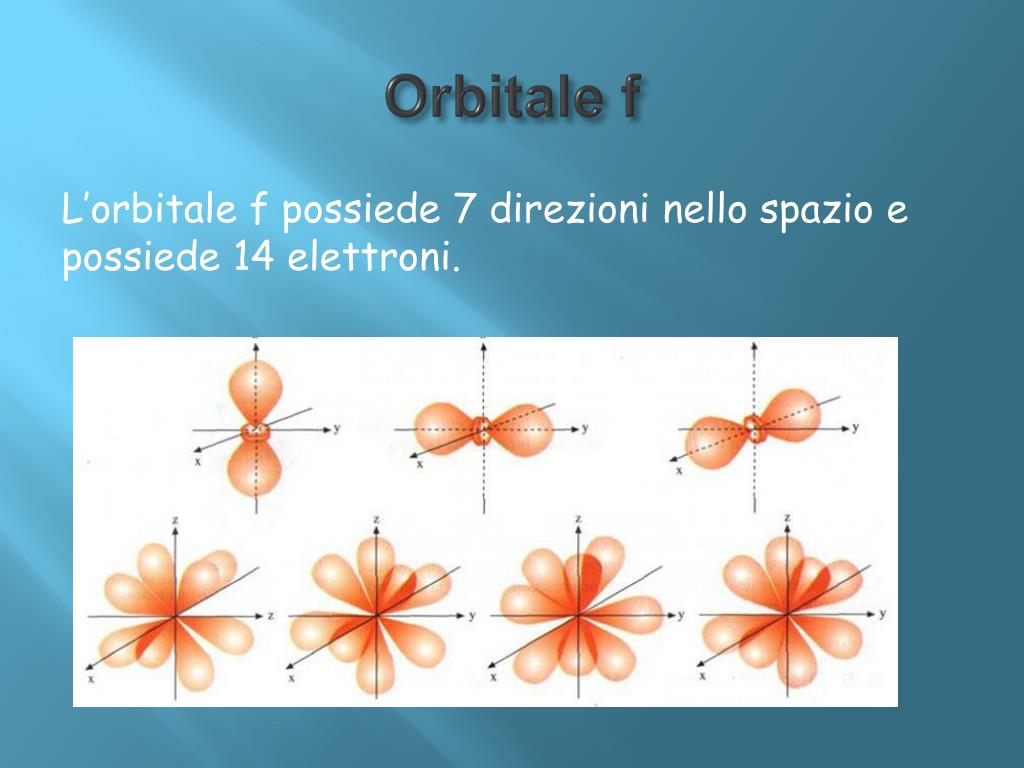
- Un sottolivello f (l=3) è costituito da 7 orbitali f, ognuno dei quali può contenere 2 elettroni, per un totale di 14 elettroni.
Consigli Pratici per l'Apprendimento
Capire quanti elettroni possono stare in un orbitale è fondamentale per comprendere la tavola periodica e le proprietà chimiche degli elementi. Ecco alcuni suggerimenti per facilitare l'apprendimento:
- Visualizzazione: Utilizza modelli 3D o simulazioni interattive per visualizzare la forma degli orbitali e come gli elettroni si dispongono nello spazio. Siti web come PhET Interactive Simulations (University of Colorado Boulder) offrono risorse gratuite e interattive.
- Esercizi: Fai pratica con esercizi di configurazione elettronica. Inizia con elementi semplici come l'idrogeno e l'elio, e poi passa a elementi più complessi.
- Analogia: Pensa agli orbitali come a delle stanze in un palazzo (l'atomo). Ogni stanza (orbitale) può ospitare solo due persone (elettroni). Il numero di stanze disponibili (orbitali in un sottolivello) dipende dal piano del palazzo (livello energetico).
- Collaboration: Studia con i tuoi compagni di classe. Spiegare i concetti ad altri aiuta a consolidare la tua comprensione.
Come Insegnare Efficacemente il Concetto di Orbitale
Se sei un insegnante, ecco alcune strategie per rendere più comprensibile il concetto di orbitale ai tuoi studenti:

- Introduzione graduale: Inizia spiegando il modello atomico di Bohr, per poi introdurre gradualmente il concetto di orbitale come una raffinazione del modello precedente.
- Analogia con sistemi familiari: Utilizza analogie che gli studenti possano capire, come quella del palazzo o quella del ventilatore che abbiamo già menzionato.
- Attività pratiche: Organizza attività pratiche come la costruzione di modelli di orbitali con materiali semplici come plastilina o palloncini.
- Tecnologia: Integra strumenti digitali come simulazioni e video esplicativi per rendere l'apprendimento più interattivo e coinvolgente.
- Valutazione formativa: Utilizza domande e quiz a risposta breve per verificare la comprensione degli studenti durante la lezione e per identificare eventuali difficoltà.
Superare le Difficoltà Comuni
Molti studenti trovano difficile accettare il concetto di probabilità associato agli orbitali. È importante sottolineare che la meccanica quantistica descrive il mondo a livello atomico in termini di probabilità, e che questa è una caratteristica fondamentale della natura.
Un'altra difficoltà comune è la comprensione dei numeri quantici. Spiega i numeri quantici uno alla volta, usando esempi concreti. Ad esempio, puoi spiegare il numero quantico principale come il numero di piani in un palazzo, e il numero quantico azimutale come il tipo di stanze presenti in ogni piano (stanze singole, doppie, ecc.).

Ricorda sempre che l'apprendimento richiede tempo e pazienza. Non scoraggiarti se non capisci tutto subito. Continua a studiare e a fare domande, e alla fine tutto diventerà più chiaro.
Conclusione: Un Passo alla Volta Verso la Padronanza
Comprendere quanti elettroni possono essere contenuti in un orbitale è un passo cruciale per padroneggiare la chimica. Attraverso una combinazione di concetti chiari, visualizzazioni efficaci e pratica costante, puoi superare le difficoltà e raggiungere i tuoi obiettivi. Ricorda, ogni grande scoperta inizia con un piccolo passo. Continua a esplorare, a imparare e a crescere!
Non aver paura di chiedere aiuto se ne hai bisogno. Ci sono molte risorse disponibili, come libri di testo, tutorial online e insegnanti qualificati, che possono supportarti nel tuo percorso di apprendimento. Credi in te stesso e nelle tue capacità, e sarai in grado di raggiungere il successo!








quindi+in+un+orbitale+ci+sono+:.jpg)