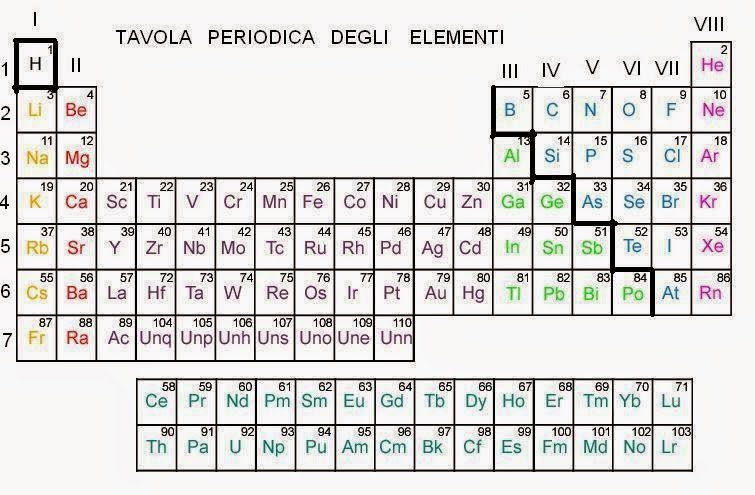
Quanti Gruppi Ci Sono Nella Tavola Periodica

Nella tavola periodica degli elementi, i gruppi rappresentano colonne verticali di elementi che condividono proprietà chimiche simili. Questi elementi presentano configurazioni elettroniche esterne analoghe, il che determina il loro comportamento chimico.
Struttura e Significato dei Gruppi
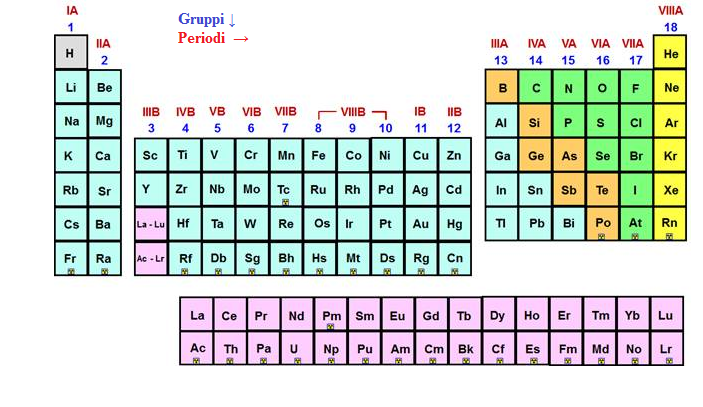
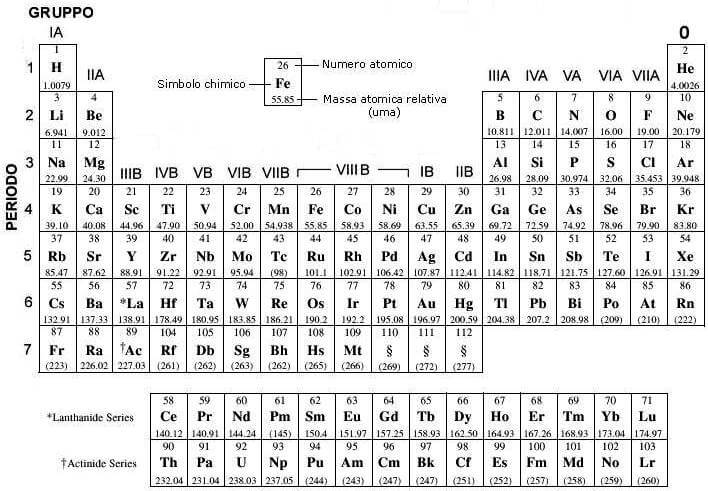
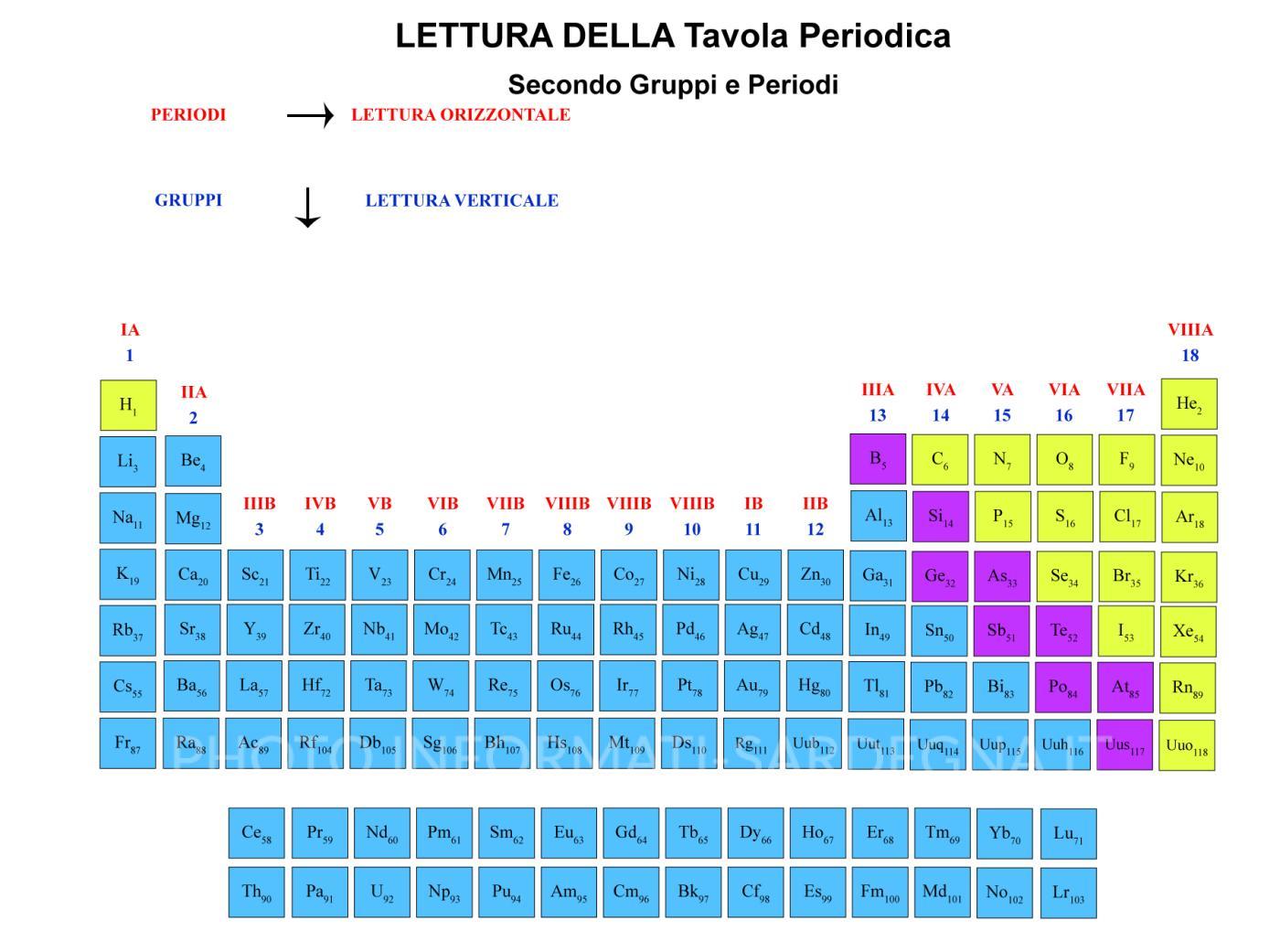
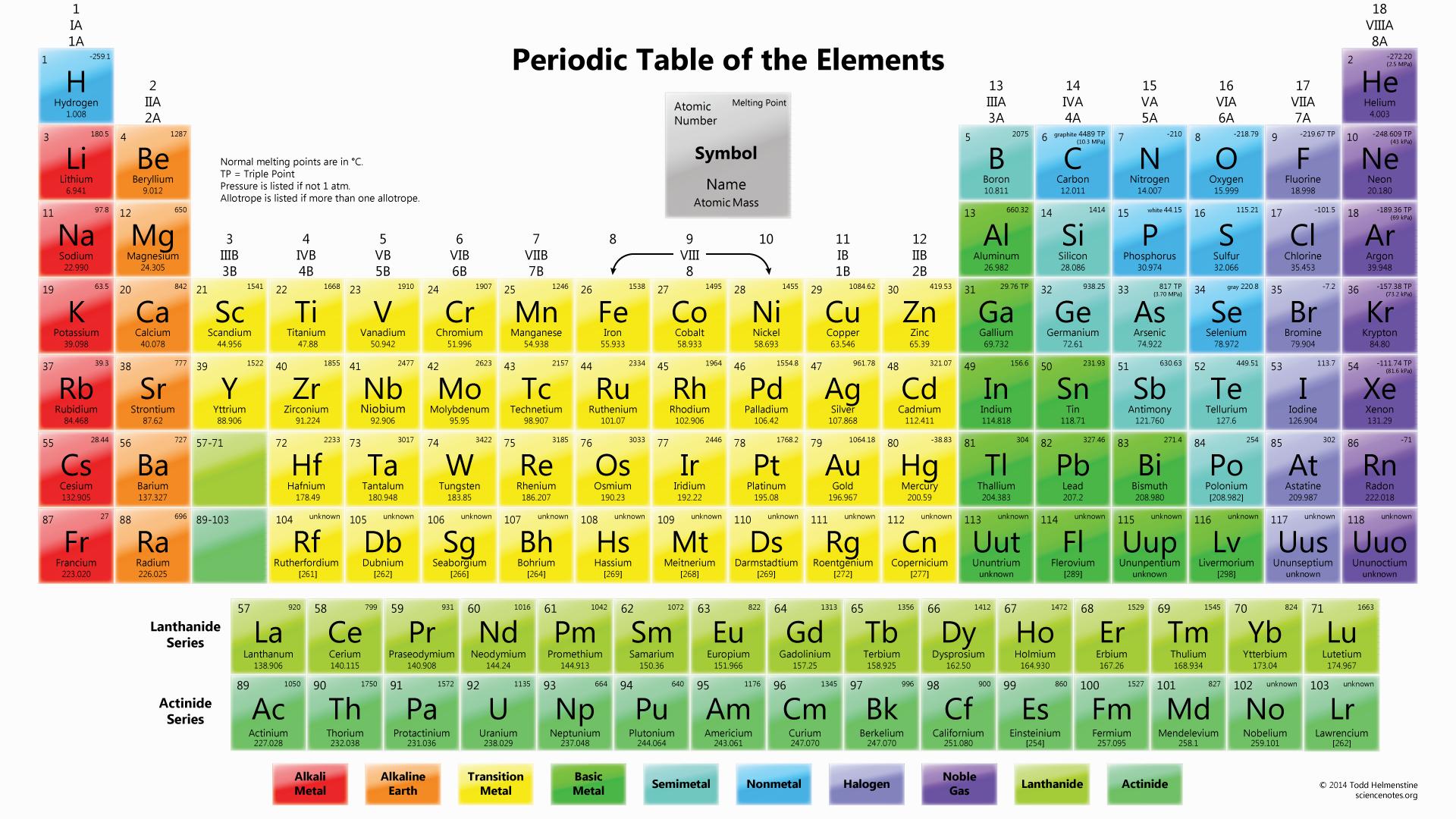
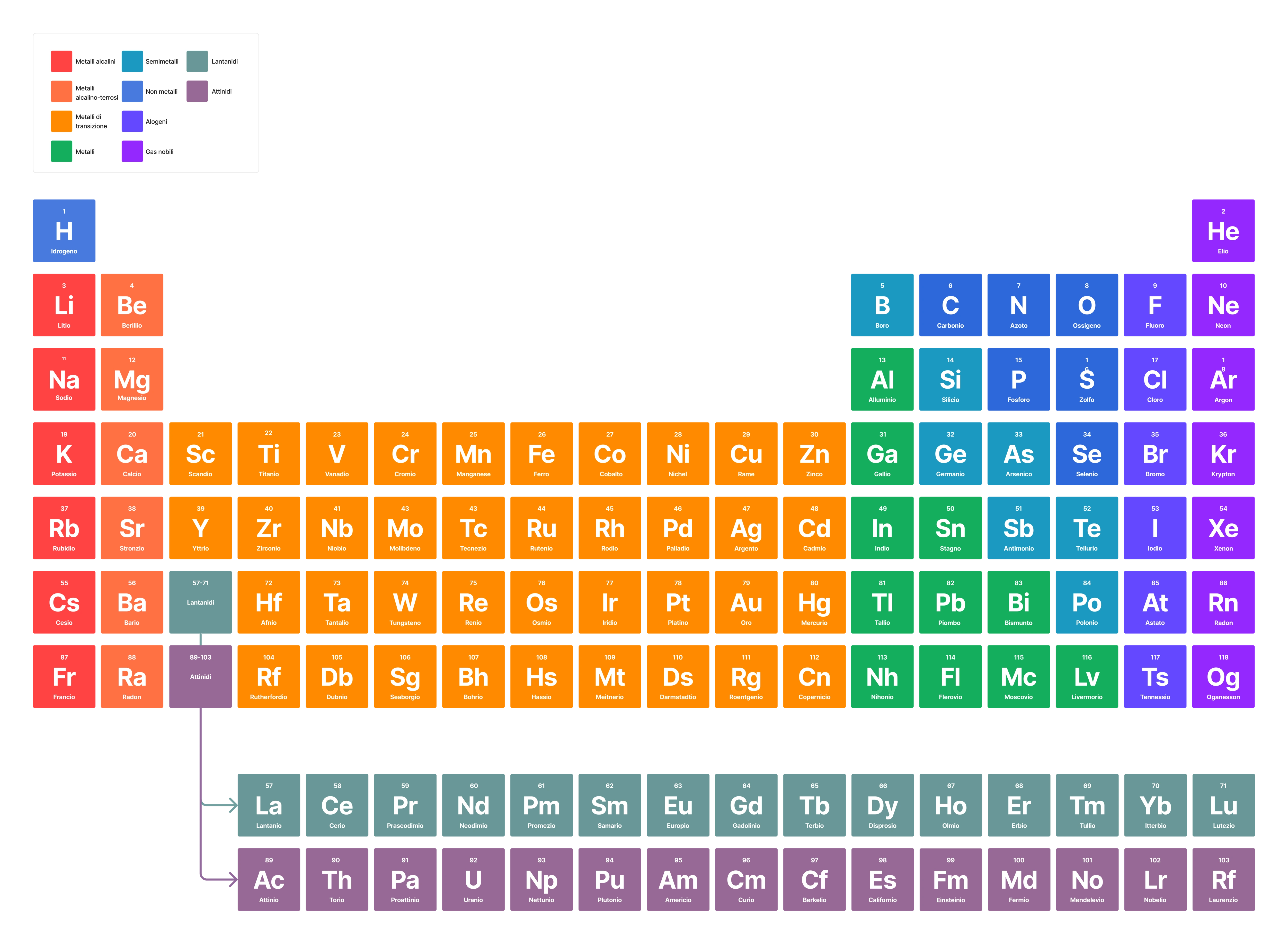
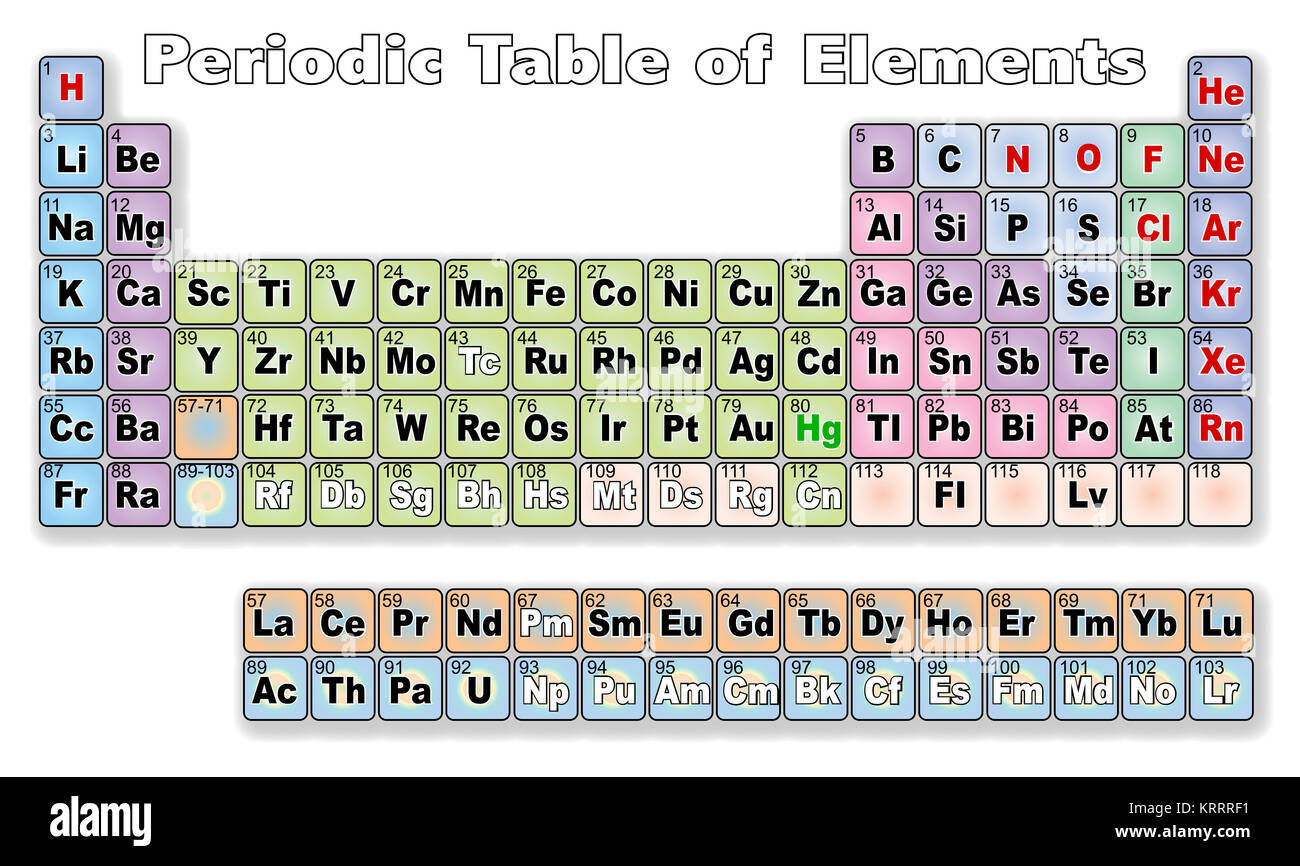
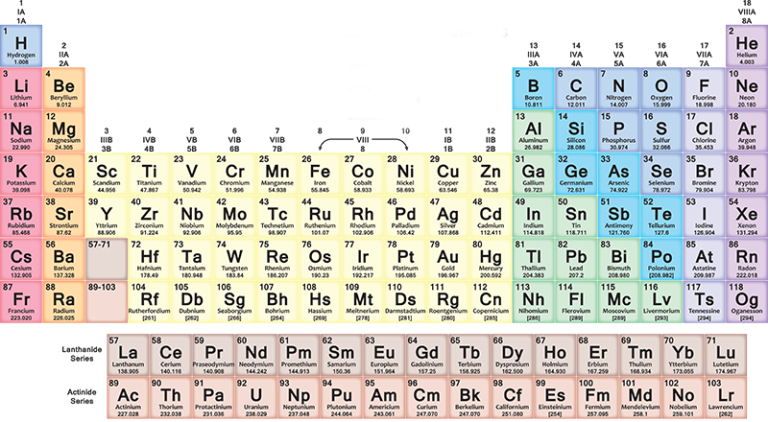
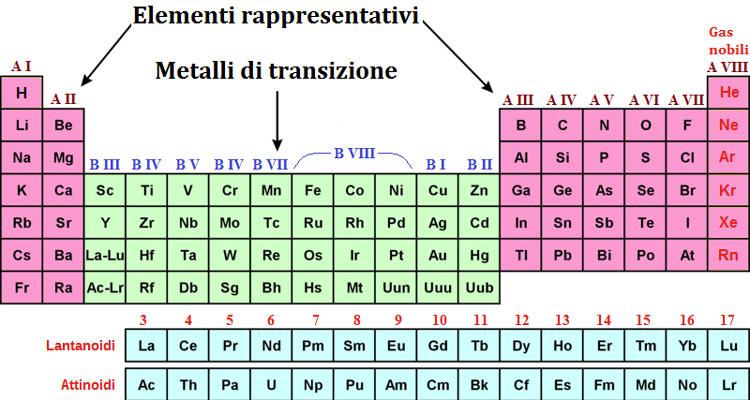
La tavola periodica è organizzata in 18 gruppi numerati da 1 a 18. Ogni gruppo comprende elementi che reagiscono in modo simile con altre sostanze. La posizione di un elemento in un gruppo fornisce informazioni cruciali sulla sua valenza e sulla sua capacità di formare legami chimici.
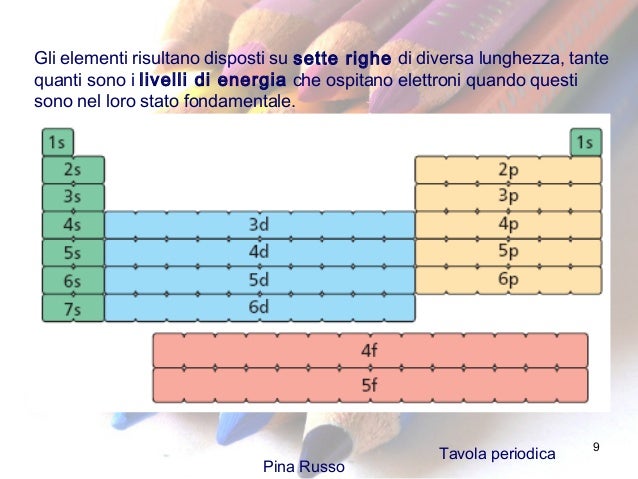
La configurazione elettronica esterna, cioè il numero di elettroni presenti nell'ultimo livello energetico di un atomo, è il fattore determinante per le proprietà chimiche di un elemento. Gli elementi dello stesso gruppo hanno lo stesso numero di elettroni di valenza, il che spiega la loro somiglianza chimica.
Must Read
Perché i Gruppi Sono Importanti?
Comprendere i gruppi della tavola periodica è fondamentale per diversi motivi:
- Previsione delle Proprietà Chimiche: Sapere a quale gruppo appartiene un elemento permette di prevederne le proprietà chimiche e la reattività.
- Comprensione dei Legami Chimici: I gruppi aiutano a capire come gli elementi si combinano per formare composti, in base alla loro tendenza a cedere, acquisire o condividere elettroni.
- Organizzazione delle Conoscenze Chimiche: La tavola periodica, con i suoi gruppi, fornisce un quadro organizzato per studiare la chimica, facilitando la memorizzazione e la comprensione delle proprietà degli elementi.
"La tavola periodica non è solo un elenco di elementi, ma un potente strumento per comprendere la relazione tra la struttura atomica e le proprietà chimiche." - Linus Pauling, vincitore del Premio Nobel per la Chimica.
L'organizzazione in gruppi permette di classificare gli elementi in famiglie con caratteristiche comuni. Ad esempio, il gruppo 1 è costituito dai metalli alcalini, elementi altamente reattivi che tendono a cedere un elettrone per formare ioni positivi. Il gruppo 17 è composto dagli alogeni, elementi altrettanto reattivi che tendono ad acquisire un elettrone per formare ioni negativi.
Impatto sull'Apprendimento degli Studenti
Lo studio dei gruppi della tavola periodica è cruciale per gli studenti di chimica. Ecco come influisce sulla loro formazione:

- Semplificazione dell'Apprendimento: Invece di memorizzare le proprietà di ogni singolo elemento, gli studenti possono imparare le caratteristiche generali di ciascun gruppo, riducendo il carico di memorizzazione.
- Risoluzione di Problemi: La conoscenza dei gruppi permette agli studenti di prevedere le reazioni chimiche e di risolvere problemi legati alla formazione di composti.
- Applicazione Pratica: La chimica è presente in molti aspetti della vita quotidiana. La comprensione dei gruppi permette agli studenti di capire i principi chimici che regolano fenomeni come la corrosione, la combustione e la produzione di materiali.
Un esercizio utile per gli studenti è quello di confrontare le proprietà di elementi appartenenti allo stesso gruppo, come il sodio (Na) e il potassio (K), entrambi metalli alcalini. Oppure, confrontare il cloro (Cl) e lo iodio (I), alogeni che si trovano nel gruppo 17. Questi confronti permettono di evidenziare le somiglianze e le differenze all'interno dello stesso gruppo e di comprendere come le proprietà variano lungo la tavola periodica.
In conclusione, la suddivisione della tavola periodica in 18 gruppi è una chiave di volta per la comprensione della chimica. Permette di organizzare le informazioni sugli elementi, di prevedere le loro proprietà e di capire come si comportano nelle reazioni chimiche. Per gli studenti, una solida comprensione dei gruppi è essenziale per affrontare con successo lo studio della chimica e per apprezzarne le applicazioni nel mondo che ci circonda.