Spettro Di Assorbimento E Di Emissione

Ciao! Capisco benissimo: gli spettri di assorbimento e di emissione possono sembrare un labirinto, soprattutto quando si studiano materie scientifiche. Sembra tutto così astratto e complicato! Ma non preoccuparti, siamo qui per rendere tutto più chiaro e, speriamo, anche un po' più interessante.
Cosa sono gli Spettri? Un'introduzione amichevole
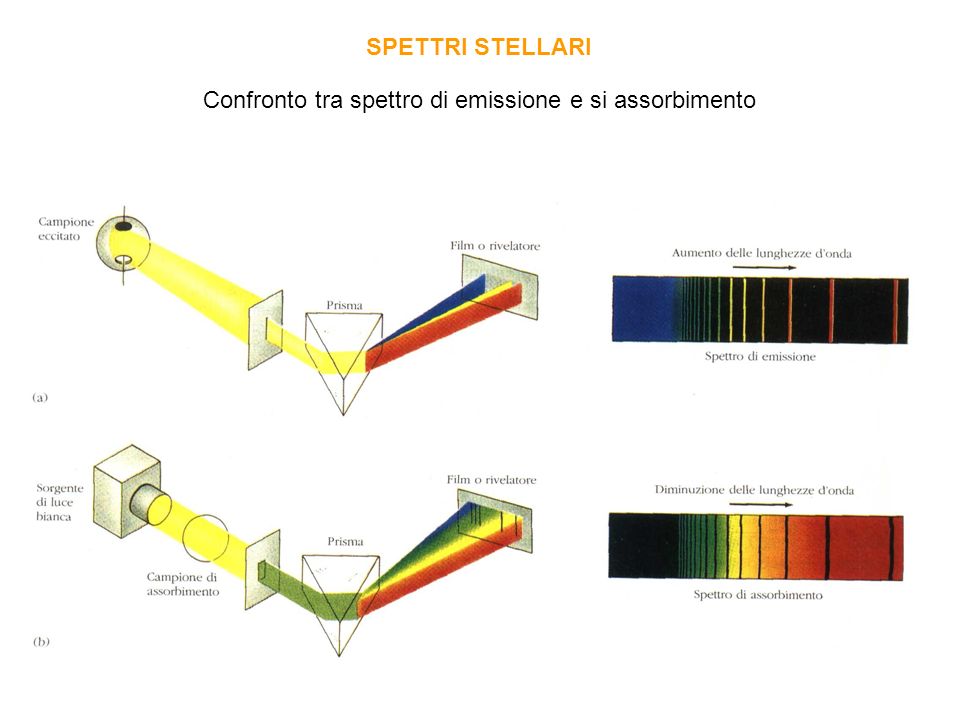
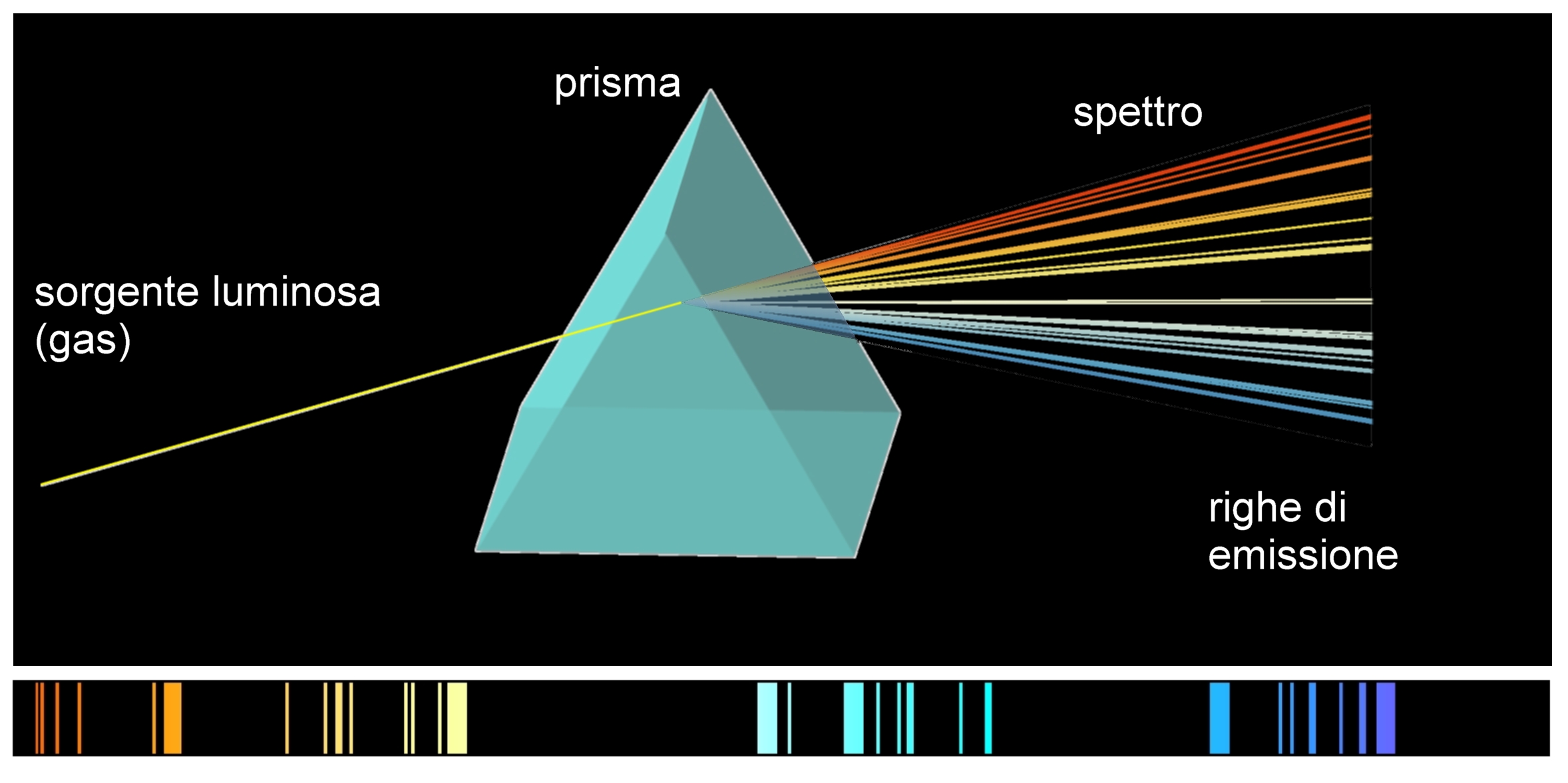
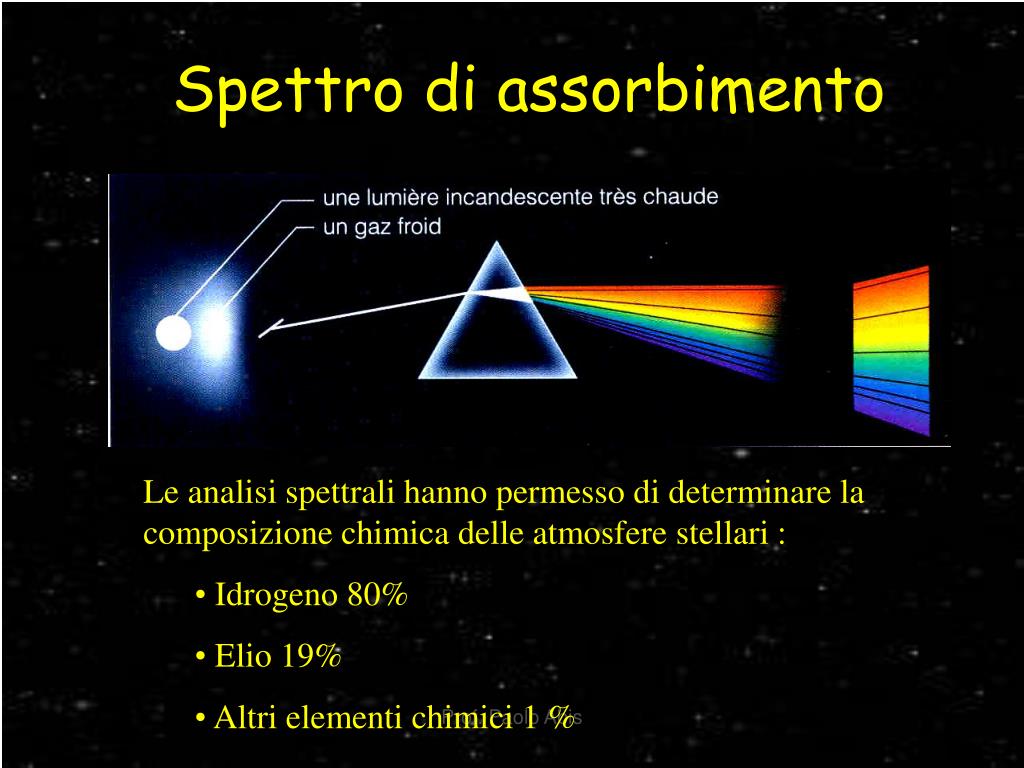
Immagina la luce del sole. A noi appare bianca, ma in realtà è composta da tanti colori, come quelli dell'arcobaleno. Uno spettro è proprio la separazione di questa luce nei suoi diversi colori, o meglio, nelle sue diverse lunghezze d'onda. Possiamo visualizzare lo spettro attraverso un prisma, che scompone la luce bianca nei suoi colori costituenti.
Lo Spettro di Emissione: quando gli atomi brillano
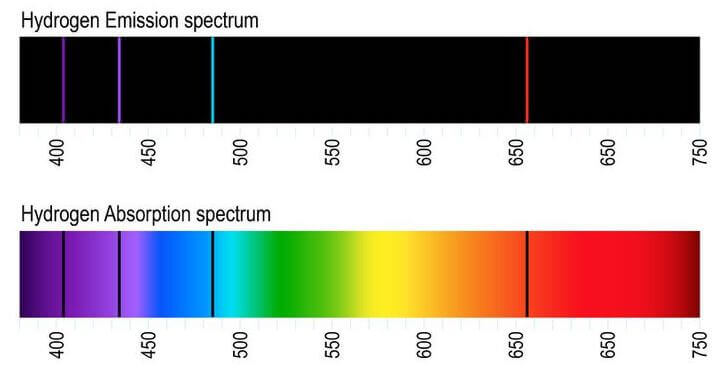
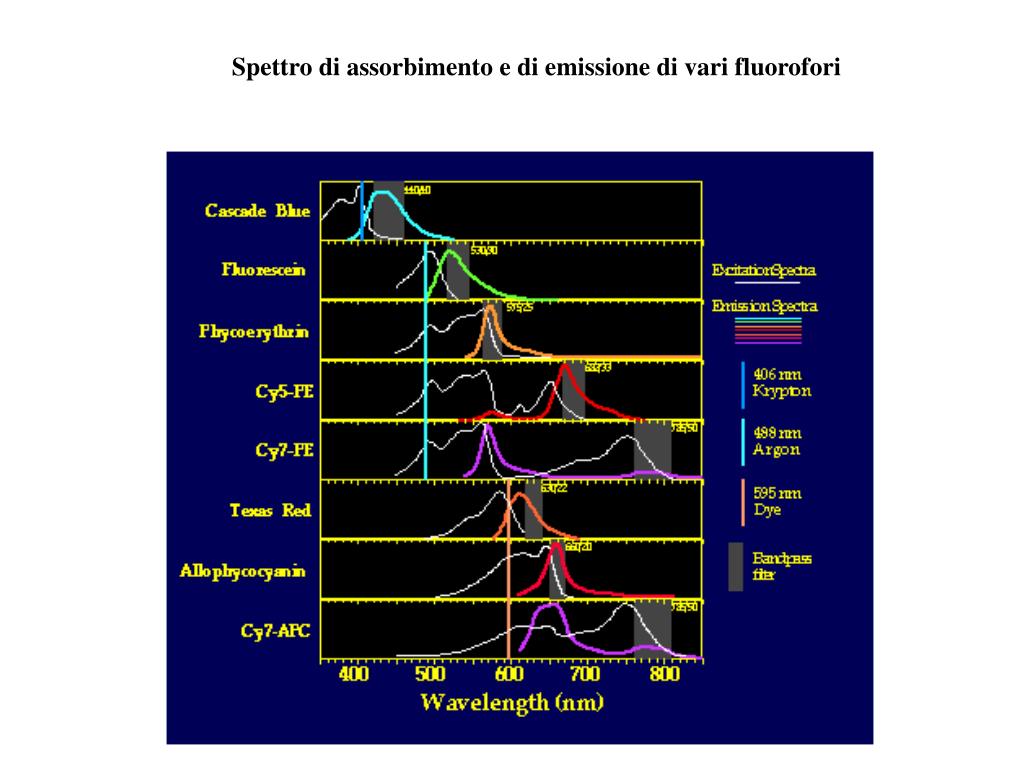
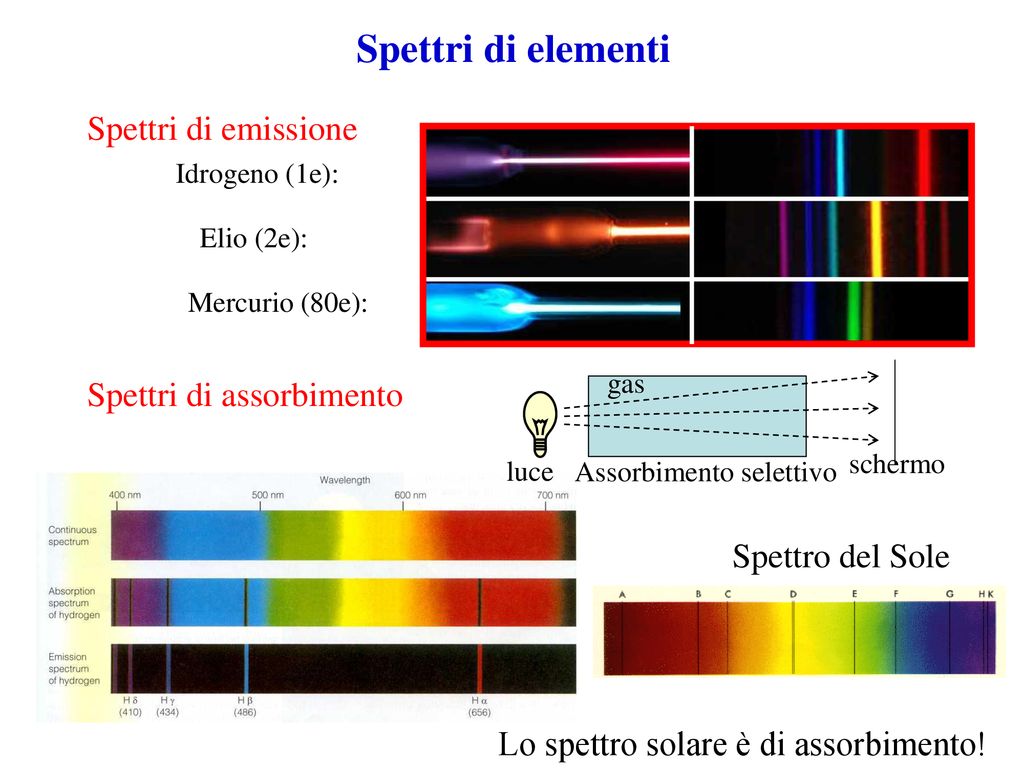
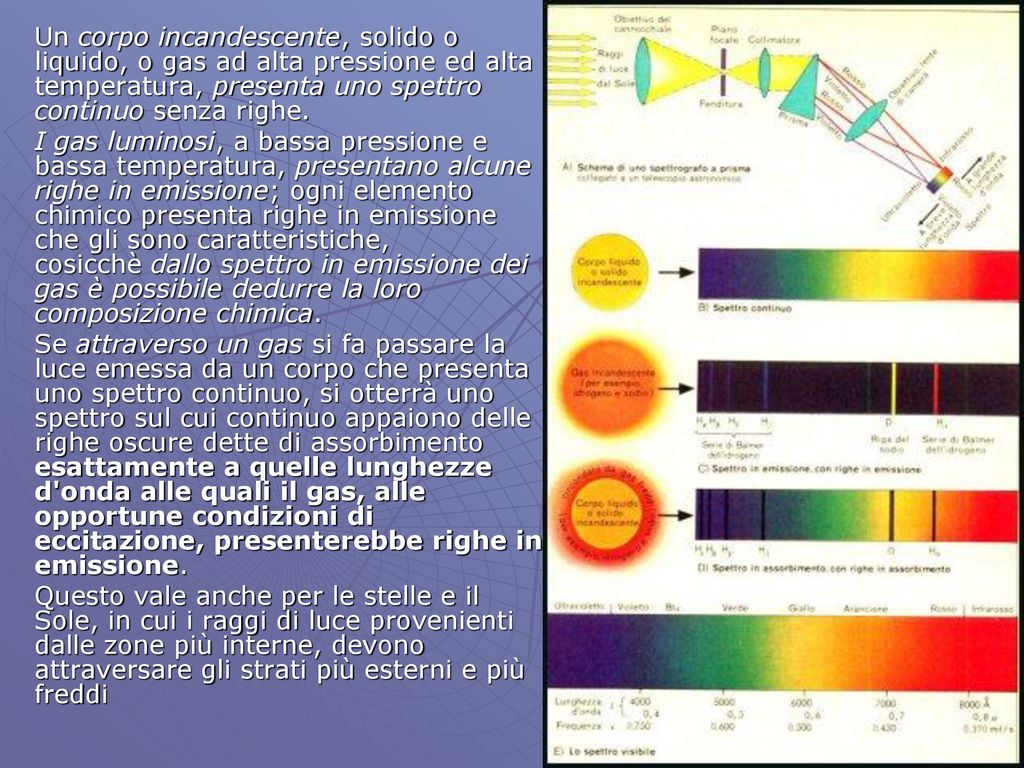
Lo spettro di emissione è come l'impronta digitale di un elemento chimico. Pensa a un fuoco d'artificio: ogni colore che vedi è prodotto dall'eccitazione degli atomi di un determinato elemento. Quando un atomo assorbe energia (ad esempio, dal calore), i suoi elettroni saltano a livelli energetici superiori. Quando ritornano al loro livello originale, emettono energia sotto forma di luce a specifiche lunghezze d'onda. Queste lunghezze d'onda sono uniche per ogni elemento e appaiono come linee colorate su sfondo nero nello spettro di emissione.
Must Read
Un esempio pratico: il neon. Quando la corrente elettrica passa attraverso il neon, gli atomi di neon emettono luce rossa, caratteristica del suo spettro di emissione.
Lo Spettro di Assorbimento: le "ombre" della luce
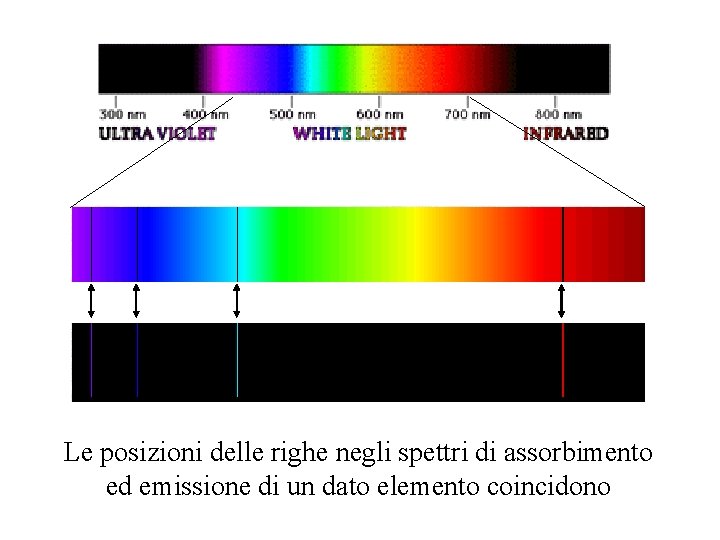
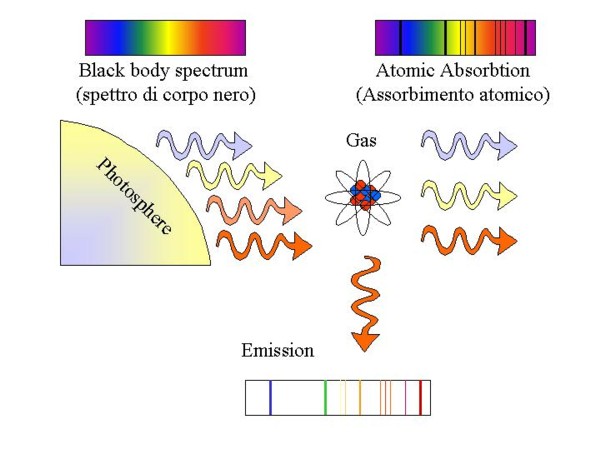
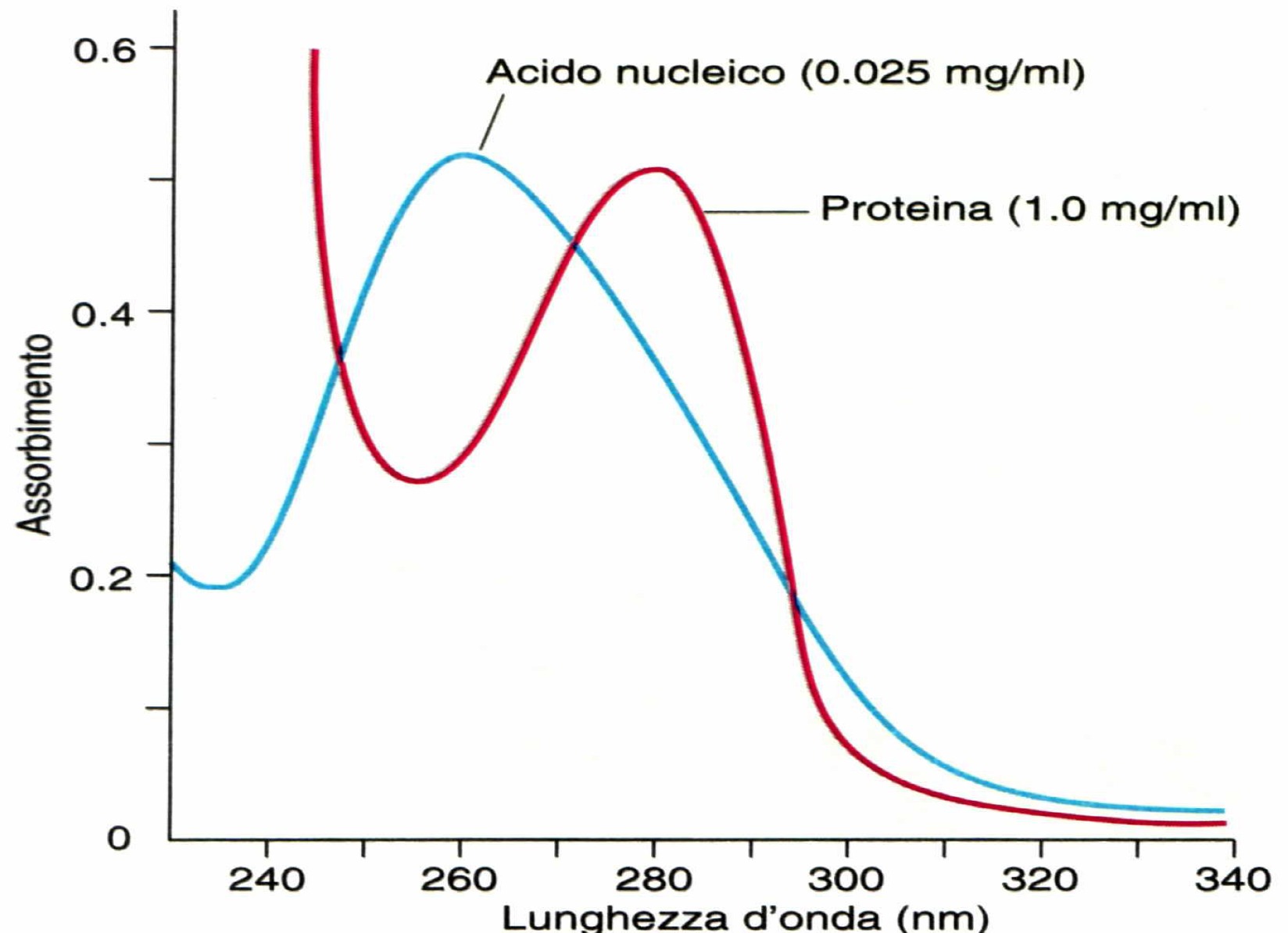
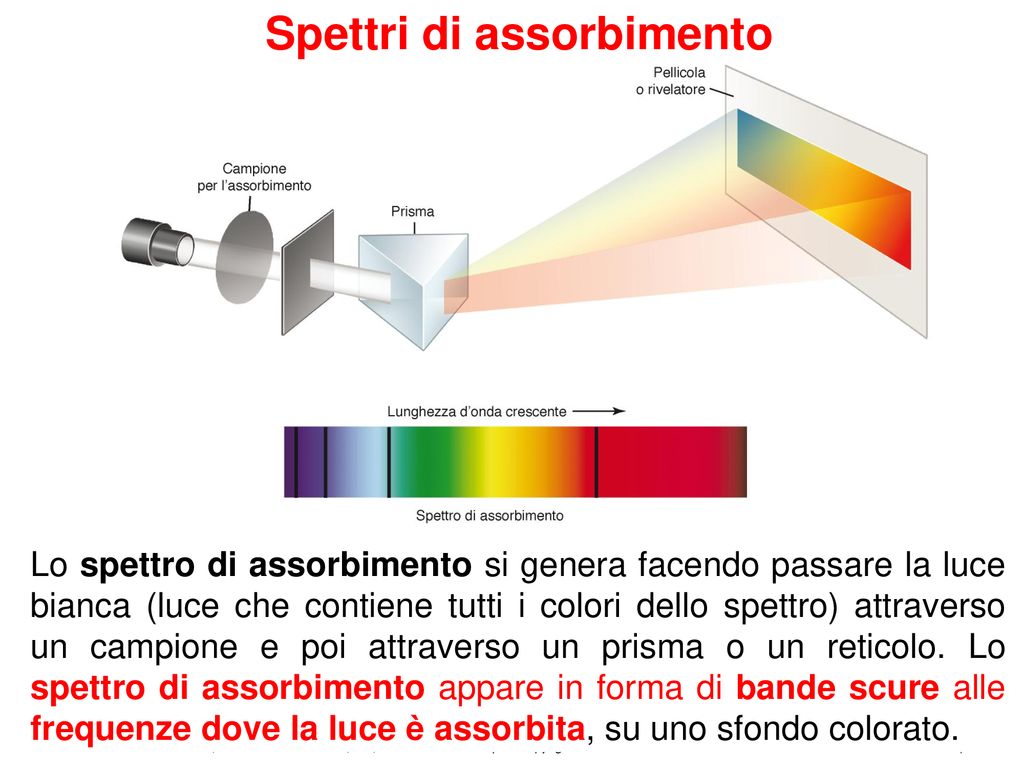
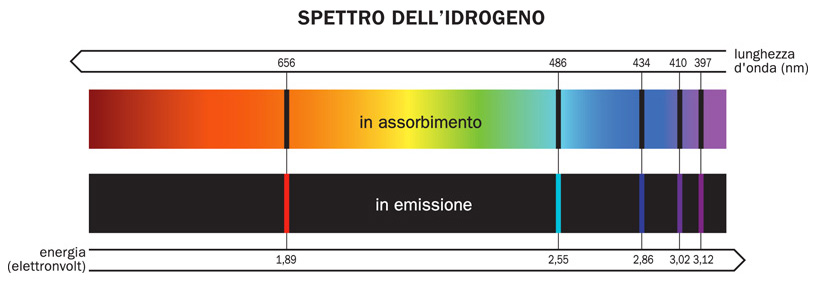
Lo spettro di assorbimento è l'opposto dello spettro di emissione. Invece di vedere linee colorate su sfondo nero, vediamo linee nere (o zone scure) su uno sfondo colorato, come un arcobaleno continuo. Questo accade quando la luce bianca (che contiene tutte le lunghezze d'onda) passa attraverso una sostanza. Gli atomi di quella sostanza assorbono specifiche lunghezze d'onda, corrispondenti a quelle che emetterebbero se fossero eccitati. Le lunghezze d'onda assorbite appaiono quindi come zone scure perché la luce a quelle lunghezze d'onda è stata "rimossa".
Immagina che la luce bianca sia un pacchetto regalo pieno di caramelle di tutti i colori. Se fai passare questo "pacchetto" attraverso un filtro che assorbe le caramelle rosse, vedrai che mancano le caramelle rosse. Questo è, in sostanza, quello che succede nello spettro di assorbimento.
Differenze chiave e come ricordarle
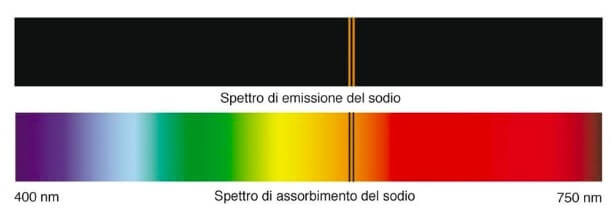
La differenza principale è che lo spettro di emissione mostra le lunghezze d'onda emesse da un elemento eccitato, mentre lo spettro di assorbimento mostra le lunghezze d'onda assorbite da un elemento. Un trucco per ricordarlo: pensa che "emissione" significa "uscita" (di luce), mentre "assorbimento" significa "entrata" (mancanza di luce).
Esempi Pratici e Consigli per lo Studio
- Astronomia: Gli astronomi usano gli spettri di assorbimento e di emissione per determinare la composizione chimica delle stelle e delle galassie. Analizzando la luce che riceviamo da questi oggetti celesti, possiamo capire quali elementi sono presenti e in quali quantità.
- Chimica: Gli spettri sono utilizzati per identificare sostanze sconosciute in laboratorio. Ogni elemento ha un suo spettro unico, quindi possiamo utilizzarlo come "firma" per identificarlo.
Consiglio: Quando studi, prova a disegnare schemi e diagrammi per visualizzare il processo di emissione e assorbimento. Crea delle flashcards con le definizioni e gli esempi. Non aver paura di chiedere aiuto al tuo professore o ai tuoi compagni di classe! Studiare in gruppo può rendere l'apprendimento più divertente e efficace.
Non mollare!
Gli spettri di assorbimento e di emissione possono sembrare ostici all'inizio, ma con un po' di pazienza e pratica, diventeranno più chiari. Ricorda, la scienza è un viaggio, non una destinazione. Goditi il processo di apprendimento e non aver paura di fare domande. Continua a esplorare e a scoprire le meraviglie del mondo che ti circonda!