Un Metallo Si Differenzia Da Un Non Metallo Perché

Nel mondo che ci circonda, la materia si manifesta in una miriade di forme, ognuna con le sue proprietà uniche. Una delle distinzioni fondamentali nella chimica e nella fisica dei materiali è quella tra metalli e non metalli. Questa differenza non è solo una questione di apparenza, ma riflette differenze profonde nella struttura atomica e nel comportamento fisico-chimico di queste due categorie di elementi.
Struttura Atomica e Legami Chimici: La Base della Differenza
La chiave per comprendere le differenze tra metalli e non metalli risiede nella loro struttura atomica, in particolare nella configurazione degli elettroni di valenza, ovvero gli elettroni presenti nel guscio elettronico più esterno. Questi elettroni sono responsabili della formazione dei legami chimici e determinano in gran parte le proprietà di un elemento.
Elettronegatività e Tendenza alla Formazione di Ioni
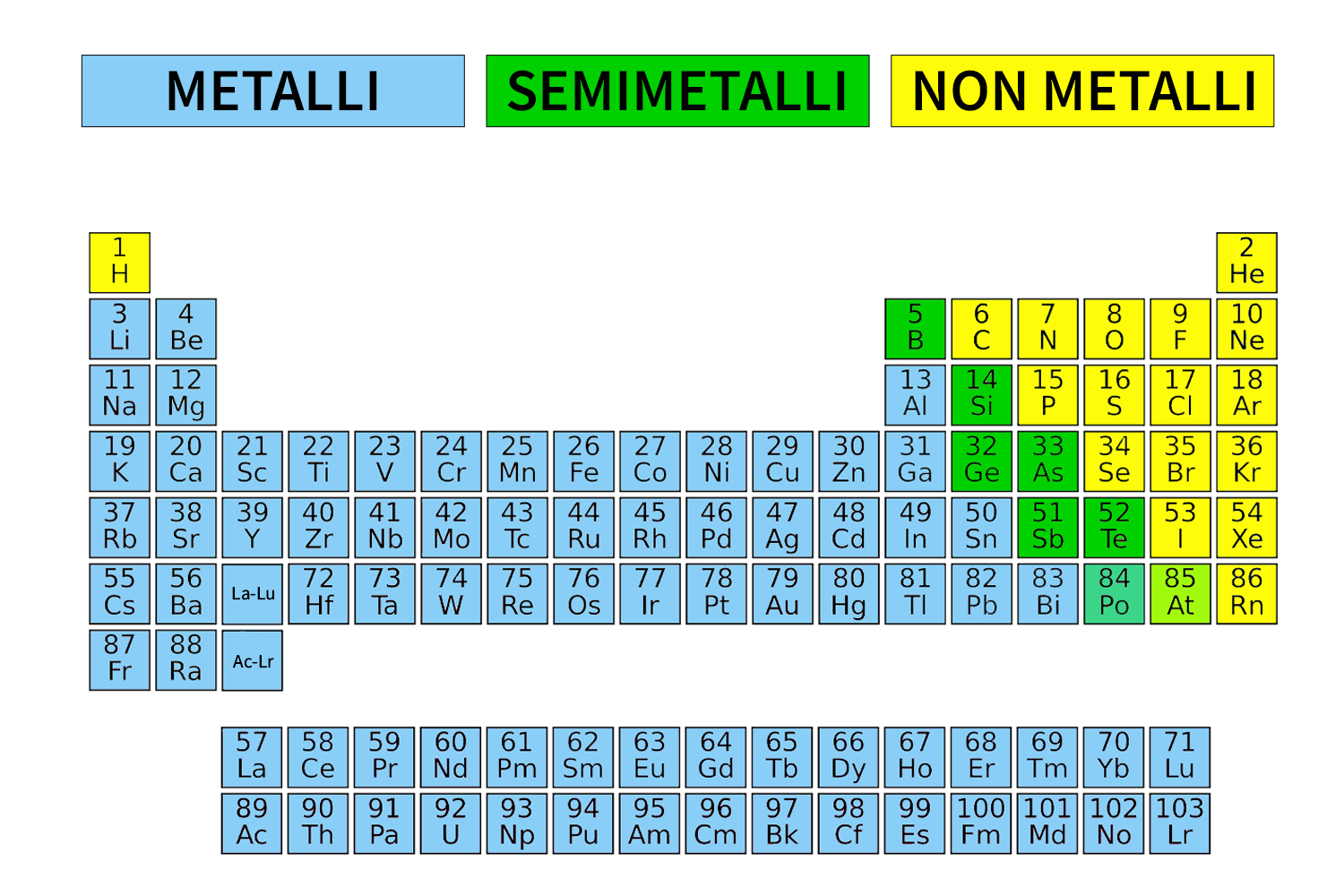
I metalli tendono ad avere una bassa elettronegatività, il che significa che hanno una scarsa capacità di attrarre elettroni. Di conseguenza, tendono a cedere elettroni per formare ioni positivi (cationi). Ad esempio, il sodio (Na) cede facilmente un elettrone per formare lo ione Na+, raggiungendo una configurazione elettronica più stabile.
Must Read
I non metalli, al contrario, hanno un'alta elettronegatività. Questo li rende inclini ad attrarre elettroni e a formare ioni negativi (anioni). Il cloro (Cl), ad esempio, accetta volentieri un elettrone per formare lo ione Cl-, completando il suo ottetto elettronico.
Legame Metallico vs Legami Covalenti e Ionici
La differenza nella tendenza a cedere o accettare elettroni porta alla formazione di tipi di legami chimici molto diversi. I metalli formano un legame metallico, in cui gli elettroni di valenza sono delocalizzati e si muovono liberamente attraverso una "nuvola" di elettroni che circonda i nuclei atomici. Questa delocalizzazione è responsabile di molte delle proprietà caratteristiche dei metalli.
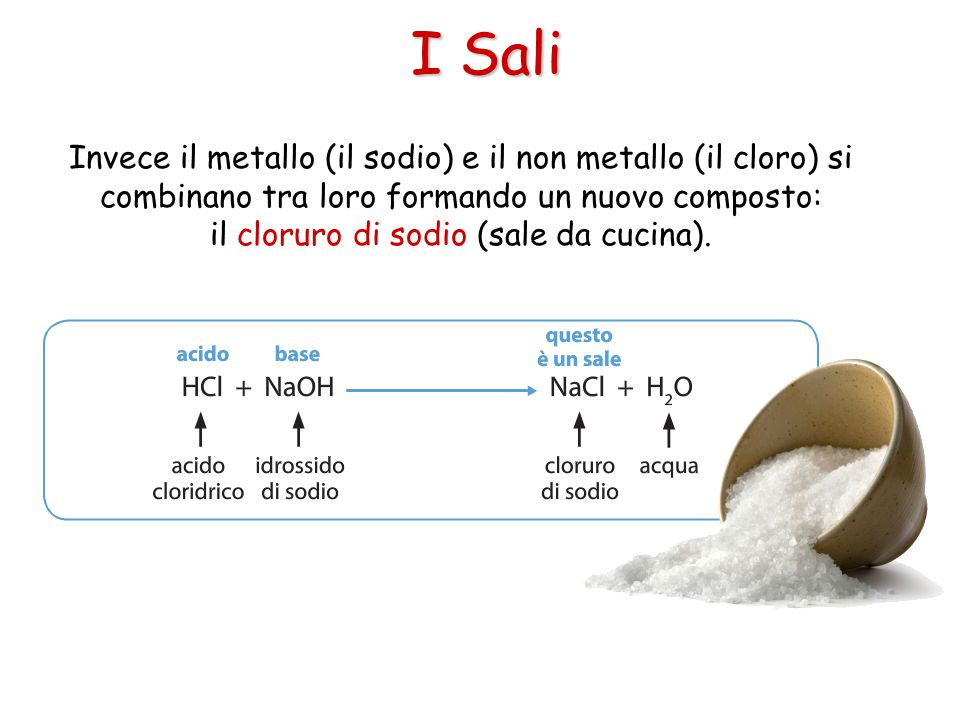
I non metalli, invece, tendono a formare legami covalenti, in cui gli atomi condividono elettroni per raggiungere una configurazione elettronica stabile. Possono anche formare legami ionici quando si combinano con metalli, come nel caso del cloruro di sodio (NaCl), in cui il sodio cede un elettrone al cloro.
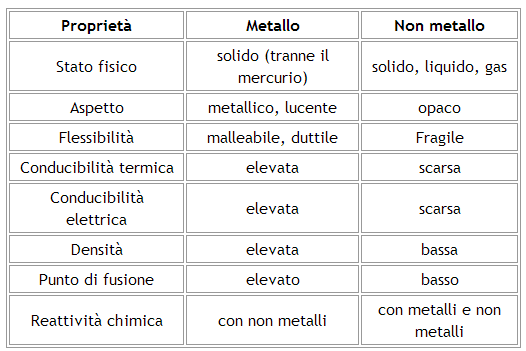
Proprietà Fisiche: Conseguenze della Struttura
Le differenze nella struttura atomica e nei legami chimici si traducono in notevoli differenze nelle proprietà fisiche di metalli e non metalli.
Conducibilità Elettrica e Termica
Una delle proprietà più distintive dei metalli è la loro eccellente conducibilità elettrica e termica. Questo è dovuto alla presenza degli elettroni delocalizzati che possono muoversi liberamente attraverso la struttura metallica, trasportando carica elettrica ed energia termica. Il rame (Cu) e l'argento (Ag) sono esempi classici di metalli con elevata conducibilità, utilizzati ampiamente in cablaggi elettrici e dispositivi elettronici.
I non metalli, al contrario, sono generalmente scarsi conduttori di elettricità e calore. Poiché i loro elettroni sono legati in legami covalenti o ionici, non sono liberi di muoversi e trasportare carica o energia. Esistono, tuttavia, eccezioni come il grafite, una forma allotropica del carbonio, che ha una buona conducibilità elettrica grazie alla sua struttura a strati con elettroni delocalizzati.
Lucentezza Metallica
La lucentezza metallica è un'altra proprietà caratteristica dei metalli. Quando la luce colpisce la superficie di un metallo, gli elettroni delocalizzati assorbono e riemettono la luce, conferendo al metallo un aspetto brillante e riflettente. L'oro (Au) e il platino (Pt) sono apprezzati per la loro lucentezza e resistenza alla corrosione, che li rende ideali per la gioielleria.
I non metalli, in generale, non possiedono lucentezza metallica. Possono essere opachi, trasparenti o traslucidi e presentare una varietà di colori. Lo zolfo (S), ad esempio, è un non metallo di colore giallo opaco.

Malleabilità e Duttilità
I metalli sono generalmente malleabili (possono essere modellati in lamine sottili) e duttili (possono essere tirati in fili). Questa proprietà è dovuta alla capacità degli atomi metallici di scorrere l'uno sull'altro senza rompere i legami, grazie alla delocalizzazione degli elettroni. Il ferro (Fe) è un esempio di metallo malleabile, utilizzato nella produzione di lamiere e strutture.
I non metalli sono generalmente fragili e si rompono facilmente quando vengono sottoposti a stress. I loro legami covalenti o ionici sono direzionali e non permettono agli atomi di scorrere liberamente. Il silicio (Si), un non metallo semiconduttore, è un esempio di materiale fragile utilizzato nell'industria elettronica.
Punti di Fusione ed Ebollizione
I metalli tendono ad avere punti di fusione ed ebollizione elevati, a causa della forza del legame metallico. Per rompere i legami e separare gli atomi metallici, è necessaria una grande quantità di energia. Il tungsteno (W), ad esempio, ha un punto di fusione estremamente alto (3422 °C) ed è utilizzato nei filamenti delle lampadine ad incandescenza.
I non metalli possono presentare punti di fusione ed ebollizione variabili, a seconda della forza dei legami intermolecolari. Alcuni non metalli, come i gas nobili, sono gassosi a temperatura ambiente e hanno punti di fusione ed ebollizione molto bassi. Altri, come il diamante (una forma allotropica del carbonio), hanno punti di fusione elevati a causa della forte rete di legami covalenti.
Proprietà Chimiche: Reattività e Comportamento
Le differenze tra metalli e non metalli si manifestano anche nelle loro proprietà chimiche, in particolare nella loro reattività con altre sostanze.

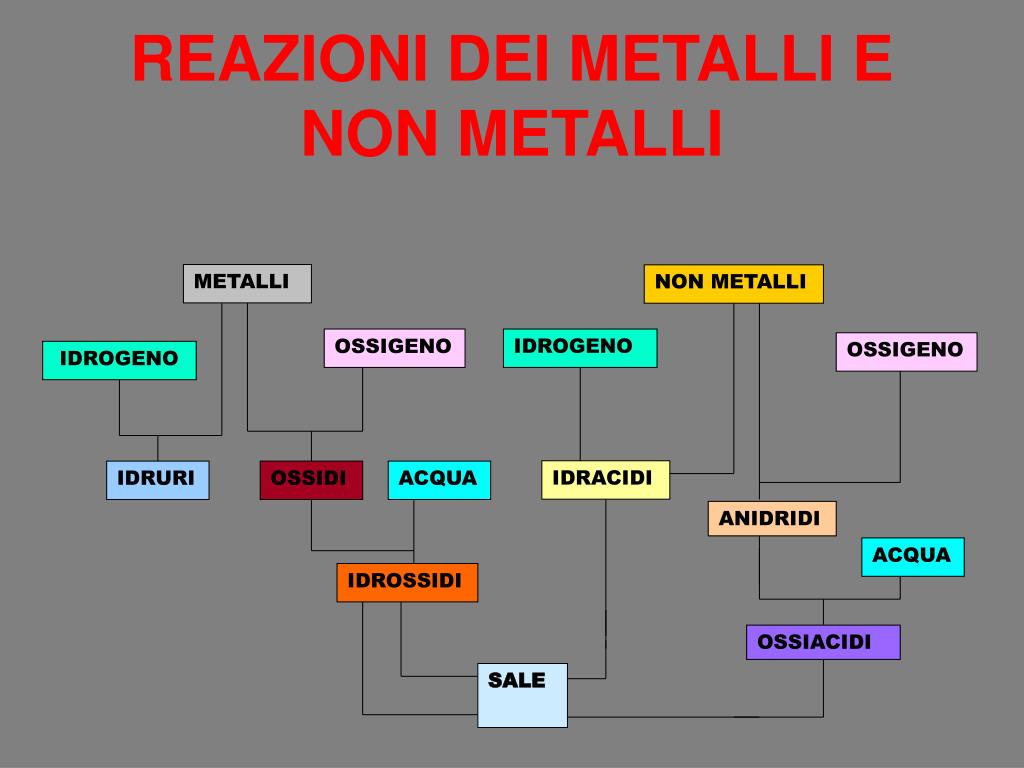
Reattività con l'Ossigeno
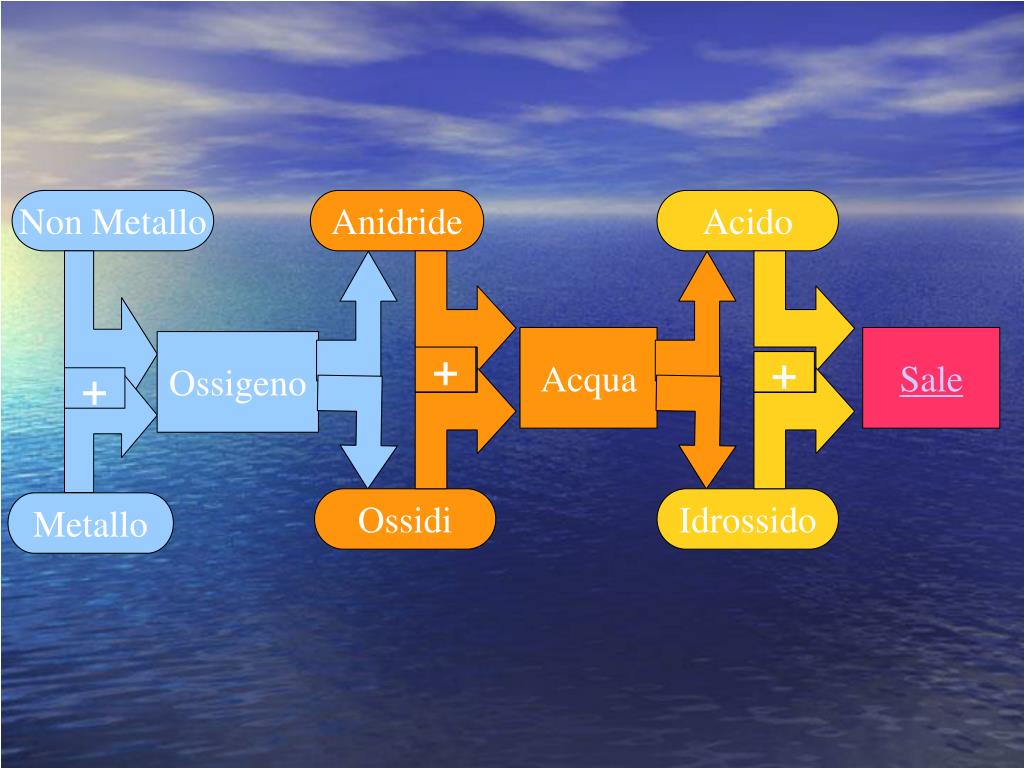
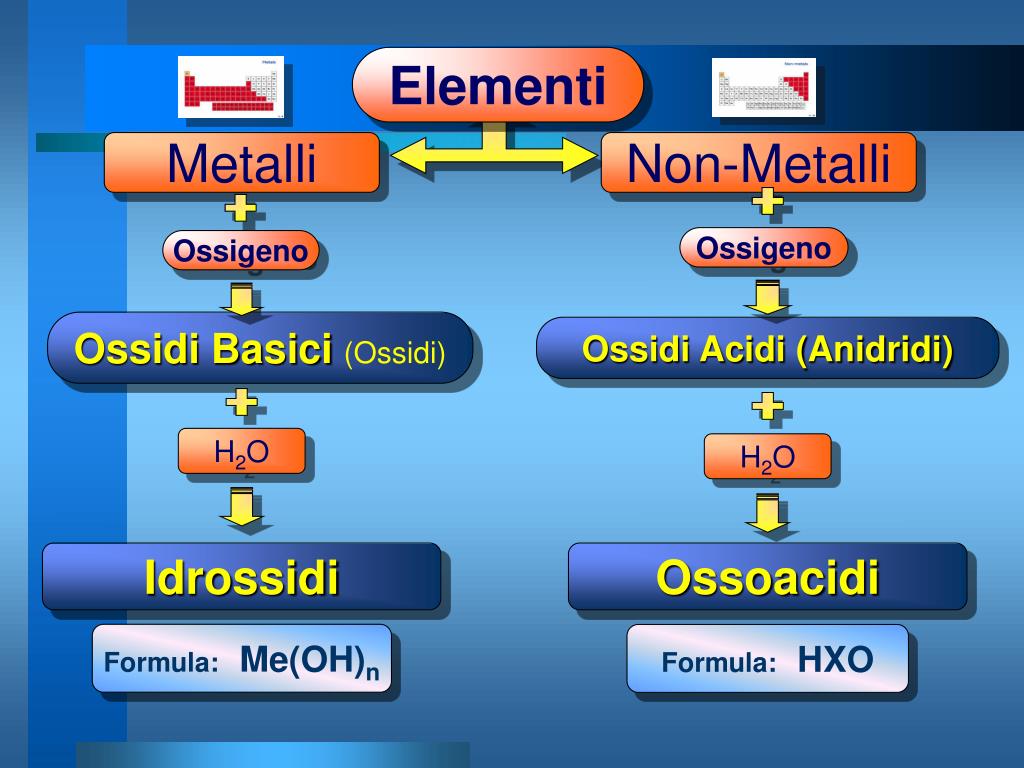
I metalli reagiscono con l'ossigeno per formare ossidi. La velocità e l'intensità di questa reazione variano a seconda del metallo. Alcuni metalli, come il sodio e il potassio, reagiscono violentemente con l'ossigeno, mentre altri, come l'oro e il platino, sono inerti. Il ferro, in presenza di ossigeno e umidità, si ossida formando la ruggine (ossido di ferro).
Anche i non metalli reagiscono con l'ossigeno per formare ossidi. Ad esempio, il carbonio brucia in presenza di ossigeno per formare anidride carbonica (CO2). Il tipo di ossido formato e le sue proprietà dipendono dal non metallo coinvolto.
Reattività con gli Acidi
Molti metalli reagiscono con gli acidi per formare sali e idrogeno gassoso. Il magnesio (Mg), ad esempio, reagisce con l'acido cloridrico (HCl) per formare cloruro di magnesio (MgCl2) e idrogeno (H2).
I non metalli, in generale, non reagiscono con gli acidi diluiti. Tuttavia, alcuni non metalli possono reagire con acidi forti o ossidanti in condizioni particolari.

Esempi e Applicazioni Pratiche
Le proprietà distintive dei metalli e dei non metalli li rendono adatti a una vasta gamma di applicazioni. Ecco alcuni esempi:
* Metalli: Utilizzati in costruzioni (acciaio), elettronica (rame, alluminio), trasporti (alluminio, titanio), gioielleria (oro, argento, platino) e medicina (titanio, acciaio inossidabile). * Non metalli: Utilizzati in agricoltura (azoto, fosforo), elettronica (silicio, germanio), chimica (carbonio, idrogeno, ossigeno), medicina (iodio, cloro) e materiali da costruzione (carbonio, silicio).L'industria moderna dipende fortemente dalle proprietà uniche di metalli e non metalli, e la ricerca continua a sviluppare nuovi materiali con proprietà ancora più avanzate.
Conclusione
La distinzione tra metalli e non metalli è fondamentale per comprendere la chimica e la fisica dei materiali. Le differenze nella struttura atomica, nei legami chimici e nelle proprietà fisiche e chimiche determinano le diverse applicazioni di questi elementi nella vita di tutti i giorni. Comprendere queste differenze non solo arricchisce la nostra conoscenza del mondo che ci circonda, ma ci permette anche di sviluppare nuovi materiali con proprietà specifiche per soddisfare le esigenze tecnologiche del futuro.
Approfondire la conoscenza delle proprietà dei materiali e delle loro applicazioni è essenziale per lo sviluppo di nuove tecnologie e per la risoluzione di sfide ambientali e sociali. Invitiamo quindi a continuare ad esplorare e a informarsi sulle ultime scoperte nel campo della scienza dei materiali, perché il futuro dipende dalla nostra capacità di innovare e di utilizzare le risorse in modo responsabile.





+nomenclatura+IUPAC.jpg)