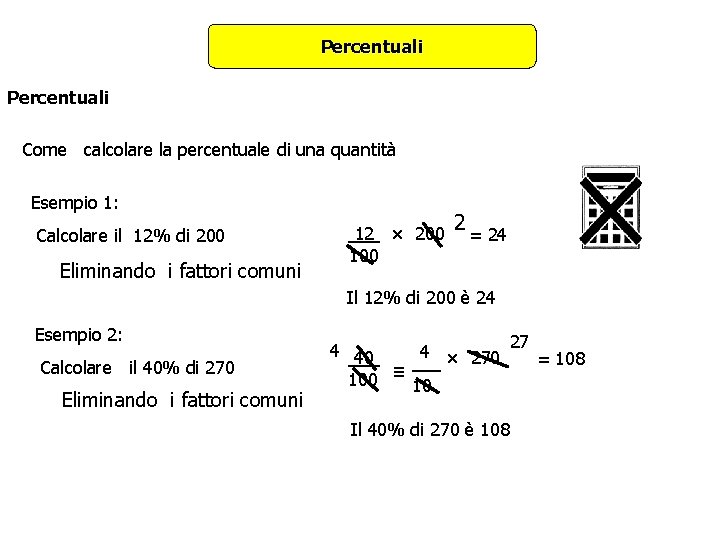
Esercizi Sulle Concentrazioni Percentuali Con Soluzioni

Ti sei mai trovato a fissare un'etichetta di un prodotto, chiedendoti cosa significassero tutti quei numeri e percentuali? Oppure, peggio ancora, ti sei bloccato durante un compito di chimica, incapace di risolvere un semplice esercizio sulle concentrazioni percentuali? Non sei solo! Molti studenti e persone comuni faticano a comprendere e manipolare questi concetti. Questo articolo è pensato proprio per te, per demistificare le concentrazioni percentuali e fornirti gli strumenti necessari per risolvere gli esercizi in modo efficace.
Cosa sono le Concentrazioni Percentuali?
Le concentrazioni percentuali esprimono la quantità di soluto presente in una soluzione, in relazione a 100 parti di soluzione. Immagina di avere una torta: la concentrazione percentuale ti dice quanta farina (soluto) c'è rispetto alla torta intera (soluzione).
Esistono principalmente tre tipi di concentrazioni percentuali:
Must Read
- Percentuale Massa/Massa (% m/m): Indica i grammi di soluto presenti in 100 grammi di soluzione.
- Percentuale Massa/Volume (% m/V): Indica i grammi di soluto presenti in 100 millilitri di soluzione.
- Percentuale Volume/Volume (% V/V): Indica i millilitri di soluto presenti in 100 millilitri di soluzione.
Capire la differenza tra queste tre tipologie è fondamentale per risolvere correttamente gli esercizi. Ad esempio, una soluzione al 5% m/m di sale in acqua significa che ci sono 5 grammi di sale in 100 grammi di soluzione (acqua + sale).
Esercizi Risolti Passo Passo
Ora passiamo alla parte pratica: analizziamo alcuni esercizi tipici e vediamo come risolverli.
Esercizio 1: Calcolo della Percentuale Massa/Massa (% m/m)
Problema: Si dissolvono 25 grammi di zucchero in 175 grammi di acqua. Calcola la concentrazione percentuale massa/massa della soluzione.
Soluzione:
- Identifica i dati:
- Massa del soluto (zucchero) = 25 g
- Massa del solvente (acqua) = 175 g
- Calcola la massa della soluzione: Massa della soluzione = Massa del soluto + Massa del solvente = 25 g + 175 g = 200 g
- Applica la formula: % m/m = (Massa del soluto / Massa della soluzione) * 100 = (25 g / 200 g) * 100 = 12.5%
Risposta: La concentrazione percentuale massa/massa della soluzione è del 12.5%.

Consiglio: Assicurati sempre di avere le unità di misura corrette (grammi per massa, millilitri per volume) prima di effettuare i calcoli.
Esercizio 2: Calcolo della Percentuale Massa/Volume (% m/V)
Problema: Si dissolvono 10 grammi di cloruro di sodio (NaCl) in acqua, ottenendo 250 ml di soluzione. Calcola la concentrazione percentuale massa/volume della soluzione.
Soluzione:
- Identifica i dati:
- Massa del soluto (NaCl) = 10 g
- Volume della soluzione = 250 ml
- Applica la formula: % m/V = (Massa del soluto / Volume della soluzione) * 100 = (10 g / 250 ml) * 100 = 4%
Risposta: La concentrazione percentuale massa/volume della soluzione è del 4%.
Attenzione: Non confondere il volume del solvente con il volume della soluzione. L'esercizio fornisce direttamente il volume della soluzione.

Esercizio 3: Calcolo della Percentuale Volume/Volume (% V/V)
Problema: Si mescolano 30 ml di etanolo con 70 ml di acqua. Calcola la concentrazione percentuale volume/volume della soluzione.
Soluzione:
- Identifica i dati:
- Volume del soluto (etanolo) = 30 ml
- Volume del solvente (acqua) = 70 ml
- Calcola il volume della soluzione: Volume della soluzione = Volume del soluto + Volume del solvente = 30 ml + 70 ml = 100 ml
- Applica la formula: % V/V = (Volume del soluto / Volume della soluzione) * 100 = (30 ml / 100 ml) * 100 = 30%
Risposta: La concentrazione percentuale volume/volume della soluzione è del 30%.
Ricorda: In questo caso, poiché si tratta di volumi, è importante sommarli per ottenere il volume totale della soluzione.
Esercizio 4: Calcolo della Massa del Soluto
Problema: Quanti grammi di glucosio sono necessari per preparare 500 g di una soluzione al 5% m/m?

Soluzione:
- Identifica i dati:
- % m/m = 5%
- Massa della soluzione = 500 g
- Rielabora la formula: Sappiamo che % m/m = (Massa del soluto / Massa della soluzione) * 100. Dobbiamo ricavare la Massa del soluto. Quindi: Massa del soluto = (% m/m * Massa della soluzione) / 100 = (5 * 500 g) / 100 = 25 g
Risposta: Sono necessari 25 grammi di glucosio.
Esercizio 5: Calcolo del Volume della Soluzione
Problema: Qual è il volume di una soluzione di etanolo al 20% v/v che contiene 40 ml di etanolo?
Soluzione:
- Identifica i dati:
- % v/v = 20%
- Volume del soluto (etanolo) = 40 ml
- Rielabora la formula: Sappiamo che % v/v = (Volume del soluto / Volume della soluzione) * 100. Dobbiamo ricavare il Volume della soluzione. Quindi: Volume della soluzione = (Volume del soluto * 100) / % v/v = (40 ml * 100) / 20 = 200 ml
Risposta: Il volume della soluzione è di 200 ml.

Consigli Utili per la Risoluzione degli Esercizi
- Leggi attentamente il testo: Identifica chiaramente cosa ti viene chiesto e quali dati ti vengono forniti.
- Scrivi i dati: Annota i valori noti con le relative unità di misura.
- Scegli la formula corretta: In base ai dati e a ciò che devi calcolare, seleziona la formula appropriata (% m/m, % m/V, % V/V).
- Rielabora le formule: Se devi calcolare la massa del soluto o il volume della soluzione, dovrai rielaborare la formula di base.
- Controlla le unità di misura: Assicurati che tutte le unità di misura siano coerenti (grammi, millilitri, etc.).
- Verifica il risultato: Controlla se il risultato ottenuto ha senso nel contesto del problema.
- Esercitati: Più ti eserciti, più diventerai bravo a risolvere gli esercizi sulle concentrazioni percentuali.
Perché è Importante Comprendere le Concentrazioni Percentuali?
La comprensione delle concentrazioni percentuali non è solo utile per superare un esame di chimica. Ha implicazioni pratiche in molti aspetti della vita quotidiana:
- Cucina: Molte ricette richiedono di misurare ingredienti in base alla concentrazione (ad esempio, soluzione salina).
- Medicina: I farmaci vengono spesso somministrati in base alla concentrazione (ad esempio, soluzione di antibiotico).
- Pulizia della casa: I prodotti per la pulizia indicano le concentrazioni dei principi attivi.
- Industria: La concentrazione è un parametro fondamentale nel controllo qualità dei prodotti.
- Agricoltura: I fertilizzanti e i pesticidi vengono diluiti a specifiche concentrazioni.
In sintesi, le concentrazioni percentuali sono uno strumento fondamentale per comprendere e manipolare il mondo che ci circonda.
Risorse Utili
Se hai bisogno di ulteriore aiuto, ecco alcune risorse utili:
- Libri di testo di chimica: Consulta il tuo libro di testo per una spiegazione più approfondita dei concetti.
- Siti web educativi: Molti siti web offrono lezioni e esercizi interattivi sulle concentrazioni.
- Tutoraggio: Se hai difficoltà, considera di chiedere aiuto a un tutor di chimica.
Con un po' di pratica e impegno, sarai in grado di padroneggiare le concentrazioni percentuali e risolvere gli esercizi con sicurezza!
Non arrenderti! La chimica può sembrare complicata all'inizio, ma con la giusta guida e un po' di perseveranza, diventerai un esperto!




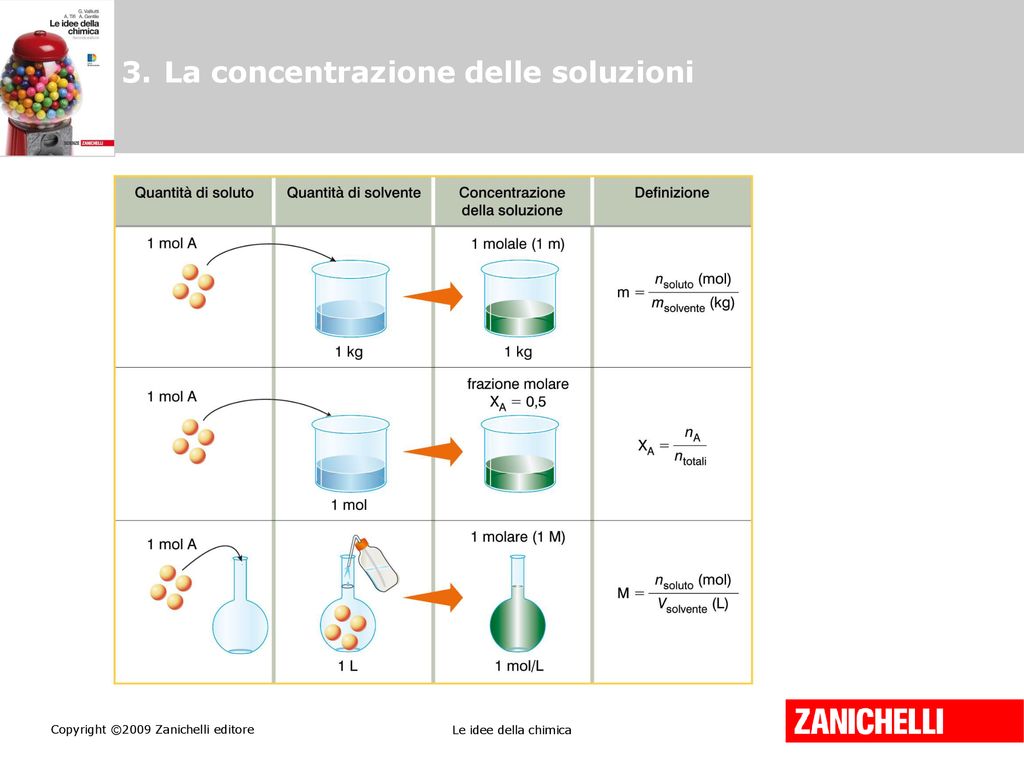



+indica+la+quantità+in+grammi+di+soluto+sciolta+in+100+mL+di+soluzione..jpg)